鸡源双抗平台NKCE的亲和力、表位覆盖范围及功能活性评估
2026-01-16 来源:生物制药小编 点击次数:258本文来源于微信公众: 生物制药小编 作者: wothman
T细胞接合器(TCE)一直是双抗领域中绕不开的一座大山。
在这种类型的双特异性抗体中,其中一端特异性通过其表面的CD3受体招募T细胞,另一端特异性通过肿瘤相关受体如EpCAM、CD19、CD20、BCMA、GPRC5D或DLL3结合癌细胞上的肿瘤相关抗原,从而实现将免疫细胞直接动员至肿瘤部位,在那里它们激活免疫细胞介导的抗肿瘤免疫反应,同时不伤害健康细胞。
自从2014年以来,TCE已经在血液肿瘤中获得了惊人的成功,虽然有效,但是安全和剂量限制毒性问题不可忽视。尤其是细胞因子释放综合征(CRS)常常会限制TCE双抗的使用。
与T细胞不同,NK细胞无需预先致敏即可快速识别并摧毁异常细胞,且副作用相对温和。采用NK细胞作为NK细胞接合器(NKCE)的策略已有多家Biotech企业尝试开发中。
最近OmniAb公司就在mAbs发布了该公司的NKCE平台技术,不过让人意想不到的是,这个技术平台以“鸡”这种动物的抗体作为技术核心之一。
通用轻链和鸡鼠平台
开发双特异性抗体面临一个主要技术难题:轻链错配。一个典型的抗体由两条重链和两条轻链组成。在实验室中同时生产两种不同的抗体“半成品”(分别针对A靶点和B靶点)时,它们的重链和轻链很容易随机组合,产生四种组合,由于目标只有一种,那么就产生了大量非目标产物,严重影响纯度和产量。
因此,科学界常常采用“共同轻链”(cmLC)技术,指的是靶向不同targets的不同抗体中所使用的轻链是一致的。这样,在组装针对不同靶点的抗体时,就完全避免了轻链的混乱配对,使得大规模生产高质量的双特异性抗体成为可能。
2017年获批的血友病药物emicizumab(Hemlibra®)就是首款成功的cmLC双抗。不过要如何快速筛选出这种cmLC双抗呢?
研究团队采用两个互补的动物平台,它们都能产生全人源序列的cmLC抗体。
OmniClic™ 和 OmniFlic®。它们都基于“通用轻链”(cmLC)技术,能产生完全人源序列的抗体,但宿主动物截然不同——前者使用基因工程改造的鸡,后者则使用大鼠。
哺乳动物(包括人类和大鼠)通过V(D)J重组机制产生抗体多样性,即从多个基因片段中随机拼接出不同的重链和轻链。
而鸡则采用一种名为“基因转换”(gene conversion)的独特机制:它们只有一个功能性重链V基因,但通过高频替换其可变区,从一系列伪基因中拷贝小片段DNA来对其进行修饰和多样化,也能生成高度多样化的抗体库。
这种进化上的“另类路径”,使得鸡对人类抗原可能产生与哺乳动物完全不同的识别方式,从而挖掘出全新的抗体表位。而大鼠等哺乳动物与人类更近缘,它们的免疫系统可能觉得NKp46似曾相识,从而跳过某些表位,限制了抗体表位多样性。研究假设:联合使用Clic和Flic平台,可以获得比任何单一平台更全面、互补的抗体库。
研究团队以NK细胞上的重要激活器NKp46为模型靶点开展实验。他们分别用NKp46蛋白免疫OmniClic鸡和OmniFlic大鼠,随后从单个B细胞中分离出特异性抗体,并对其亲和力、表位覆盖范围及功能活性进行全面评估。
鸡鼠互补
研究的核心突破在于对表位多样性的深度解析。表位是抗原上被抗体识别的具体区域,不同表位的抗体可能触发不同的生物学效应。拥有针对多个不同表位的抗体,对于设计最优化的疗法至关重要。
团队采用高通量表面等离子共振(SPR)技术,对119个抗体克隆进行了“表位分箱”(epitope binning)分析——即测试任意两个抗体是否能同时结合NKp46,若不能,则说明它们识别的是重叠或邻近的表位。
研究结果显示:OmniFlic大鼠平台成功重现了文献中已知的四个经典NKp46抗体(Innate-1至4)所对应的全部四个表位群;
而OmniClic鸡平台虽仅重现其中一个(Innate-2),却发现了六个全新、鼠类平台无法产生的独特表位群,这证明了研究人员最初的假设,即使用鸡源平台能够提供一个完全不同的视角来更好找到新表位;
两个平台共识别出14个不同的表位社区(communities),其中仅有2个为共享,其余均为各自独有。

随后,研究人员还利用氢氘交换质谱(HDX-MS)这项技术通过测量蛋白质主链氢原子与溶液中氘原子的交换速率,定位抗体结合后受保护的区域。
结果验证了SPR分箱结果的可靠性。如Com-4C1能结合L39-F62区域,与Innate-4基准重叠。Com-3(如dAb D01)可结合H108-F121,位于蛋白远端的独特口袋。Com-2a以L135-Y147为核心,但成员间有细微差异。最引人注目的是C08——一个Clic抗体,拥有从未见过的独特表位(Com-2U),直接与Innate-1基准竞争,这表明它结合了一个关键的功能区域。
ADCC实战检验
研究人员将三个代表性抗体(分别来自鸡和鼠的不同表位群)改造为EGFR/NKp46双特异性抗体,采用Morrison格式(2+2四价结构,两个NKp46臂和两个EGFR臂)。这种四聚体结构像分子交联剂,强制NK细胞与肿瘤细胞亲密接触。利用经典的A549肺癌细胞系和人源NK细胞进行抗体依赖性细胞毒性(ADCC)实验。
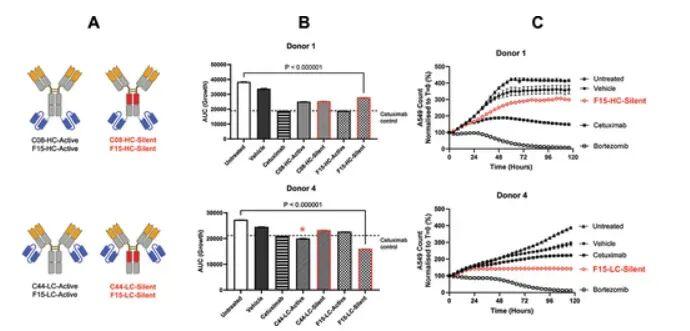
他们测试了两种配置:将EGFR臂连接在NKp46抗体的重链或轻链末端,并使用活性Fc(结合CD16a)或“沉默”Fc。
他们发现了以下三种规律:
①所有测试的双抗均能在无Fc效应功能(即沉默Fc,排除CD16a通路干扰)的情况下介导肿瘤杀伤,证明单纯激活NKp46就足以触发NK细胞杀伤活性。
②活性Fc未增效,最佳表现者反而是Flic来源的F15的沉默Fc轻链连接版本,显著优于活性Fc版本,甚至超过西妥昔单抗对照。
③轻链大于重链,将EGFR-scFv连接在抗体轻链末端(LC-tethered)的格式,比连接在重链末端(HC-tethered)更有效。
传统上,科学家通常认为激活FcγRIIIa(CD16a)能增强ADCC。但在此系统中,同时激活NKp46和CD16a反而可能因空间位阻或信号干扰而降低效率。
这表明,在设计NKCE时,还需要考虑分子几何结构与价态问题,并非激活越多就越好。
总结
总的来说,这项研究证明了OmniClic平台可以作为啮齿类系统的可行替代,同时也说明了NKCE开发的复杂挑战,还有更多的基础研究有待开发,期望未来NKCE相关平台能有更好发展。

