人间充质干细胞外泌体高效培养与分离指南
2026-04-02 来源:本站 点击次数:19人间充质干细胞(MSC)来源广泛(脐带、骨髓、脂肪等),其分泌的外泌体富含蛋白质、脂质、核酸等生物活性物质,在抗炎修复、免疫调节、疾病诊断与治疗等领域具有极高的科研与临床价值。但在实际实验中,很多科研人员常常面临外泌体培养效率低、分离纯度不高、活性流失等问题,严重影响实验进度与数据可靠性。

本文结合多年实验经验与行业规范,整理出一套实用的人间充质干细胞外泌体高效培养与分离指南,从细胞准备、培养条件优化、外泌体分离提取到纯度鉴定,全流程拆解关键要点,助力科研人员少走弯路,高效获取高纯度、高活性的外泌体,同时结合合规要求,推荐适配的核心试剂,兼顾实验效率与合规性。
一、前期准备:细胞筛选与试剂选择,筑牢实验基础
外泌体的培养与分离,前期准备是关键,核心在于“优质细胞+适配试剂”,两者直接决定外泌体的分泌量与纯度。
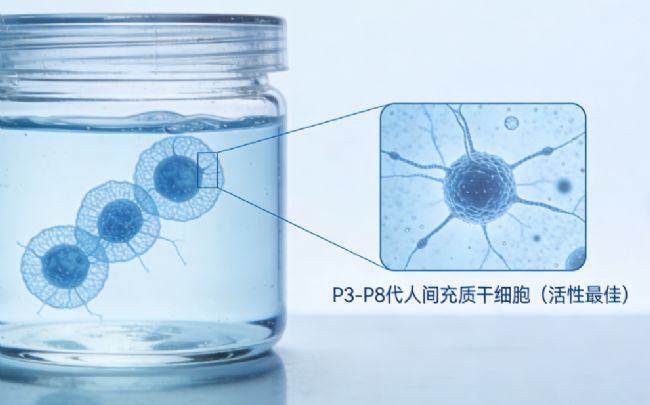
1. 细胞筛选:优先选择P3-P8代的人间充质干细胞,此时细胞活性强、增殖稳定,外泌体分泌量处于峰值,且细胞表型稳定,能最大程度保证外泌体的生物学活性。避免使用传代过多的细胞,此类细胞增殖能力下降,外泌体分泌量减少,且可能出现表型异常,影响实验结果。
2. 试剂选择:这是实验成功的核心,尤其是培养基的选择,直接影响外泌体的纯度与实验合规性。传统含血清培养基存在致命弊端——血清中含有大量外源外泌体和杂蛋白,会严重干扰后续外泌体的分离提取与鉴定,且不符合818号令中“外泌体制备所用培养基不含血清及替代物”的合规要求,无法用于临床相关研究。


建议选择专用的无血清外泌体培养基,如埃泽思生物(Applied Cell®)自主研发的人间充质干细胞外泌体无血清培养基,其核心优势的是无外源外泌体干扰,采用成分清晰可控的配方,不含动物源成分、无血清添加,从源头杜绝外源干扰,同时能稳定维持人间充质干细胞的活性与增殖能力,促进外泌体高效分泌,完美契合科研与临床转化的合规要求,适配脐带、骨髓、脂肪等多种来源的间充质干细胞。
此外,需提前准备无菌PBS、胰酶、超速离心管、滤膜(0.22μm)、外泌体提取试剂等,所有试剂与耗材需提前灭菌处理,避免污染。

二、高效培养:优化培养条件,提升外泌体分泌量

人间充质干细胞的培养条件,直接影响外泌体的分泌效率,需重点优化以下4个方面,兼顾细胞生长与外泌体分泌:

1. 接种密度:将筛选好的人间充质干细胞,以1×10^5 - 2×10^5 cells/cm²的密度接种至培养瓶中,接种密度过高会导致细胞过度拥挤,影响细胞活性与外泌体分泌;密度过低则会延长细胞增殖周期,降低实验效率,此密度范围能让细胞快速贴壁、增殖,同时维持较高的外泌体分泌量。
2. 培养环境:采用37℃、5% CO₂的恒温培养箱,保持培养环境的湿度稳定,避免温度、CO₂浓度波动,否则会影响细胞代谢,进而减少外泌体分泌。同时,培养过程中避免频繁开盖,减少污染风险。
3. 培养基更换:接种后24小时,更换新鲜的埃泽思生物人间充质干细胞外泌体无血清培养基,去除未贴壁的死细胞与杂质;后续每48小时更换一次培养基,确保细胞生长所需的营养充足,同时及时收集含外泌体的培养基,避免外泌体在培养基中停留过久,导致活性流失。
4. 培养时长:常规培养48-72小时后,细胞融合度达到80%-90%时,外泌体分泌量达到峰值,此时可收集培养基,进行外泌体分离提取。若培养时间过长,细胞会进入衰老期,外泌体分泌量下降,且可能出现细胞脱落,影响外泌体纯度。
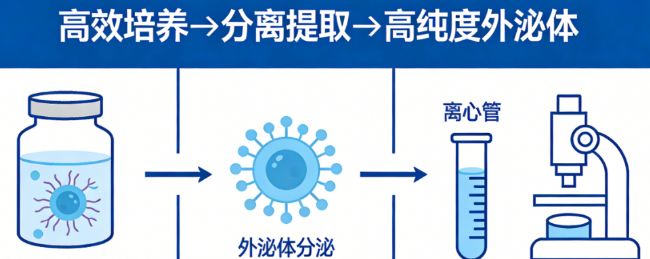
三、分离提取:分步操作,获取高纯度外泌体
外泌体的分离提取核心是“去除杂质、保留活性”,结合实验室常规设备,推荐采用“离心+过滤”的经典方法,操作简单、性价比高,适合大多数科研实验室,
具体步骤如下:
具体步骤如下:
1. 初步离心去杂质:将收集到的含外泌体的培养基,放入离心管中,4℃、300×g离心10分钟,去除培养基中的死细胞与大体积杂质;随后将上清液转移至新的离心管,4℃、2000×g离心20分钟,进一步去除细胞碎片与小颗粒杂质,避免杂质干扰后续外泌体分离。
2. 过滤除杂:将离心后的上清液,通过0.22μm滤膜过滤,去除直径大于0.22μm的杂蛋白、脂质体等杂质,此时上清液中主要含有外泌体(直径30-150nm),过滤后需注意保持上清液无菌。
3. 超速离心获取外泌体:将过滤后的上清液转移至超速离心管中,4℃、100000×g超速离心70分钟,使外泌体沉淀;离心结束后,弃去上清液,加入适量无菌PBS,轻轻吹打沉淀,使外泌体重悬,避免剧烈吹打,防止外泌体膜破裂,影响活性。
4. 二次离心纯化:将重悬后的外泌体溶液,再次进行4℃、100000×g超速离心70分钟,进一步去除残留的杂蛋白与杂质,获得高纯度的外泌体;离心结束后,弃去上清液,用少量无菌PBS重悬,置于-80℃冰箱保存,备用。
注意:整个离心过程需保持4℃低温,减少外泌体活性流失;超速离心管需提前平衡,避免离心过程中出现破损;所有操作需在无菌环境下进行,防止污染。
四、纯度鉴定:3步验证,确保实验可靠性
分离提取后的外泌体,需进行纯度与活性鉴定,避免因杂质过多影响实验结果,推荐3种常用鉴定方法,操作简单、结果可靠:
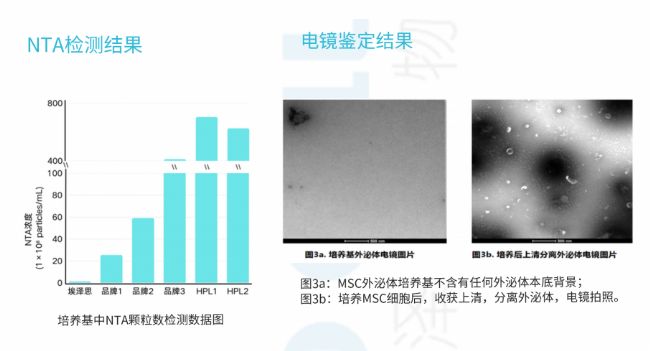
1. 形态鉴定:采用透射电子显微镜(TEM)观察外泌体形态,合格的外泌体呈圆形或椭圆形,具有典型的双层膜结构,直径在30-150nm之间,无明显杂质。


2. 粒径分析:采用纳米颗粒跟踪分析(NTA)检测外泌体的粒径分布,合格的外泌体粒径分布均匀,峰值集中在30-150nm,无明显大粒径杂质峰。
3. 标志物检测:采用Western Blot检测外泌体特征标志物,如CD63、CD81、TSG101等,若能检测到这些标志物,且无明显杂带,说明外泌体纯度达标,且保留了完整的生物学活性。
五、实验注意事项:规避常见误区,提升实验成功率


1. 全程无菌操作:外泌体对污染极为敏感,从细胞培养到外泌体分离、鉴定,所有试剂、耗材、操作环境均需无菌,避免细菌、支原体污染,否则会导致外泌体活性流失、实验失败。
2. 避免外源干扰:坚决杜绝使用含血清培养基,选择无外源外泌体干扰的专用培养基(如埃泽思生物相关产品),同时避免使用含有外源外泌体的试剂,从源头保证外泌体纯度。
3. 控制离心条件:超速离心的转速、时间、温度需严格把控,转速过低、时间不足会导致外泌体无法完全沉淀;转速过高、时间过长会导致外泌体膜破裂,影响活性。
4. 及时保存与使用:分离后的外泌体需置于-80℃冰箱保存,避免反复冻融,反复冻融会导致外泌体膜破裂、活性流失;保存时间不宜过长,建议1个月内使用完毕。
以上就是人间充质干细胞外泌体高效培养与分离的完整指南,核心在于“优质细胞+专用无血清培养基+规范操作”。其中,培养基的选择是关键,埃泽思生物(Applied Cell®)人间充质干细胞外泌体无血清培养基,无外源外泌体干扰、合规稳定,能有效提升外泌体分泌量与纯度,适配大多数科研与临床前研究场景。
如果你在人间充质干细胞外泌体培养、分离过程中,遇到分泌量低、纯度不高、外源干扰等问题,关注埃泽思生物,私信回复“培养指南”,即可获取详细的实验操作视频与产品试用申请,同时可获得专业技术人员的个性化指导,助力你的实验高效推进、少走弯路。
埃泽思服务热线:0512-82080010 18018560881 网址:www.applycell.cn
埃泽思服务热线:0512-82080010 18018560881 网址:www.applycell.cn
相关文章
更多 >

