小分子降解剂分子胶的应用
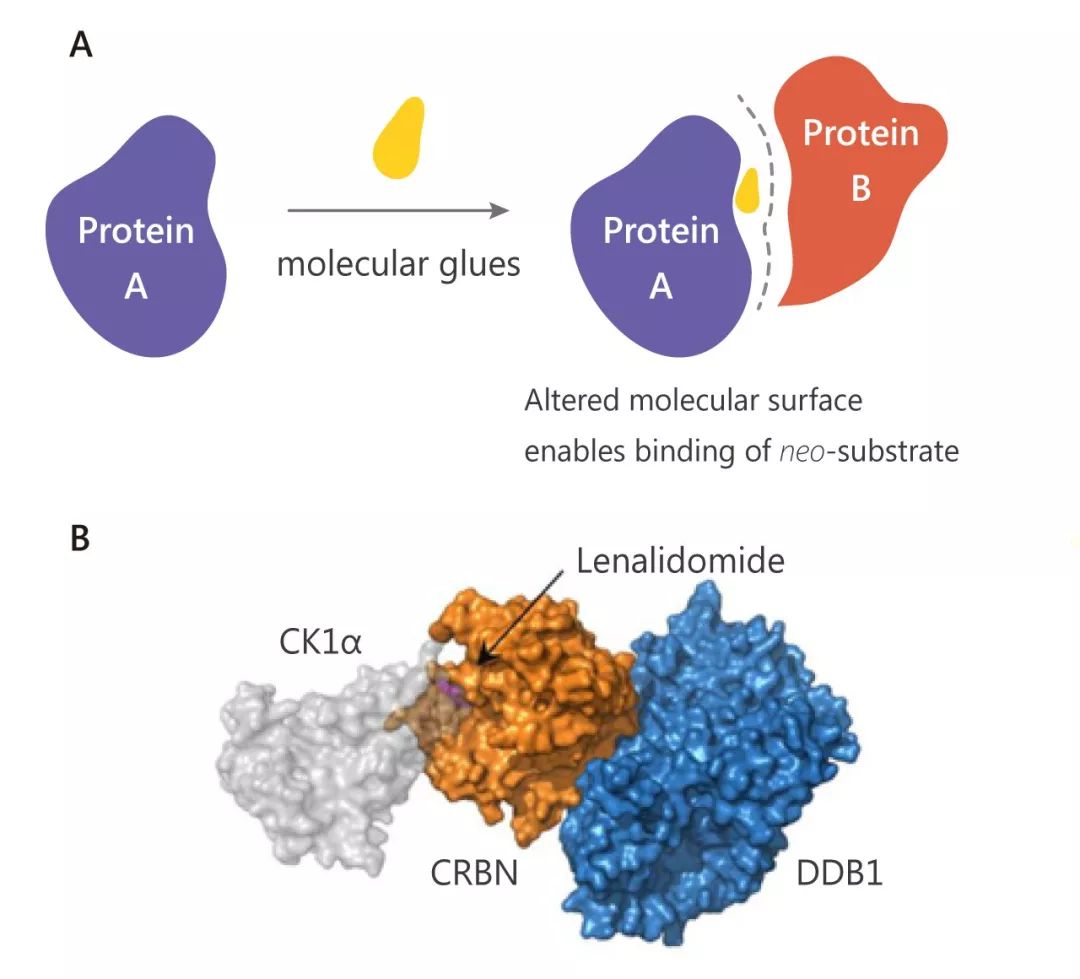
2021-08-30 来源:MedChemExpress 点击次数:2683小分子降解剂通过介导泛素化连接酶与靶蛋白的识别,对靶蛋白进行降解。目前蛋白降解剂主要有两类,一类是双功能分子降解剂,通常称为 PROTAC (蛋白水解靶向嵌合体),通过泛素-蛋白酶体途径特异性地降解靶蛋白。另一类是 “分子胶” (Molecular glues),也是通过结合泛素化连接酶,但与 PROTAC 不同的是,分子胶是通过修饰泛素化连接酶表面,从而识别并降解全新底物 (Neo-substrate)。例如磺胺类抗肿瘤药 (Indisulam); 和免疫调节药物 (IMiDs) 沙利度胺 (Thalidomide)、来那度胺 (Lenalidomide)。
A. “分子胶” 作用原理 B. 来那度胺 (Lenalidomide) 的作用机制理论来说,PROTAC 分子既可以作为 PROTAC 降解剂来结合和降解靶蛋白,也可以充当 “分子胶” 降解新底物。最近就发现一类邻苯二甲酰亚胺共轭的 PROTAC 降解剂其实是以分子胶的方式起作用,例如 MG-277。另外,最近 Benjamin Cravatt 团队开发出一种新型的“分子胶”。这类“分子胶”是以共价修饰 E3 连接酶 DCAF16 的方式,特异性促进核蛋白降解。
PROTAC “变身” 分子胶
MG-277 是对 MD-222 (PROTAC MDM2 降解剂) 进行了简单的结构修饰而来的。但正是这一小步的修饰,却带来了完全不同的靶向降解 “结局”。
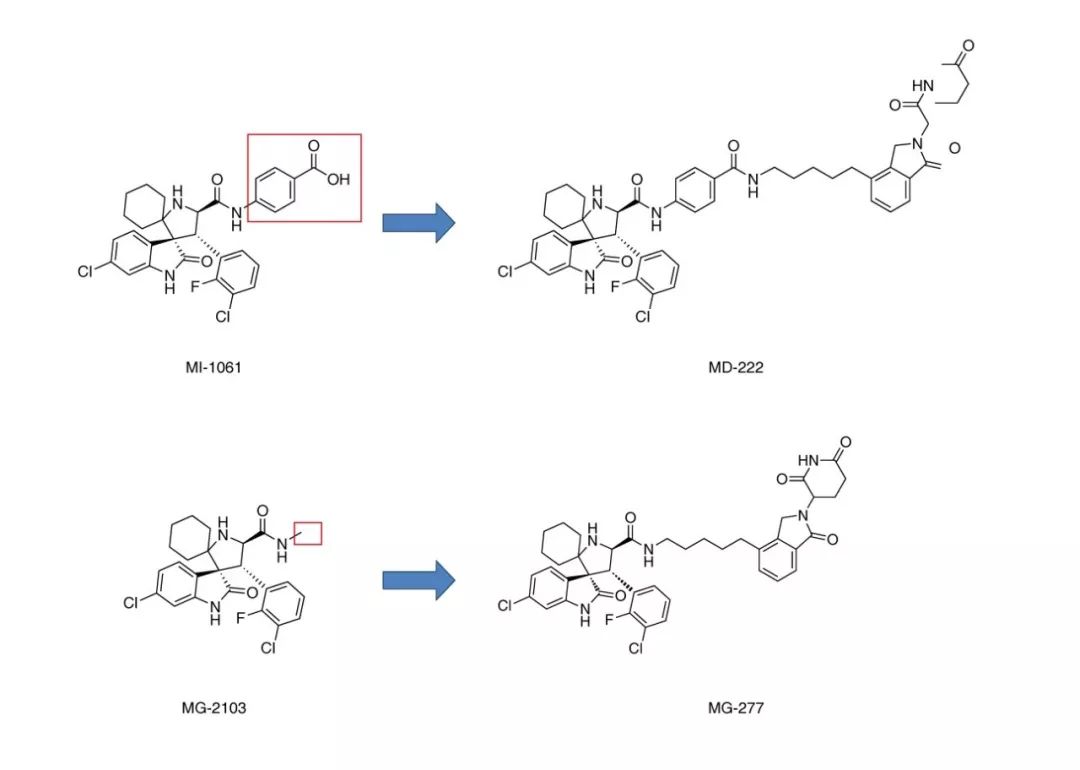
MG-277: MD-222 抑制剂部分的 MI-1061 的苯甲酸被甲基取代
首先,不同于 MD-222 对野生型 p53 (人白细胞 RS4;11) 的选择性,MG-277 对携带野生型,突变 p53 (RS4;11/IRMI-2 细胞) 或缺失 p53 的癌细胞系都有抑制作用,而且在诱导 MDM2 降解方面要比 MD-222 要低得多,且不能激活野生型 p53。通过敲除 MDM2 等试验发现,MG-277 的对细胞的抑制作用不仅不依赖 MDM2,本身也不与 MDM2 结合。
MG-277 对细胞的抑制活性,到底从何而来?
通过对 MG-277 中的戊二酰亚胺的氨基 (与 cereblon 结合相关) 甲基化,即合成了 MC-024,发现 MC-024 在抑制细胞 (RS4;11,RS4;11/IRMI-2,MDA-MB-231 和 MDA-MB-468) 生长方面的效率要低得多。在来那度胺与 MG-277 竞争实验中,来那度胺降低了 MG-277 对上述细胞系的生长抑制。因此,MG-277 对野生型和突变型 p53 细胞生长抑制活性,需要与 cereblon 结合。 据此,作者推测,MG-277 实际上可能起的分子胶的作用,通过促进某些细胞生长相关蛋白 -E3 连接酶 (CRL4CRBN) 复合物募集,进行泛素化和随后的蛋白酶体降解。
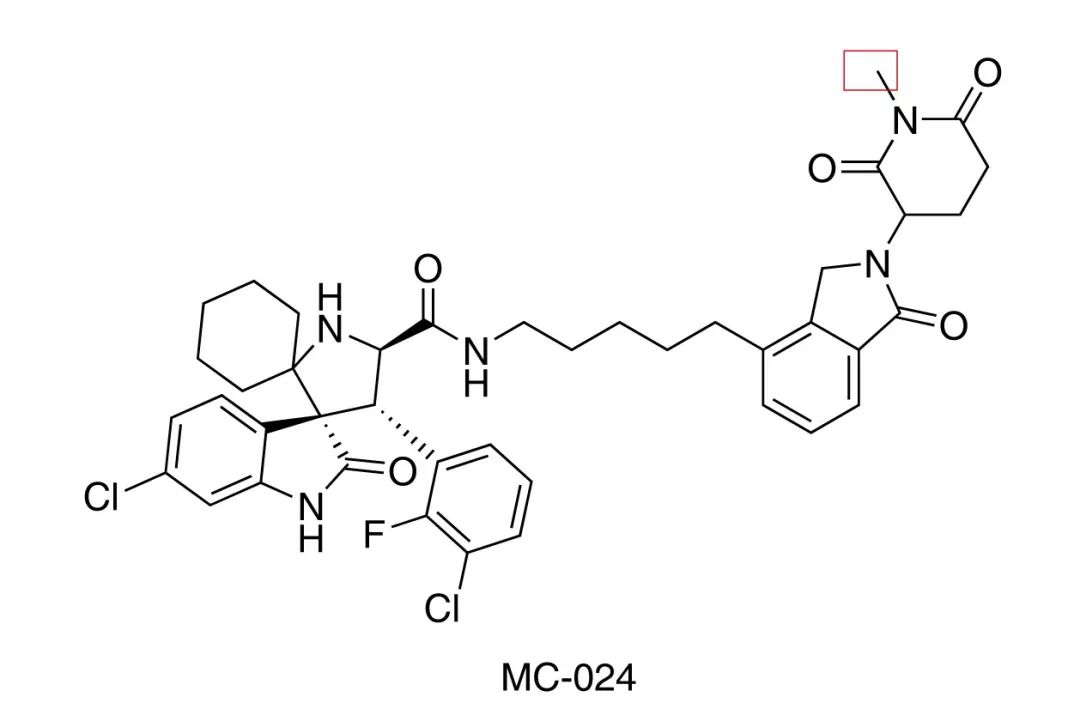
如果 MG-277 作为分子胶,真正的靶标蛋白是什么?
通过对野生型 p53 细胞和携带突变的 p53 细胞蛋白质组分析,MG-277 的靶标蛋白为 GSPT1,且降解 GSPT1 的水平取决于其与 cereblon,蛋白酶体和 Cullin-RING E3 连接酶功能的结合。MG-277 捕获了一些与相互作用有关的关键残基 (cereblon 中 Phe150 和 Glu377),这些残基对于将 GSPT1 募集到 cereblon 中是至关重要的。
总而言之,MG-277 以不依赖 p53 和 MDM2,但以依赖 cereblon,CUL4 E3 泛素连接酶和蛋白酶体的方式,在癌细胞中快速诱导 GSPT1 降解。MG-277 诱导 GSPT1 降解是其细胞生长抑制活性的原因。
而设计的邻苯二甲酰亚胺共轭降解物,既可以作为目的蛋白质的真正降解剂,也可以作为将新底物蛋白募集到 CRL4CRBN 的分子胶,用于泛素化和随后的降解。因此,在 PROTAC 降解剂的设计中需要考虑这两种机制。
特异性降解 “核蛋白” 的分子胶
接着,我们来讲讲另外一种新型“分子胶”。Benjamin Cravatt 团队找到了新的 E3 连接酶成员 DCAF16,一种目前没有文献报道过相关功能的多肽 (在哺乳动物中高度保守,但啮齿动物却不存在的多肽),此类 “分子胶” 以共价修饰 DCAF16 的方式,特异性促进核蛋白降解。
DCAF16 连接酶的发现
Benjamin Cravatt 团队在之前的工作中鉴定出一些与半胱氨酸结合共价片段,作者称为 “**” 片段 (Scoutfragment)。它们能 “搜寻” 出人类蛋白组中可配体的半胱氨酸,包括一些从未被研究的泛素化连接酶。作者将 KB02、KB03、KB05 三个“**”片段连接在 FKBP12 高亲和性的配体 SLF 上。发现 KB02-SLF、KB03-SLF、KB05-SLF 均未改变胞质蛋白 FKBP12 水平。其中,KB02-SLF 显著降低核蛋白 FKBP12 的水平。
选择性的 Cullin-RING 泛素连接酶 (CRL) 类 E3 连接酶抑制剂 MLN4924 阻断了 KB02-SLF 介导的核 FKBP12 降解,表明 KB02-SLF 是通过 CRL 的作用促进了核定位 FKBP12 的蛋白酶体降解。通过蛋白质组学以及 DCAF16 的 shRNA 沉默进一步确定 CRL 类 E3 泛素化连接酶为 DCAF16。DCAF16 在诱导核蛋白降解的过程中是如何被修饰的?
串联质谱 (MS/MS) 分析和定点诱变实验表明,KB02-SLF 是修饰了 DCAF16 的 Cys177-179 三个半胱氨酸位点。其中 DCAF16 中的 C177 和 C179 为极有可能是介导 FKBP12 降解的关键的位点。接下来,作者构建的 KB02-JQ1 双功能分子 (诱导核蛋白 BRD4 降解),在敲除的 DCAF16 细胞中,KB02-JQ1 诱导的 BRD4 降解则被抑制。
DCAF16 的发现,在 CRBN 和 VHL 的蛋白降解剂的基础上,拓展了蛋白降解剂的开发与应用前景。同时,特异性促进核蛋白的降解,避免降解了同双功能化合物结合的胞质蛋白。另外,较少成分的 DCAF16 修饰就可支持配体诱导的蛋白质降解,而未被修饰的 DCAF16 仍然能调节其底物,使蛋白降解剂能最小化受到 DCAF16 内源底物的干扰。相关产品
MG-277 是一种由 PROTAC 降解剂转化而来的分子胶。MG-277 诱导中等程度的 MDM2 降解。MG-277 以非 p53 的方式高度有效地抑制肿瘤细胞的生长,对 RS4;11 细胞和 p53 突变体 RS4;11/IRMI-2 细胞的 IC50 分别为 3.5 nM 和 3.4 nM。MG-277 有效的诱导翻译终止因子 GSPT1 的降解,DC50 为 1.3 nM。MG-277 具有有效的抗癌活性。 KB02-SLF 是一种核 FKBP12 降解剂 (molecular glue)。KB02-SLF 通过共价修饰 DCAF16 (E3 ligase) 促进 FKBP12 降解,并可以提高生物系统中蛋白质降解的持久性。KB02-SLF 由 SLF 与泛素 E3 连接酶配体 (KB02) 通过 linker 连接而成。KB02-JQ1
KB02-JQ1 是一种高选择性 BRD4 降解剂 (molecular glue)。KB02-JQ1 通过共价修饰 DCAF16 (E3 ligase) 促进 BRD4 降解,并可以提高生物系统中蛋白质降解的持久性。KB02-JQ1 由 JQ1 与泛素E3 连接酶配体 (KB02) 通过 linker 连接而成。 Pevonedistat (MLN4924) 是一种有效,选择性的 NEDD8 活化酶 (NAE) 抑制剂,IC50 为 4.7 nM。NEDD8 活化酶参与 CRL 激活的第一步,通过激活 NEDD8 并随后转移到 Ubc12,NEDD8 途径的 E2 结合酶。
参考文献
[1] Yang J, et al. Simple StructuralModifications Converting a Bonafide MDM2 PROTAC Degrader into a Molecular GlueMolecule: A Cautionary Tale in the Design of PROTAC Degraders. J Med Chem. 2019 Oct 21.[2] Cromm PM, et al. Targeted Protein Degradation: from Chemical Biology to Drug Discovery. Cell Chem Biol. 2017 Sep 21;24(9):1181-1190.
[3] Lu G, et al.The myeloma drug lenalidomide promotes the cereblon-dependent destruction of Ikaros proteins. Science. 2014 Jan 17;343(6168):305-9.
[4] Lopez-Girona A, et al. Cereblon is a direct protein target for immunomodulatory and antiproliferative activities of lenalidomide and pomalidomide. Leukemia. 2012 Nov;26(11):2326-35.
[5] Hughes S J, et al. Molecular recognition of ternary complexes: a new dimension in the structure-guided design of chemical degraders. Essays Biochem. 2017 Nov 8;61(5):505-516.
[6] Keriann M.Backus, et al. Proteome-wide covalent ligand discovery innative biological systems.Nature. 2016 Jun23;534(7608):570-4.
[7] Bar-Peled L, et al. Chemical Proteomics Identifies Druggable Vulnerabilities in a Genetically Defined Cancer.Cell. 2017 Oct 19;171(3):696-709.e23.
[8] Zhang X, et al. Electrophilic PROTACs that degrade nuclear proteins by engaging DCAF16. Nat Chem Biol. 2019 Jul;15(7):737-746.