C9orf72相关FTD和ALS的脑脊液生物标记物分析方法介绍
2022-09-14 来源:本站 点击次数:1370C9orf72 基因中的GGGGCC重复扩增是额颞叶痴呆(FTD)和肌萎缩侧索硬化(ALS)最常见的遗传原因,而且重复的非ATG翻译导致二肽重复蛋白(DPRs)的产生。随着靶向重复扩增的潜在疗法进入临床试验,迫切需要一种高敏的生物标记物对靶点作用进行分析。本文研究者利用Simoa技术开发了一种灵敏可靠的poly(GP)二肽重复蛋白测定方法。

文章题目:Development of a sensitive trial-ready poly(GP) CSF biomarker assay for C9orf72-associated frontotemporal dementia and amyotrophic lateral sclerosis
发表时间:2022年4月
期刊名称:J Neurol Neurosurg Psychiatry
影响因子:13.654
DOI:10.1136/jnnp-2021-328710
研究概述
研究人员通过Simoa平台开发了一种免疫分析方法,用于测量C9orf72相关FTD和ALS患者脑脊液(CSF)中C9orf72重复扩增产生的poly(GP) 二肽重复蛋白(DPR)。
研究表明,该分析方法高度灵敏和稳定,通过了广泛的鉴定标准,板内、板间的变异性低、标曲和样品的精密度和准确度高、稀释线性好、对样品和标准冻融具有耐受性,以及不受血红蛋白干扰。使用这种方法来测量FTD突变携带者队列收集的CSF样本中的poly(GP) (N=40 C9orf72和15个对照)。CSF中C9orf72的poly(GP) 信号,样本组的平均信号值比对照组高38倍,最低的样本比对照组高8倍,均低于该方法的定量下限。而且检测的特异性和敏感性均为100%,靶标检测的窗口较大。
这些数据表明,基于Simoa的poly(GP)DPR分析适合用于临床试验,以明确旨在减少C9orf72重复的治疗药物的靶向治疗。
研究内容
1、Simoa poly(GP) assay建立
首先使用Simoa HD-1对assay进行优化。研究人员测试了一系列抗体,包括小鼠抗GP单克隆抗体(mGP),和一系列针对不同长度GP肽的兔多克隆抗体(GP57、GP60和GP6834)。综合考虑后选择了小鼠抗GP单克隆抗体(mGP)作为捕获抗体,多克隆抗体组合(GP57−60)作为检测抗体,标准品为GST-GP32肽段。这套组合的信噪比最高,为2.51;且LLOQ最低,为1.04pg/ml(图1)。为了确保长期的兼容性,接下来将分析转移到新的Simoa HD-X平台。且对该assay进行了重新优化,将标准曲线稀释液从裂解液稀释液B(HD-1)更改为稀释液A(HD-X)效果最好(图2A)。此外,SBG从100μM降至50μM,LLOQ为1.17 pg/mL(图2B)。
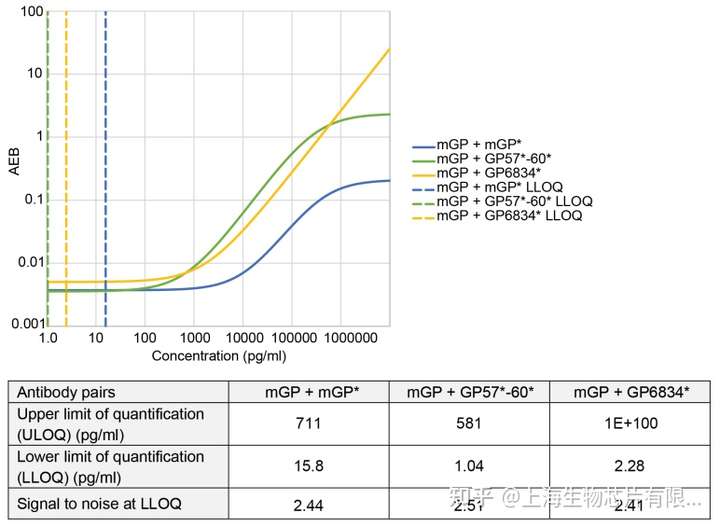
Fig.1 Simoa homebrew assay中各抗体组合的比较。虚线分别表示每种测定方法优化后预测的LLOQ。AEB:平均每颗磁珠上的酶标数;LLOQ:定量下限;Simoa:单分子阵列;*:代表此种抗体已标记上生物素。
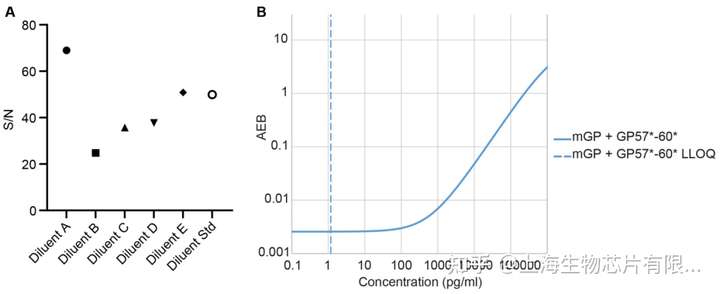
Fig.2 将poly(GP) assay转移到Simoa HD-X平台。(A)在人脑脊液加入25 pg/mL GST-GP32标准品,然后用不同的Quanterix稀释液1:2进行稀释,通过比较信号/噪声(S/N)来评估样品稀释液的效果。(B)使用Quanterix分析显像工具计算拟合的标准品曲线,虚线显示LLOQ为1.17 pg/mL。
2. Simoa poly(GP) assay验证为将该assay用于临床试验,使用标准生物标记物分析鉴定标准进行评估(表2)。由图3可知,各项结果表明,该测定具有高度的灵敏度和稳健性,通过了标准生物标记物分析鉴定标准的评估,包括板内和板间的低变异性、标准品和样品的高精密度和准确度、稀释线性、样品和标准冻融耐受性以及血红蛋白干扰测试。
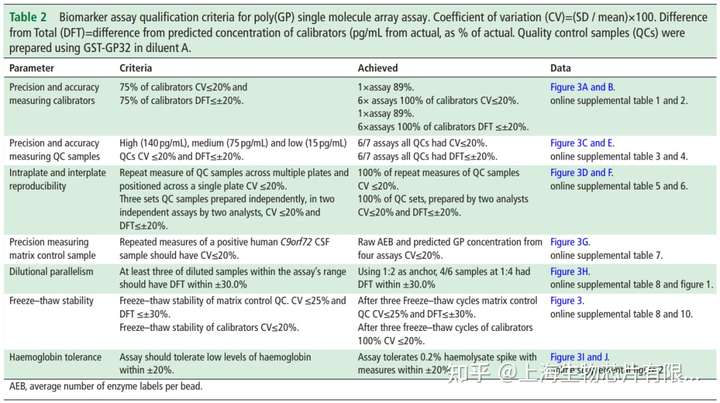
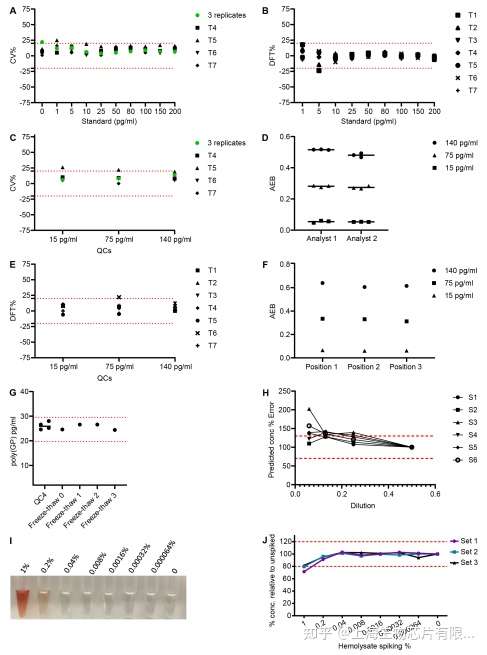
Fig.3 CSF poly(GP) Simoa assay验证结果。制备了10点标准曲线和3个质量控制(QC)样品,分别进行了7次独立检测。(A) 每个标准品的变异系数(CV)均小于20%。(B)每个标准品的总差(DFT)。DFT=标准品的预测浓度与实际浓度之差的%。(C)QC样品的CVs。(D)由两个工作人员分别制备的QC样本的AEB信号值。(E) QC样品
3.使用优化的Simoa测定法测量C9orf72 扩增载体CSF中的poly(GP)
使用这种优化后的测定方法来测量健康对照组(N=15)和C9orf72扩增阳性组(N=40)的脑脊液队列中的poly(GP)。来自最低C9orf72样本的分析信号的信噪比是对照样本平均信号的八倍,显示出与对照CSF信号的明显分离(图4A)。C9orf72组与对照组的信噪比平均为38倍。健康人脑脊液中的poly(GP)在15个样本中有13个低于检测限,其余2个低于LLOQ。
在所有C9orf72组中检测到poly(GP)高于LLOQ,在没有健康对照的情况下,敏感性和特异性均为100%。在C9orf72扩增阳性样本中,poly(GP) 的测量范围为6-148 pg/mL。发现男性和女性C9orf72扩增阳性样本之间的poly(GP) 水平没有差异。发现CSF poly(GP)水平与症状性C9orf72扩增阳性样本(n=15)的发病年龄之间没有相关性(图4C)。有趣的是,对所有40例C9orf72扩增阳性病例进行分析后发现,样本采集时的年龄与脑脊液中测得的poly(GP)之间存在显著的中度正相关(r=0.3643)。然而,如果从分析中删除具有最高poly(GP)水平的情况,则p值变为p=0.0522。
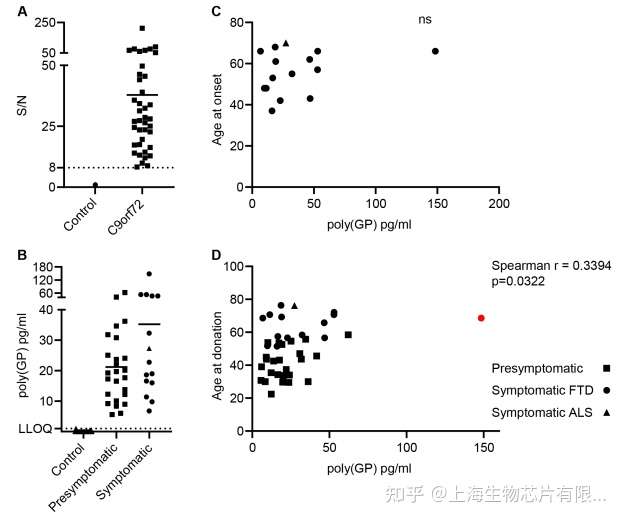
Fig.4 C9orf72扩增携带者脑脊液中Poly(GP) 水平
总结
- 准确测量FTD和ALS引起C9orf72 重复扩增产生的DPR,将是评估临床试验中重复/DPR降低策略目标参与度的关键工具。
- 现有免疫测定法,可以检测患者CSF中的poly(GP) DPR,但由于一些患者的poly(GP) 水平接近背景,可能需要提高灵敏度。
- 该研究报告了一种适合临床试验的超灵敏脑脊液聚糖蛋白检测方法的开发。能在绝大多数试验参与者中评估目标参与度,包括低聚糖蛋白水平的参与者。
参考文献:Wilson KM, Katona E, Glaria I, Carcolé M, Swift IJ, Sogorb-Esteve A, Heller C, Bouzigues A, Heslegrave AJ, Keshavan A, Knowles K, Patil S, Mohapatra S, Liu Y, Goyal J, Sanchez-Valle R, Laforce RJ, Synofzik M, Rowe JB, Finger E, Vandenberghe R, Butler CR, Gerhard A, Van Swieten JC, Seelaar H, Borroni B, Galimberti D, de Mendonça A, Masellis M, Tartaglia MC, Otto M, Graff C,Ducharme S, Schott JM, Malaspina A, Zetterberg H, Boyanapalli R, Rohrer JD, Isaacs AM; Genetic FTD Initiative (GENFI). Development of a sensitive trial-ready poly(GP) CSF biomarker assay forC9orf72-associated frontotemporal dementia and amyotrophic lateral sclerosis. J Neurol Neurosurg Psychiatry. 2022 Apr 4:jnnp-2021-328710. doi: 10.1136/jnnp-2021-328710. Epub ahead of print. PMID: 35379698.

