各肿瘤研究模型的优缺点和肿瘤类器官在药物筛选中的应用
2023-03-01 来源:本站 点击次数:2844近年来,3D 类器官技术如热浪席卷科研界,肿瘤研究方向的科研者们也纷纷把目光投向了肿瘤类器官,那么被誉为 “试药替身” 的肿瘤类器官的出现能否打破了这一 “僵局” 呢?
烫知识:肿瘤类器官是来源于患者特异性组织样本的自组织组装 3D 肿瘤细胞,它模拟了母体肿瘤的关键组织病理学、遗传和表型特征。
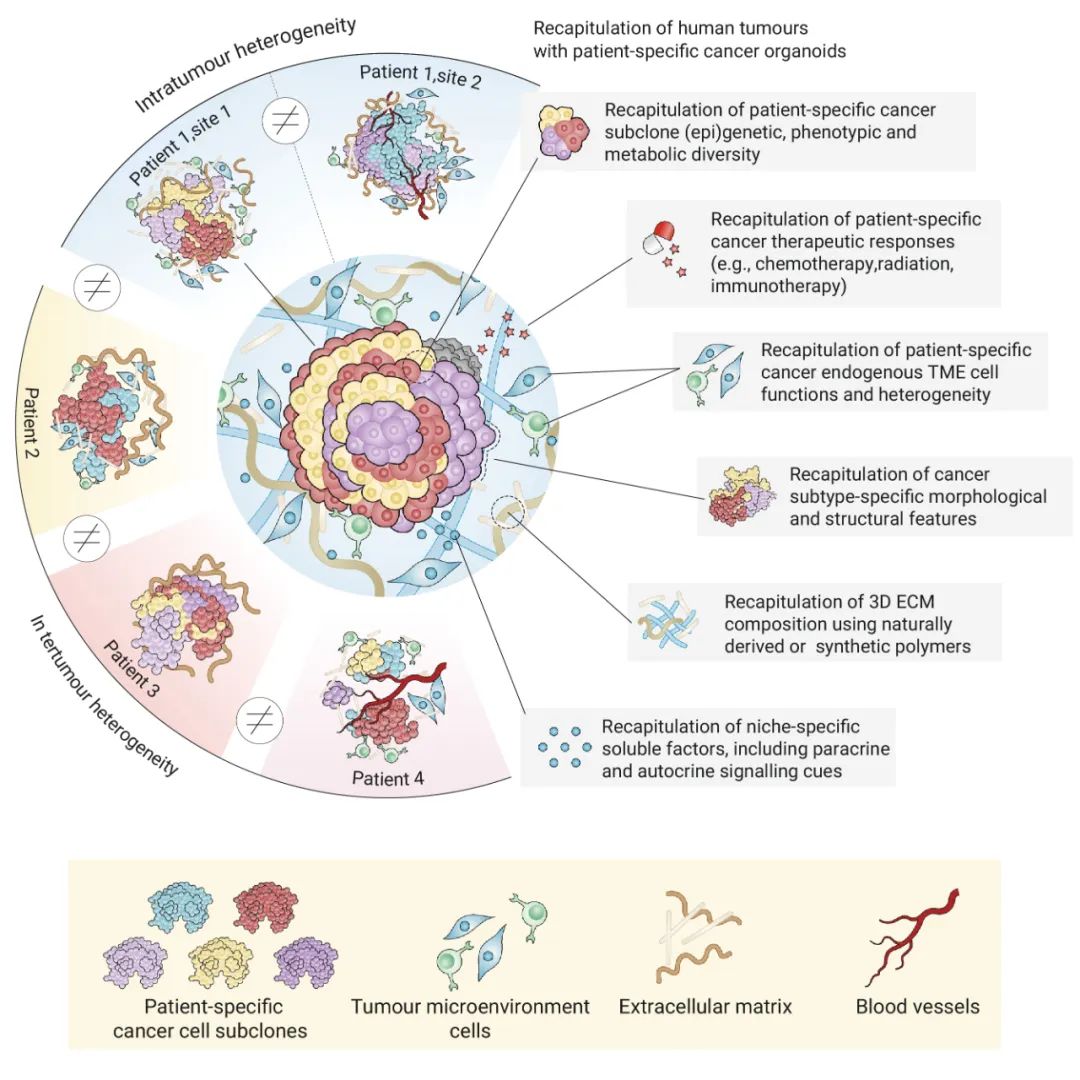
癌症作为一种异质性疾病,是一种包括不同细胞类型的复杂生态系统。除肿瘤细胞外,肿瘤还包括与肿瘤相关的基质细胞、微环境中的生长因子和代谢物,它们对肿瘤细胞的生长、侵袭能力和药物反应具有深远的影响。每个患者的肿瘤都呈现出一系列独特的细胞和环境特征,因此肿瘤内部和肿瘤之间具有巨大生物异质性。
直接来源于人类肿瘤组织的类器官模型已经被证明可以准确地再现肿瘤内和肿瘤间的生物学异质性。具体来说,肿瘤类器官可以再现不同肿瘤细胞亚克隆的极度表观遗传/遗传和表型多样性,以及它们的共同的肿瘤特异性形态学特征。因此,癌症类器官在临床中模拟患者对抗癌治疗的特异性反应中表现出巨大潜力。
“一刀切” 护理标准已经 Out 了,精准医疗的兴起意味着肿瘤异质性成为癌症治疗方向的重中之重。
图 1. 肿瘤类器官概括了患者特异性肿瘤异质性的典型特征[1]
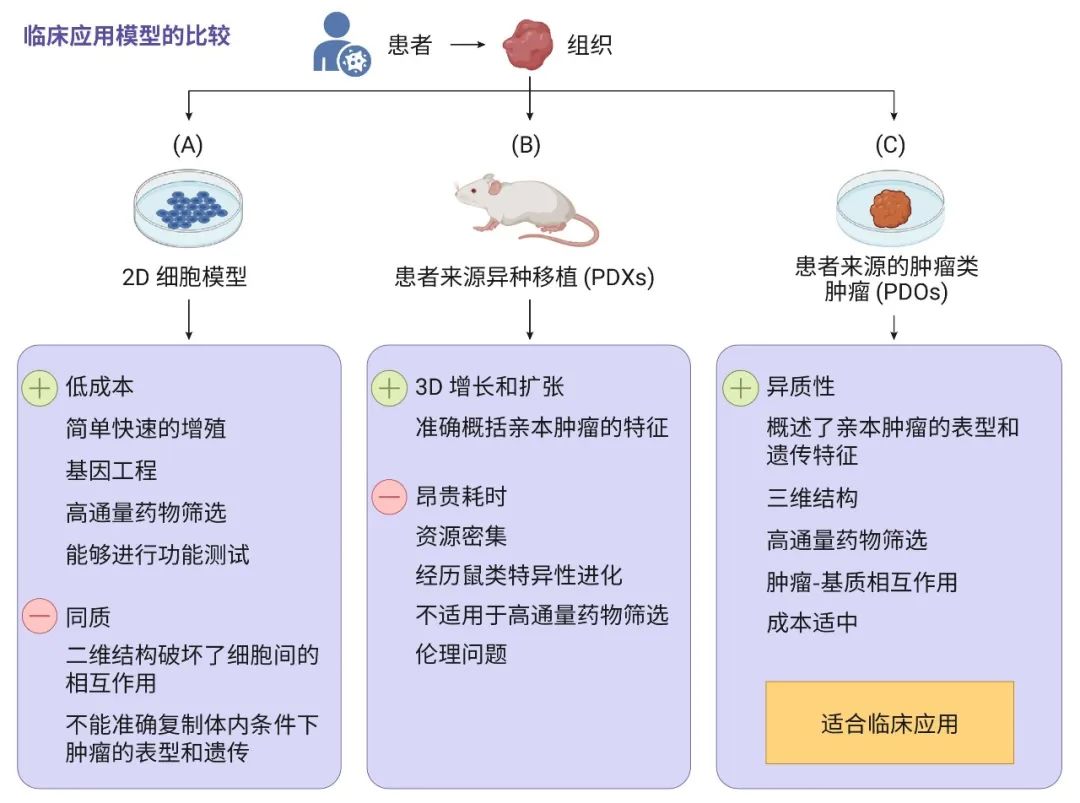
图 2. 2D 细胞模型、PDXs、患者来源的肿瘤类器官 (PDOs) 的比较[2]
2D 细胞:因易于增殖、维护成本低、易于进行功能测试而被广泛使用。但从根本上说,它们不能准确的代表体内肿瘤。其主要限制在于无法准确复制体内癌细胞的表型和遗传学特征。更重要的是,它们无法准确概括癌症的复杂性和动态性,尤其是耐药机制 (这仍然是癌症患者治愈的主要限制因素)。
患者来源的异种移植 (PDXs):能够概括人类肿瘤的生物学特征,但使用起来耗时且昂贵,此外,PDX 还表现出小鼠特异性肿瘤进化的能力,并且引发了关于使用动物模型进行实验的各种伦理问题。PDX 不适合高通量药物筛选 (HTS),主要用于实验室研究。
肿瘤类器官:与 PDX 相比,肿瘤类器官成本更低、并具有较高效率,能够模拟正常组织及不同阶段的癌变过程的组织,既反映了真实世界患者癌症的生理特征,又能应用高通量药物筛选。此外,体外基因修饰比体内更容易: 例如通过 CRISPR/Cas9 技术对肿瘤抑制因子 Trp53 和 Stag2 进行基因敲除的基因操作类器官。
类器官与肿瘤微环境:最初,肿瘤类器官因无法再现 TME 使肿瘤类器官被打上“不完美”标签,但随着类器官技术的发展,肿瘤类器官再度升级:将类器官植入高度血管化的组织或者通过基因编辑或结合混合细胞共培养 (使用微流体平台) 来实现肿瘤血管化建模。通过肿瘤类器官细胞和免疫细胞的共培养实现肿瘤-免疫相互作用的建模,可以更好地模拟肿瘤中的免疫系统功能。
已经有很多不同癌症患者来源的样本建立的类器官模型,如结肠、食管、胃、大脑、前列腺、胰腺、肝脏、乳腺癌等类器官。
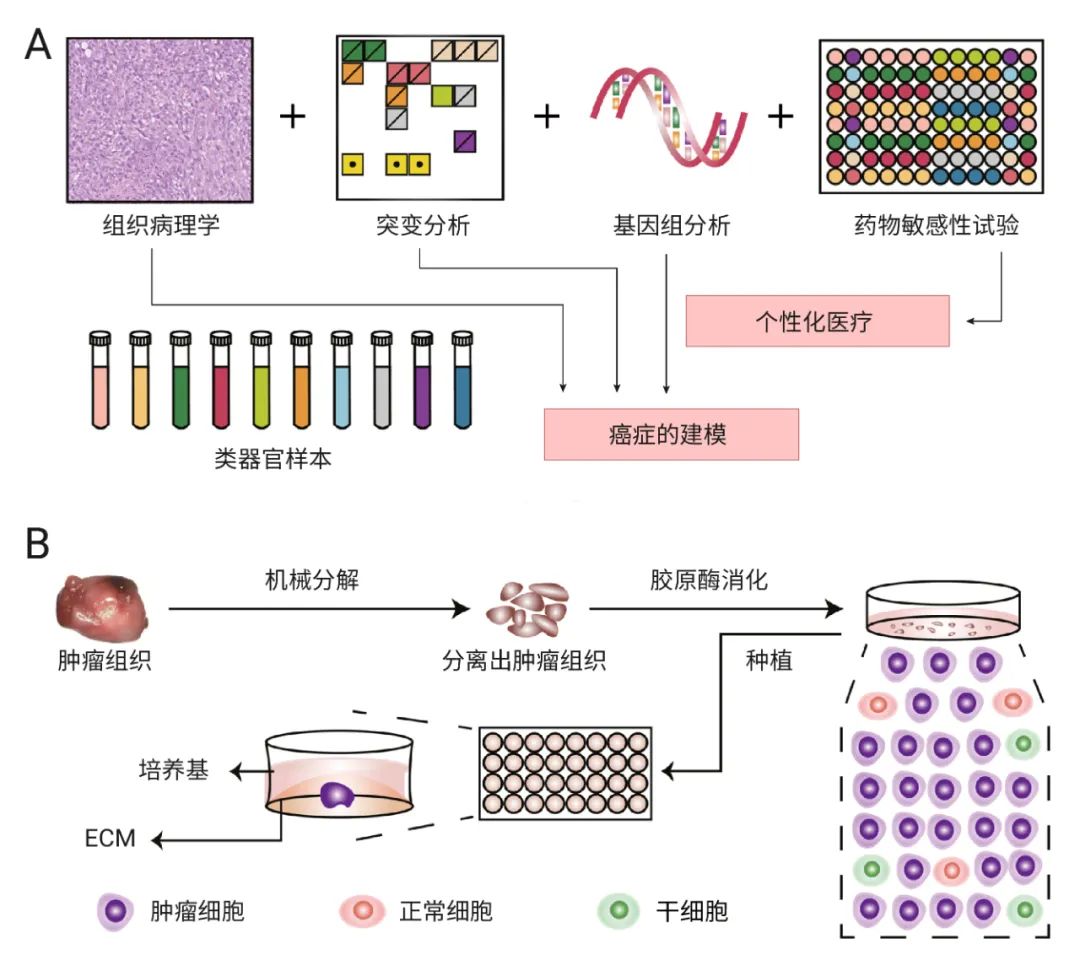
图 3. PDOs 建立的主要步骤和主要应用[1]
(A) 包含癌细胞、成体干细胞、多能干细胞或肿瘤干细胞的人类癌症组织,首先通过机械和化学方法分解成非常小的碎片、细胞簇或单细胞,并在适当的 3D 条件下在具有 ECM 成分的水凝胶中培养。(B) 肿瘤类器官能模仿原发组织组织病理学特征、遗传图谱、突变情况,甚至对治疗的反应,并且可以建立肿瘤类器官生物库。
PDOs 可用于研究耐药性、代谢、分化和癌症基因功能,近年来,多种不同组织的 PDOs 模型已经被用于药物发现探索候选治疗药物的细胞毒性和实现个性化的癌症治疗,Zilong Zhou 等人总结类器官培养平台在药物筛选中的应用,见表 1。
此外,类器官用于癌症药筛的临床相关性和预测有效性在多篇研究中都已经得到了较为充分的证实,并且基于 PDOs 模型的临床试验集中在发病率和死亡率较高的肿瘤,如结直肠癌、肺癌、胶质瘤、乳腺癌、肝癌和胰腺癌。Vlachogiannis G 团队在 Science 发表了 PDOs 模型对转移性胃肠癌的药敏测试结果,他们从 71 例晚期结直肠癌患者中提取出癌细胞样本建立 PDOs,测试了 55 种抗癌药物,研究结果显示,这些 PDOs 在预测患者对靶向药物或化疗的反应方面达到 100% 的敏感性,93% 的特异性,88% 的阳性预测率和 100% 的阴性预测率,展现了极高的临床相关性。
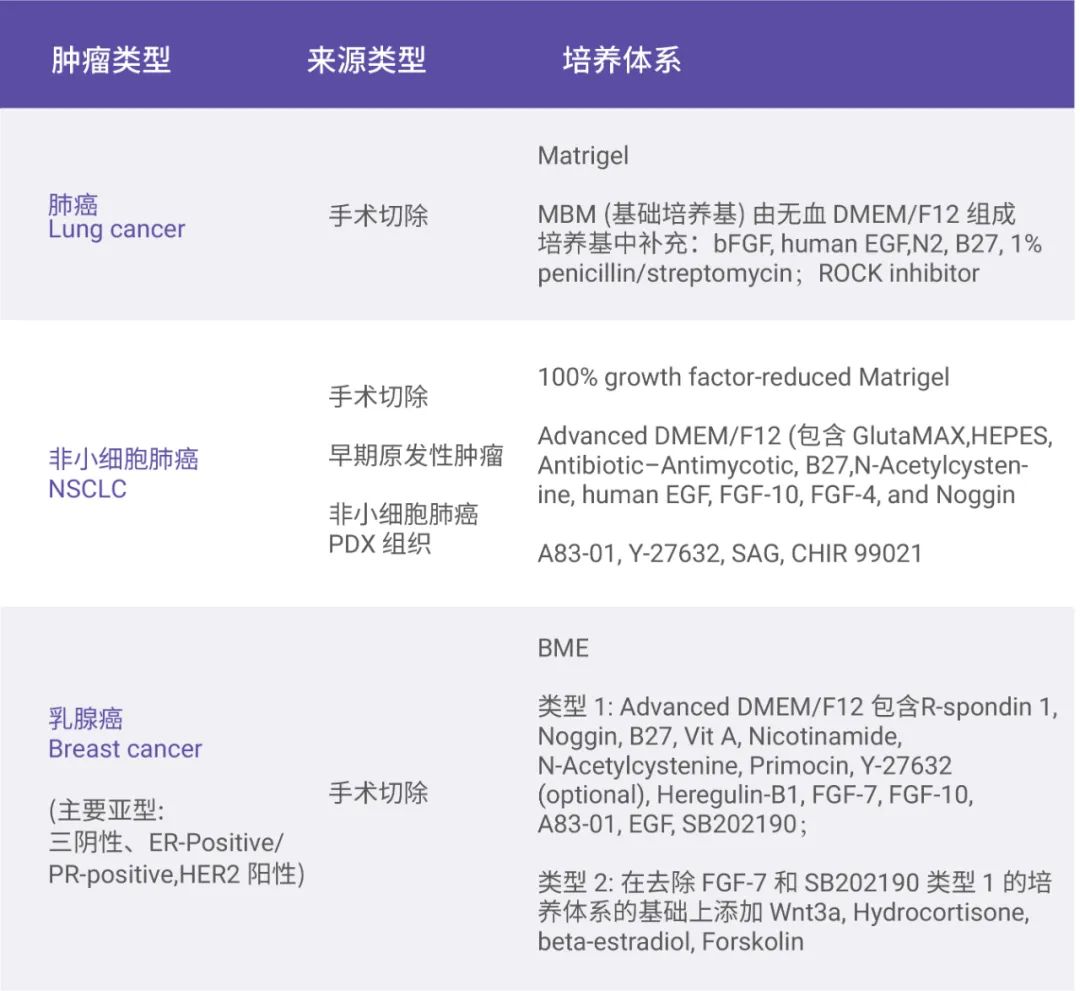
类器官培养基中需要一些生长因子和抑制剂,培养基中生长因子和抑制剂的不同组合有助于在类器官中产生不同的成分谱系。
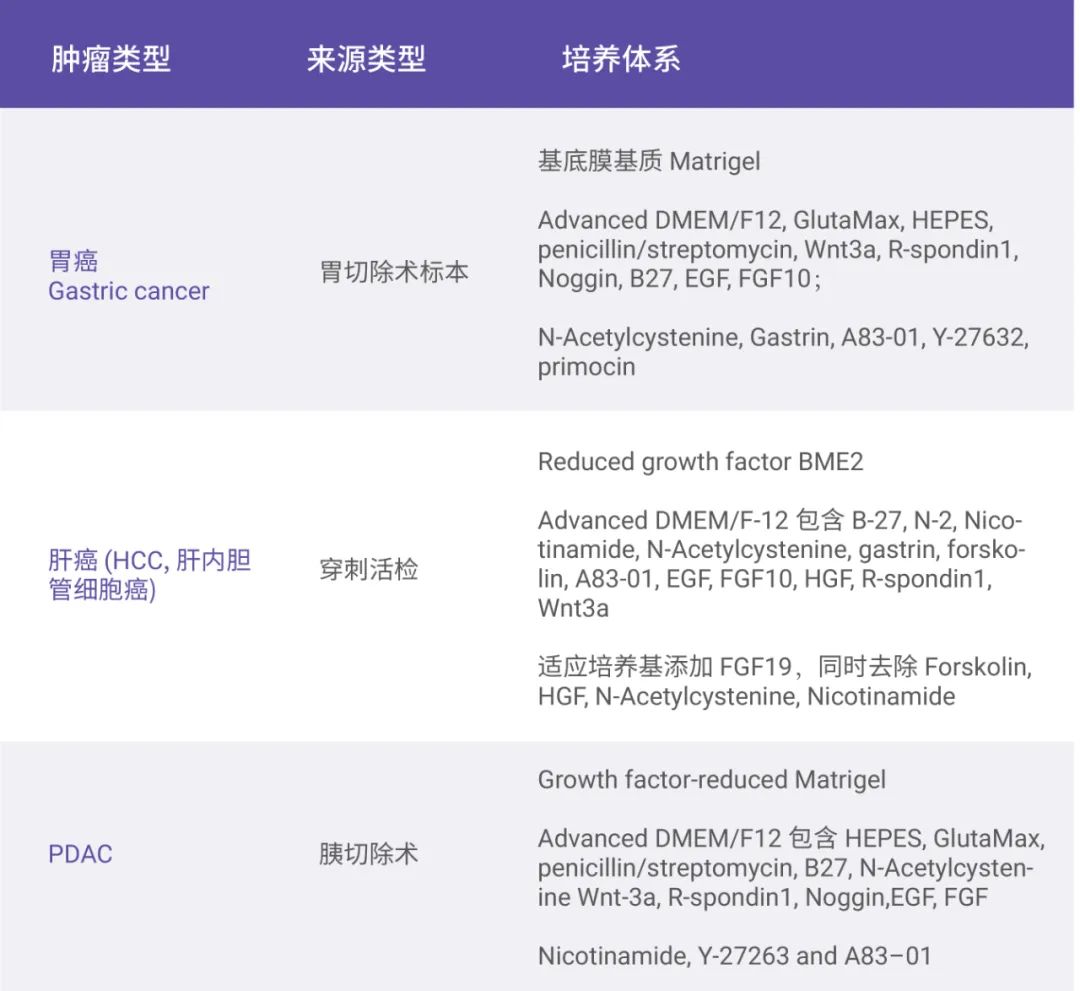
表 2. 常见肿瘤类器官培养系统
左右滑动查看更多
MCE 提供高纯度、高生物活性、低内毒素的一系列用于类器官培养的重组蛋白,类器官培养需要的小分子,研究常用染料一并奉上,助力科研!
● 高纯度 ● 高生物活性 ● 低内毒素水平 ● 稳定的一致性 ● 规格齐全
MCE 的所有产品仅用作科学研究或药证申报,我们不为任何个人用途提供产品和服务
参考文献
1. Hanxiao Xu,Dechao Jiao,Aiguo Liu,Kongming Wu. Tumor organoids: applications in cancer modeling and potentials in precision medicine. J Hematol Oncol. 2022; 15, 58.
3. Jarno Drost, Hans Clevers.Organoids in cancer research.Nat Rev Cancer. 2018 Jul;18(7):407-418.
4. Bauer L. LeSavage, Sarah C. Heilshorn, et al. Next-generation cancer organoids. Nat Mater. 2022 Feb;21(2):143-159.
5. Zilong Zhou, Lele Cong, Xianling Cong. Patient-Derived Organoids in Precision Medicine: Drug Screening, Organoid-on-a-Chip and Living Organoid Biobank. Front Oncol. 2021 Dec 30;11:762184.
6. Colin Rae, Francesco Amato, Chiara Braconi. Patient-Derived Organoids as a Model for Cancer Drug Discovery.Int J Mol Sci. 2021 Mar 27;22(7):3483.
7. Georgios Vlachogiannis, Nicola Valeri, et al. Patient-derived organoids model treatment response of metastatic gastrointestinal cancers. Science. 2018 Feb 23;359(6378):920-926.