二聚体菁染料分子间和分子内的协同聚集提供了体内自我递送和光热治疗
2024-08-14 来源:本站 点击次数:1569
近日,彭孝军院士团队研究成果在《advanced functional materials》上发表,文章标题为“Synergistic Inter- and Intramolecular Aggregation of Dimeric Cyanine Dyes Affords Highly Efficient In Vivo Self-Delivery and Photothermal Therapy”。该研究详细地描述了一种新型的光热疗法策略,从分子设计到体内外的实验验证,展示了其在抗癌治疗中的潜力。
光热疗法作为一种有前途的抗癌治疗策略,依赖于开发具有强大体内传递能力和治疗效果的光热剂(Photothermal Agents, PTAs)。然而,目前缺乏有效的分子设计方法来实现高性能的PTAs。
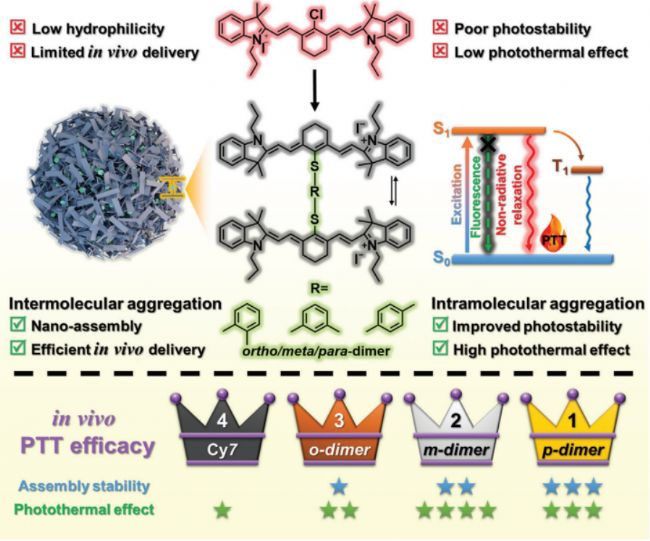
该研究提出了一种策略性设计的二聚七甲基菁(Cy7)分子,通过邻位/间位/对位-苯基二硫醇共价连接,这些设计促进了在水中自发的纳米粒子组装,这归因于有效的分子间聚集,增强了体内传递。此外,分子内Cy7单元之间的聚集促进了优越的光热转换效率(PCE),对于间位二聚体可高达74.1%。值得注意的是,对位二聚体变体不仅实现了高达61.1%的高PCE,而且还展示了最有效的药代动力学特性,导致体内无与伦比的抗癌效果。这种双重聚集策略,利用分子间和分子内的动态,为二聚体Cy7提供了卓越的自我传递能力和光热效果,为下一代光热疗法提供了一种有希望的方法。
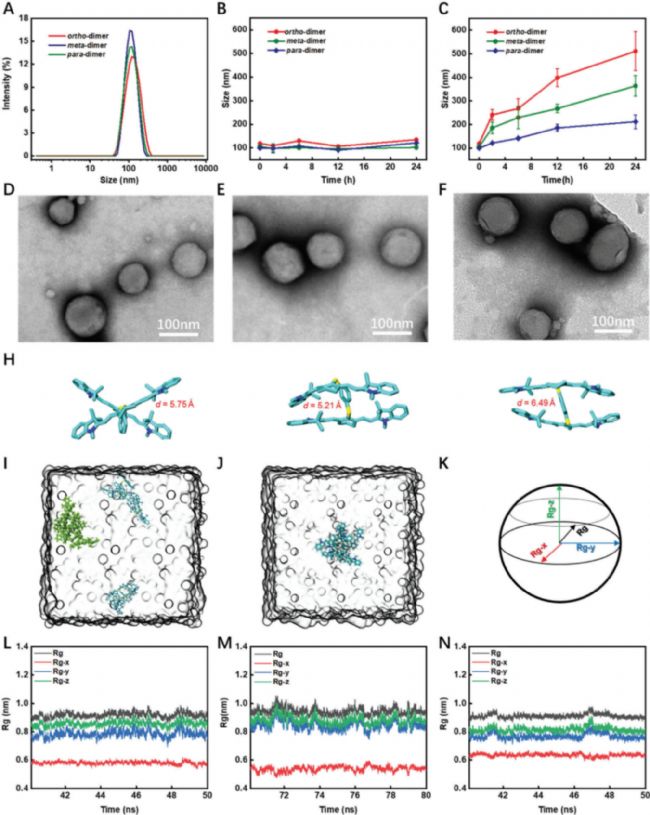
文中研究单体与二聚体分散在水中时的行为,使用动态光散射(DLS)和透射电子显微镜(TEM)对水分散的二聚体进行进一步表征。研究结果表明二聚体Cy7自发地组装成平均直径约为100纳米的球形结构,并且在模拟生理条件下(10%FBS的细胞培养基)也具有稳定性。
实验结果表示,二聚体Cy7的荧光量子产率为Φf < 0.3%,较单体显著降低;二聚体Cy7的荧光猝灭主要是通过非辐射衰减(即热产生)实现的、二聚体Cy7的光热疗法(PTT)效率显著高于单体Cy7和ICG。
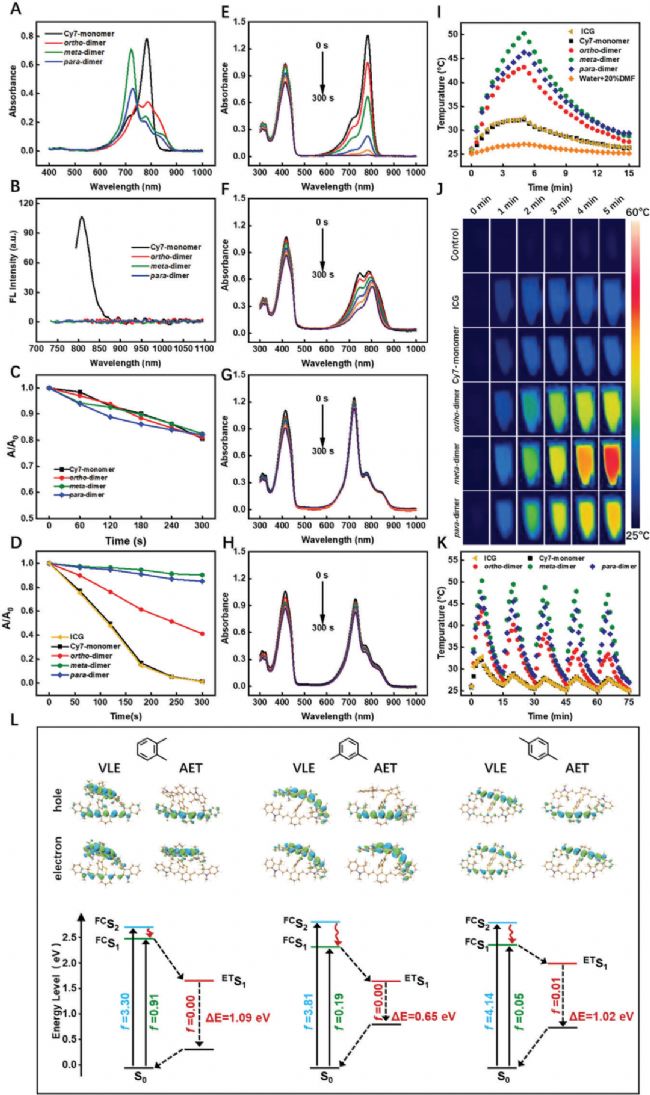
二聚体Cy7染料中强大的PET倾向有助于它们的光稳定性,并维持它们随时间的光热效率。由于荧光猝灭导致的激发态寿命减少,使这些染料不易光漂白。
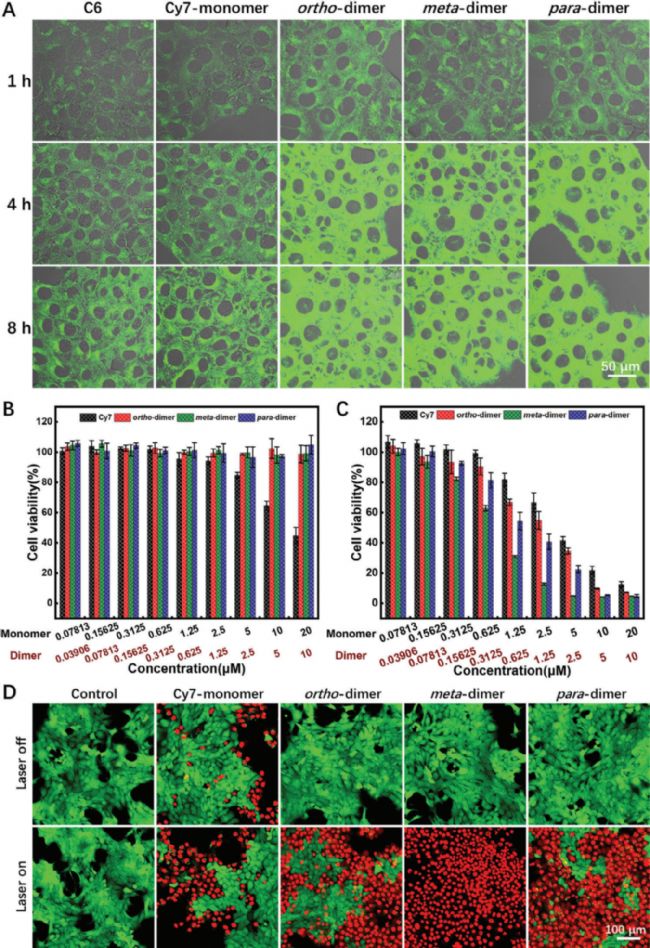
体外光疗实验结果表明,二聚体具有良好的生物相容性,并且不同程度上表现出比单体具有更强的光毒性,其中,几乎所有用间二聚体处理的4T1细胞都在照射后死亡,这突显了这些特定二聚体的强大光疗能力。
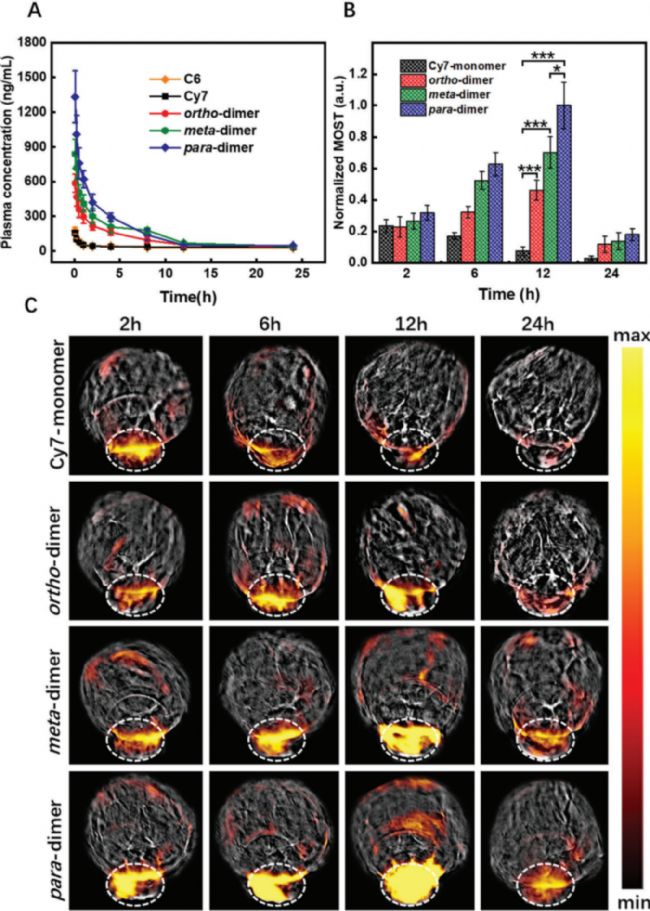
体内药代动力学结果显示,二聚体Cy7在体内的循环增强。利用二聚体Cy7的显著光热效应,采用光声成像检测其体内肿瘤积聚,注射后第12小时观察到二聚体Cy7的峰值光声信号,对二聚体在肿瘤组织中表现出最强光声强度。
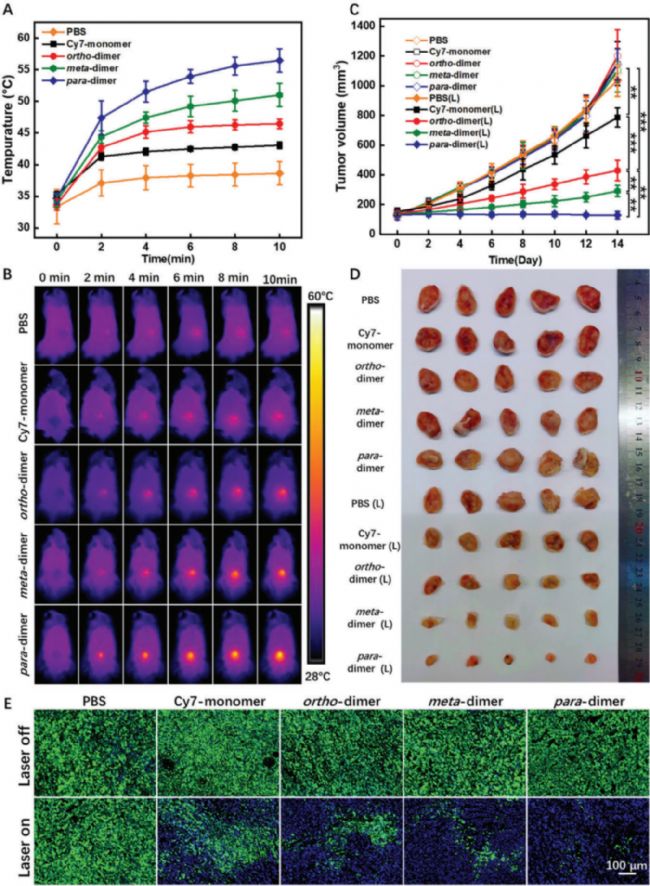
体内抗肿瘤实验显示,对二聚体显示出最显著的抗肿瘤活性,肿瘤体积几乎没有增加。
该研究成功开发了一种新型二聚体Cy7光热剂,通过分子内和分子间聚集的协同作用,实现了高效的体内自我传递和光热疗效,其中对位二聚体展现出了最佳的稳定性和抗癌效果,为光热疗法提供了一种有希望的新一代治疗策略。
原文链接:
https://doi.org/10.1002/adfm.202316452
关于iThera Medical小动物多光谱光声断层扫描(MSOT)系统
MSOT多光谱光声断层扫描系统是由德国iThera Medical公司研发并推入市场的光声成像设备,主要应用包含:可实现动物活体内实时动态成像,检测体内多种光谱信号,获得特异性标记的报告分子或生物标记物在生物体内分布的断层影像,为研究生物组织的结构形态、生理特征、代谢功能、病理特征等提供了重要手段,同时满足现今小动物活体成像趋势所需的“功能”和“结构”成像,主要应用在肿瘤研究、肿瘤药物靶向与代谢检测、血氧分布与浓度研究、分子探针开发、脑科学研究、药物递送、药物动力学与生物分布研究等领域。
关于冷泉港生物
冷泉港生物科技股份有限公司于1987年在中国台湾成立,深耕中国市场的精密仪器及试剂销售30多年,一直致力于将全球生物医学前沿技术引入中国市场并获得独家代理权,如NanoString、MaxCyte、Cell Microsystems、CELLINK、iThera Medical和Phoenix Micron、CYTENA等,助力国内科学研究及转化医学研究。
相关文章
更多 >

