血小板反应蛋白-1经整合素/YAP通路抑铁死亡缓骨关节炎
2025-10-24 来源:本站 点击次数:575Thrombospondin-1 mitigates osteoarthritis progression by inhibiting mechanical stress-induced chondrocyte ferroptosis via the integrin/YAP pathway
Keywords: THBS1; chondrocytes; ferroptosis; mechanical stress; osteoarthritis.
骨关节炎(OA)是一种累及全身关节的退行性疾病,尤其好发于承重关节,显著影响中老年人群的生活质量。随着全球人口老龄化进程加速,OA患者数量持续攀升,已成为临床常见病。然而,目前针对OA的治疗药物主要局限于缓解疼痛症状,无法有效阻止关节软骨的进行性丢失和退变。因此,深入探究OA的发病机制并寻找有效的治疗靶点,以遏制疾病进展,是当前亟待解决的重大临床需求。
点击了解: 仿生压力细胞培养仪
异常的机械应力是诱发和加速OA进展的关键因素。关节软骨细胞暴露于超负荷或异常的机械应力下,可触发多种细胞死亡途径,包括凋亡、坏死以及近年来备受关注的铁死亡。铁死亡是一种铁依赖性的、由脂质过氧化驱动的新型细胞死亡方式,其特征是谷胱甘肽过氧化物酶4(GPX4)活性受抑,导致活性氧(ROS)积累和细胞膜磷脂的氧化损伤。研究表明,机械应力可通过激活压电离子通道等途径诱导软骨细胞发生铁死亡,从而加剧软骨破坏和OA进展。
点击了解: 细胞力学刺激培养
血小板反应蛋白-1(THBS1)是一种重要的细胞外基质蛋白,在细胞-基质相互作用和机械信号转导中扮演关键角色。它作为整合素的重要配体,其构象在机械应力作用下发生改变,暴露出整合素结合位点,从而增强与整合素的结合亲和力。在人类OA患者的承重区域软骨组织中,THBS1蛋白的表达水平显著降低。这提示THBS1表达下降可能与OA的机械应力损伤和软骨细胞死亡密切相关。因此,山东大学齐鲁医院骨科在一项研究中,深入探讨THBS1在机械应力诱导软骨细胞铁死亡中的作用及其分子机制,并评估THBS1作为延缓OA进展的新型治疗策略的潜力。研究成果发表于“Frontiers in immunology”期刊题为“Thrombospondin-1 mitigates osteoarthritis progression by inhibiting mechanical stress-induced chondrocyte ferroptosis via the integrin/YAP pathway”。

首先,研究人员在膝关节骨关节炎(OA)患者的软骨组织样本中,转录组测序分析揭示了一个重要现象,与非负重区域相比,负重区域的THBS1表达显著降低(图1a)。进一步的富集分析显示,细胞外基质(ECM)及其受体相互作用通路在此背景下显著富集(图1b)。鉴于THBS1已被报道在细胞-ECM相互作用中起关键作用,这一发现提示THBS1表达下调可能与机械应力诱导的软骨损伤相关。为验证此关联,分析了OA患者负重区与卸载区的软骨切片。组织学染色清晰显示负重区存在严重的软骨结构破坏,表现为多处软骨裂隙和蛋白聚糖丢失(图1c-e)。更重要的是,免疫组织化学染色证实了负重区软骨细胞中THBS1蛋白表达水平的确降低(图1f,g)。此外,透射电镜观察负重区软骨细胞,发现了线粒体嵴减少、膜增厚等特征性改变,提示存在铁死亡迹象(图1h)。这些结果共同指向THBS1表达减少与OA负重区软骨细胞在机械应力下损伤的密切联系。

图1 在患有膝骨关节炎的病人中,其关节软骨上承受压力的区域,THBS1这种蛋白质的表达量减少了。
然后,为探究THBS1在骨关节炎(OA)中的作用,研究人员构建腺相关病毒载体(AAV-THBS1)进行关节腔过表达实验。将30只Wistar大鼠分为对照组(CON)、AAV-GFP组和AAV-THBS1组,分别注射PBS、AAV-GFP及AAV-THBS1至左膝关节腔(图2a)。注射2周后IVIS检测证实病毒成功递送(图2b),4周时随机取样显示AAV-THBS1组软骨组织THBS1转录及蛋白表达显著高于对照组(图2c-e)。12周龄时建立DMM骨关节炎模型,8周后分析显示,微CT证实AAV-THBS1组显著抑制了OA相关的骨赘增生(图2f,g);Safranin O染色揭示该组软骨破坏程度减轻,OARSI评分降低(图2h,i);IHC分析进一步表明THBS1过表达促进合成代谢标志物表达,同时抑制分解代谢标志物(图2j-n)。这些结果证实THBS1过表达可通过调控软骨代谢平衡延缓OA进展。
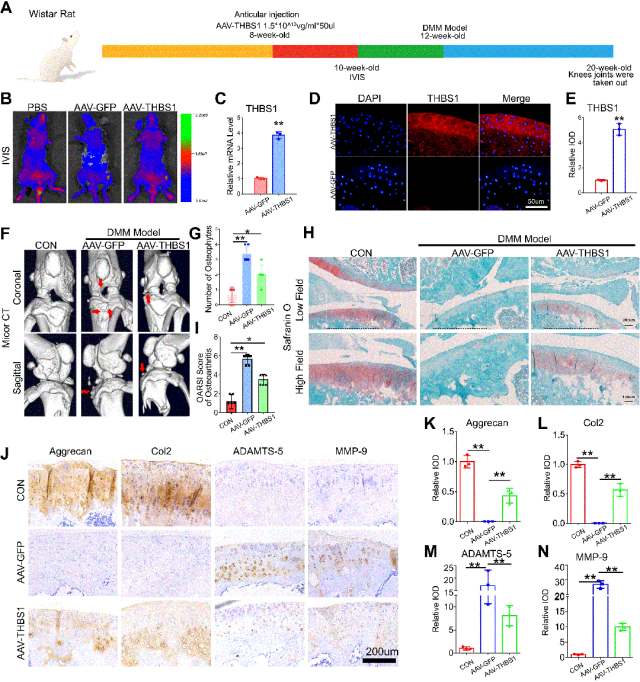
图2 THBS1保护关节软骨并延缓骨关节炎的进展。
接着,为阐明THBS1在机械应力下保护软骨细胞的机制,研究人员建立体外加压模型(1 MPa)。结果显示,异常机械应力可诱导软骨细胞铁死亡,表现为线粒体嵴减少、膜增厚及GPX4表达下降(图3i,j);而添加重组人THBS1(rhTHBS1)能显著逆转上述改变,恢复线粒体活性并降低ROS水平(图3a-h)。同时,rhTHBS1上调合成代谢标志物和GPX4的表达,抑制分解代谢因子的转录与蛋白水平(图3j-l)。关键验证实验中,软骨特异性GPX4敲除小鼠失去THBS1的骨保护作用,表现为骨赘增生加剧和软骨损伤恶化。此外,rhTHBS1同样可拮抗RSL3引发的线粒体功能障碍和GPX4抑制。这些结果证实THBS1通过调控GPX4依赖性铁死亡通路抵抗机械应力损伤。

图3 THBS1抑制过度机械应力诱导的软骨细胞铁死亡。
为阐明THBS1调控机械应力诱导软骨细胞铁死亡的机制,研究人员通过STRING数据库构建THBS1互作网络,发现其与整合素β1、β3及CD36、CD47等受体存在潜在关联(图4A)。聚焦细胞膜受体(图4B),免疫荧光染色显示,在机械应力刺激下,THBS1与整合素β1显著共定位,而与整合素β3、CD36、CD47无共定位现象(图4C,D)。进一步通过Co-IP实验验证,THBS1抗体在机械应力条件下可特异性沉淀整合素β1,而在静态条件下结合较弱(图4E)。该结果证实机械应力增强THBS1与整合素β1的直接结合,为解析其下游信号通路奠定基础。
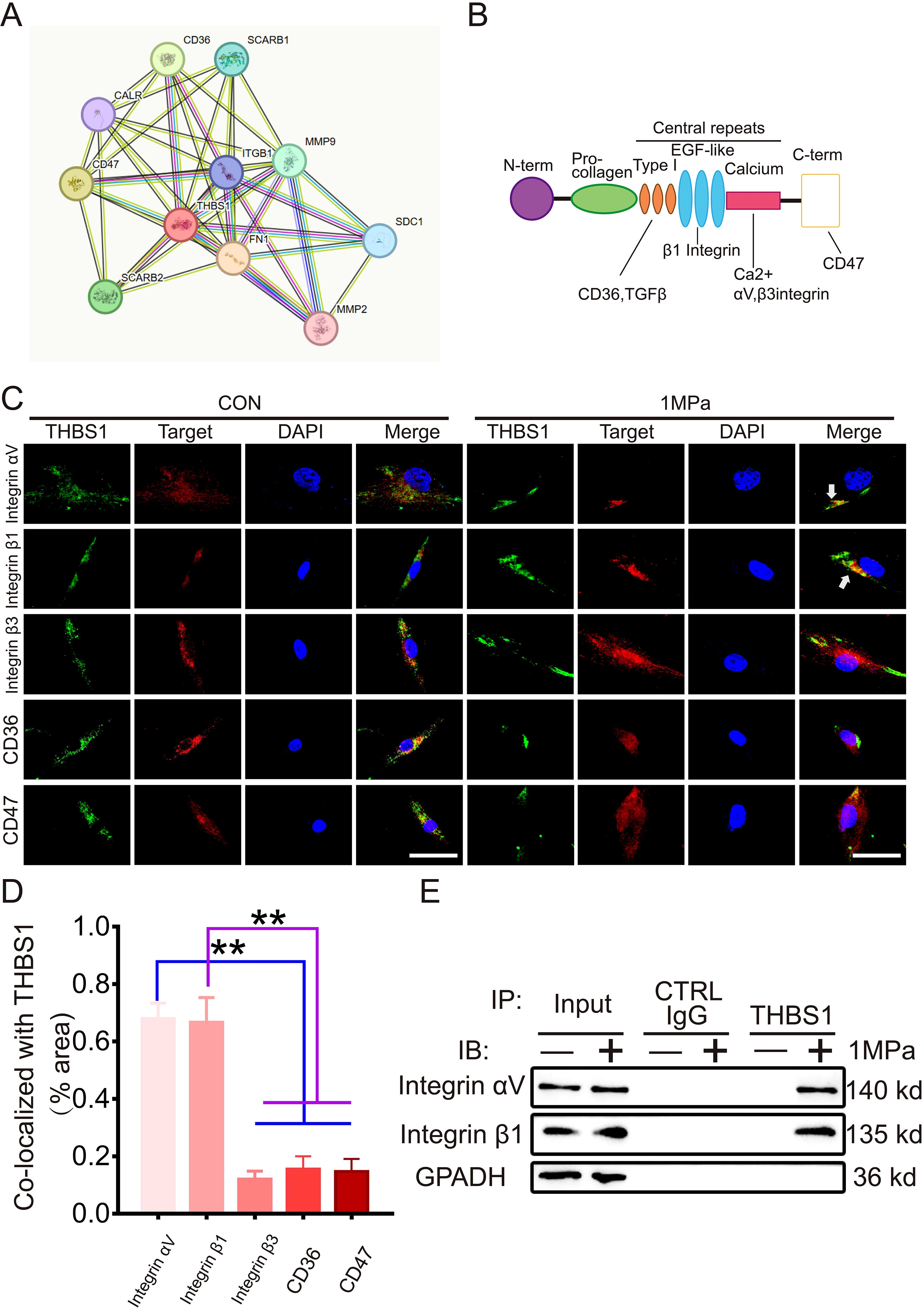
图4 在机械应力作用下,THBS1与整合素αVβ1之间的相互作用增强。
为验证THBS1是否通过整合素β1通路抑制机械应力诱导的软骨细胞铁死亡,研究人员引入整合素β1抑制剂进行阻断实验。结果显示,机械应力下rhTHBS1原本可恢复的细胞活性(图5A,B)和线粒体功能(图5C,D)在整合素抑制后完全失效;透射电镜观察到抑制剂组线粒体嵴消失、膜破裂等典型铁死亡特征(图5E)。同时,rhTHBS1对机械应力下ROS清除(图5F-I)、GSH水平维持(图5J)以及代谢标志物的调控作用均被抑制剂逆转(图5K-N)。这些数据证实THBS1通过整合素β1依赖的分子机制调控GPX4活性及氧化还原平衡,从而抵抗机械应力诱导的铁死亡。
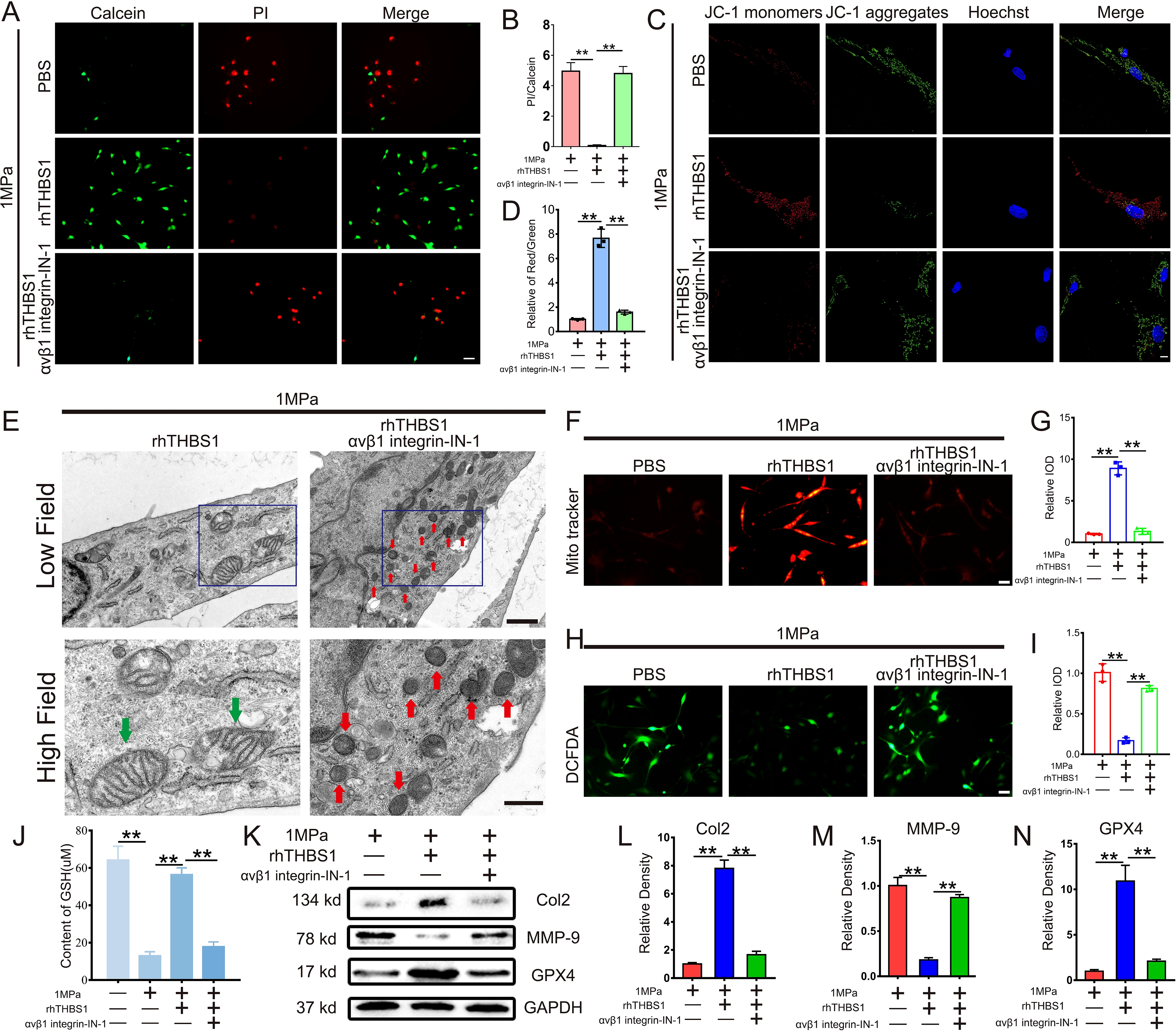
图5 THBS1通过整合素αVβ1抑制机械应力诱导的软骨细胞铁死亡。
为解析THBS1通过整合素/YAP通路调控软骨细胞铁死亡的机制,研究人员发现,机械应力刺激下,敲低THBS1可显著抑制YAP1的核转位(图6a-d);而外源性rhTHBS1通过整合素β1信号促进YAP1核转位及蛋白表达,该效应可被整合素抑制剂阻断(图6e-h)。功能验证显示,YAP1抑制剂可消除rhTHBS1对机械应力诱导的铁死亡的保护作用,表现为线粒体膜电位降低(图6l,m)、GSH耗竭(图6n)及线粒体结构损伤(图6k)。这些结果证实THBS1通过整合素β1/YAP1轴增强软骨细胞抗氧化能力,维持线粒体稳态以抵抗铁死亡。
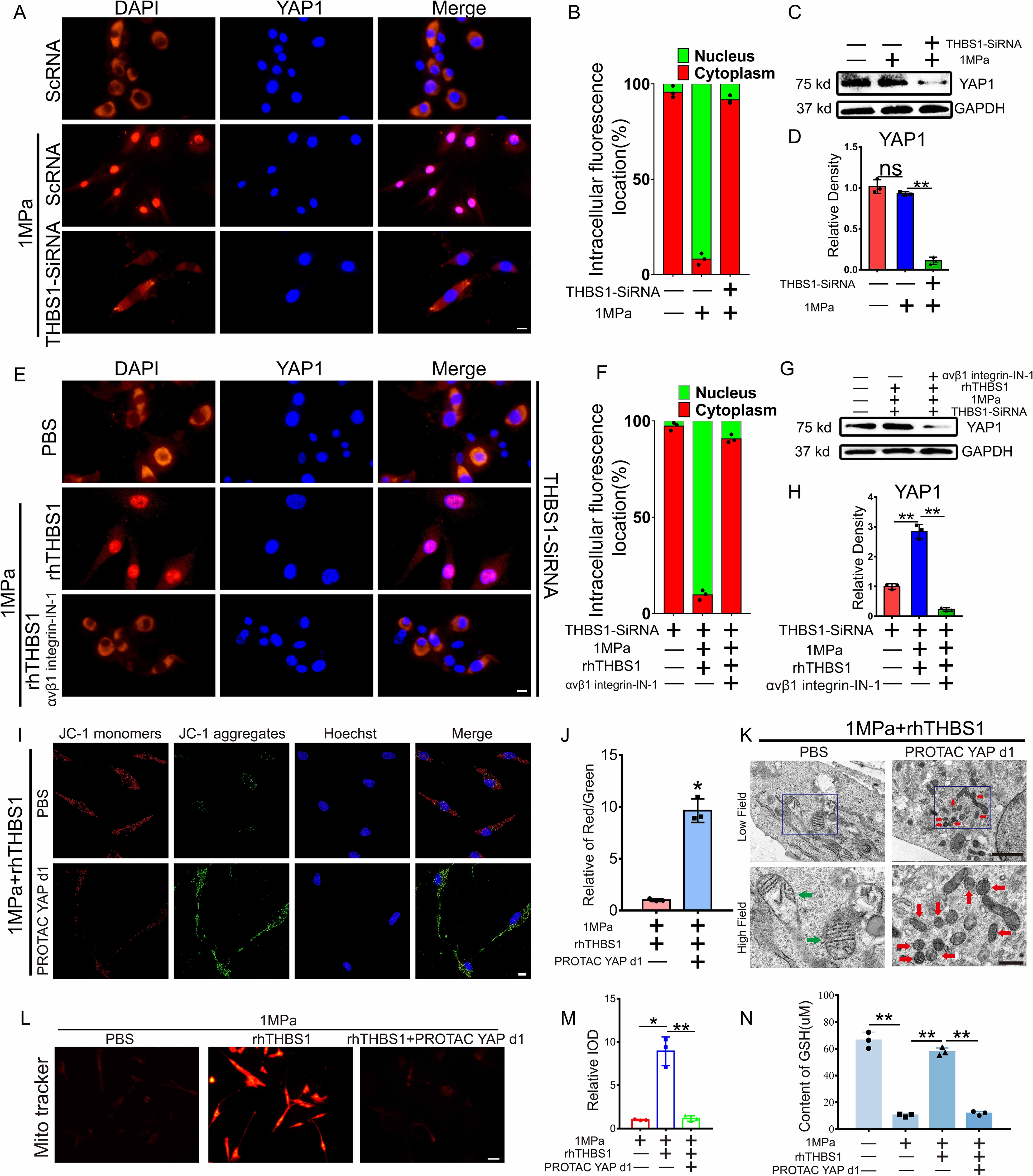
图6 THBS1通过整合素V1/YAP通路抑制软骨细胞铁死亡。
最后,为评估THBS1样肽(ABT-510)的治疗潜力,研究人员在小鼠DMM骨关节炎模型中开展实验。术后给予膝关节腔注射ABT-510,8周后分析显示,Micro-CT证实ABT-510组骨赘形成显著减少(图7b,c);Safranin O染色显示关节软骨破坏减轻,OARSI评分降低(图7d,e);IHC分析表明ABT-510促进合成代谢标志物表达,抑制分解代谢因子表达(图7f-n)。综上,THBS1模拟肽ABT-510通过调控软骨代谢平衡有效延缓OA进展。
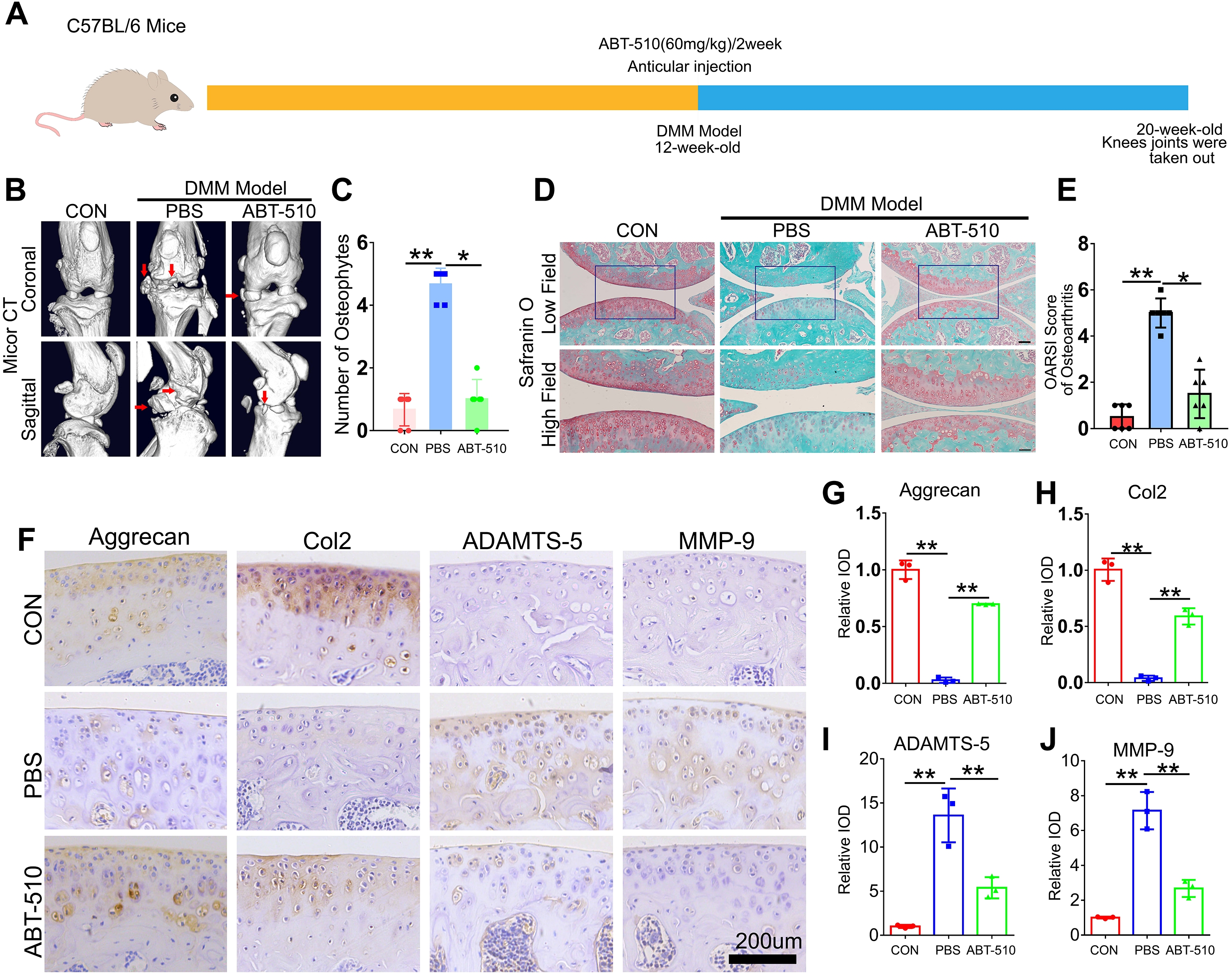
图7 研究表明,THBS1样肽能显著抑制骨关节炎的进展并保护关节软骨。
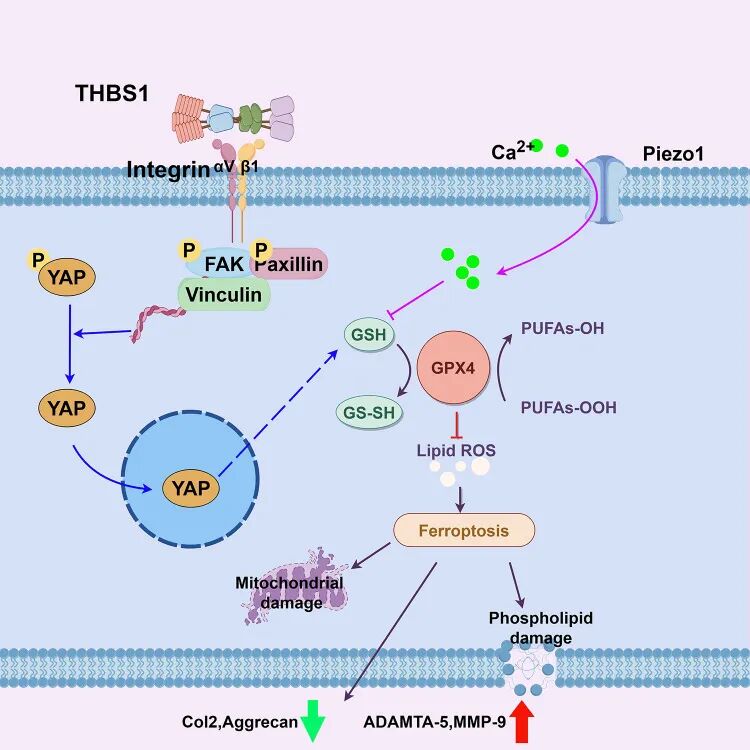
图8 图片摘要。
总之,研究揭示血小板反应蛋白-1(THBS1)通过整合素β1/YAP信号轴调控机械应力诱导的软骨细胞铁死亡,为骨关节炎(OA)治疗提供新靶点。机械应力通过激活整合素β1介导THBS1构象改变,促进其与整合素结合并激活YAP核转位,进而维持谷胱甘肽(GSH)稳态和GPX4活性,抑制脂质过氧化及线粒体损伤。该通路阐明机械应力通过THBS1-整合素β1-YAP-GPX4级联反应驱动OA进展,靶向该通路通过平衡软骨代谢有效延缓疾病发展。
参考文献:Wang S, Zhou X, Zhang F, Zhai H, Zhang Y, Guo Y. Thrombospondin-1 mitigates osteoarthritis progression by inhibiting mechanical stress-induced chondrocyte ferroptosis via the integrin/YAP pathway. Front Immunol. 2025 May 22;16:1577234. doi: 10.3389/fimmu.2025.1577234. PMID: 40475787; PMCID: PMC12137073.
原文链接:https://pubmed.ncbi.nlm.nih.gov/40475787/
图片来源:所有图片均来源于参考文献
小编旨在分享、学习、交流生物科学等领域的研究进展。如有侵权或引文不当请联系小编修正。如有任何的想法以及建议,欢迎联系小编。感谢各位的浏览以及关注!进入官网www.naturethink.com或关注“Naturethink”公众号,了解更多相关内容。
点击了解: 仿生压力细胞培养仪
点击了解: 细胞力学刺激培养

