文献解读:NR4A3-FOS轴关键作用的发现破解CAR-T耗竭难题
2026-04-29 来源:本站 点击次数:57
嵌合抗原受体(CAR)T 细胞在肿瘤微环境中的功能障碍,是其治疗实体瘤效果不佳的主要障碍。
陆军军医大学卞修武教授团队在Science Advances发表题为” Enhanced FOS expression improves tumor clearance and resists exhaustion in NR4A3-deficient CAR-T cells under chronic antigen exposure”文章。
通过对胶质瘤患者肿瘤浸润 T 细胞进行单细胞 RNA 测序分析,研究发现NR4A 家族基因与 T 细胞耗竭密切相关,且与功能障碍基因HAVCR2和TIGIT共表达。值得注意的是,NR4A3 敲低的 CAR-T 细胞表现出增强的肿瘤杀伤活性,在体内可更有效地清除肿瘤并延长生存期。然而,这种抗耗竭表型的提升会随着肿瘤负荷的持续存在而减弱。T 细胞功能的这种下降,与 NR4A3 敲低后慢性抗原暴露所诱导的FOS 代偿性下调有关。在敲低 NR4A3 的同时过表达 FOS,可通过改变 CAR-T 细胞的表型与转录谱,使其远离耗竭、转向更强的效应功能,从而显著增强其抗肿瘤应答。
这些发现为 CAR-T 细胞治疗的临床改造提供了一种具有前景的策略。
实验部分
1. 验证CAR-T细胞的肿瘤浸润能力
在胶质母细胞瘤(GBM)小鼠异种移植模型中,研究通过免疫荧光染色标记肿瘤组织中的CD3(CAR-T细胞标志物)和CD31(血管标志物),并利用 TissueFAXS 系统在20×放大倍数下采集图像。该技术能够清晰呈现CAR‑T细胞在肿瘤局部的分布特征,直接证明**FOS过表达联合NR4A3敲低(FOS OE/NR4A3 KD)的CAR-T细胞具有更广泛的肿瘤浸润范围**,为其增强的 antitumor活性提供了形态学证据。
2. 支持肿瘤微环境中细胞相互作用的可视化
TissueFAXS的高分辨率成像能力可区分肿瘤细胞、CAR-T细胞及血管结构的空间关系,帮助研究者观察CAR-T细胞是否成功穿透肿瘤组织并靠近靶细胞,为“CAR-T细胞浸润不足是实体瘤治疗瓶颈”这一核心问题提供了直接观察依据,也验证了基因修饰策略对改善浸润的作用。
3. 提供定量分析的可靠图像基础
研究中对9个不同组别的肿瘤组织切片进行成像分析,通过该技术获取的标准化图像可用于后续定量统计(如CAR-T细胞浸润密度、血管分布密度等),为各组别间的疗效差异提供客观的形态学量化支持,确保实验结果的可重复性和说服力。
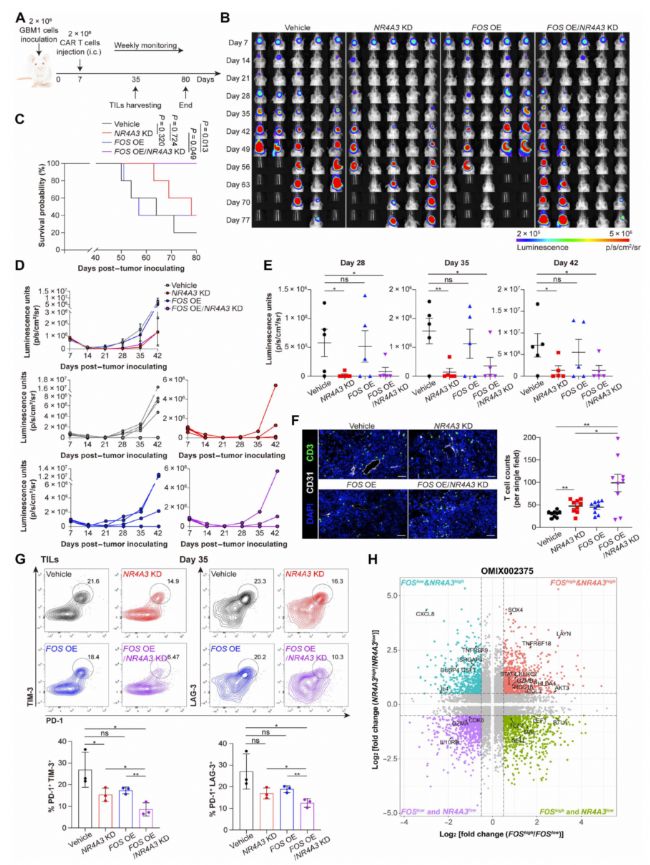 Figure 7 FOS 过表达联合 NR4A3 敲低通过抑制 T 细胞耗竭增强 CAR-T 细胞体内抗肿瘤活性
Figure 7 FOS 过表达联合 NR4A3 敲低通过抑制 T 细胞耗竭增强 CAR-T 细胞体内抗肿瘤活性

陆军军医大学卞修武教授团队在Science Advances发表题为” Enhanced FOS expression improves tumor clearance and resists exhaustion in NR4A3-deficient CAR-T cells under chronic antigen exposure”文章。
通过对胶质瘤患者肿瘤浸润 T 细胞进行单细胞 RNA 测序分析,研究发现NR4A 家族基因与 T 细胞耗竭密切相关,且与功能障碍基因HAVCR2和TIGIT共表达。值得注意的是,NR4A3 敲低的 CAR-T 细胞表现出增强的肿瘤杀伤活性,在体内可更有效地清除肿瘤并延长生存期。然而,这种抗耗竭表型的提升会随着肿瘤负荷的持续存在而减弱。T 细胞功能的这种下降,与 NR4A3 敲低后慢性抗原暴露所诱导的FOS 代偿性下调有关。在敲低 NR4A3 的同时过表达 FOS,可通过改变 CAR-T 细胞的表型与转录谱,使其远离耗竭、转向更强的效应功能,从而显著增强其抗肿瘤应答。
这些发现为 CAR-T 细胞治疗的临床改造提供了一种具有前景的策略。
实验部分
1. 验证CAR-T细胞的肿瘤浸润能力
在胶质母细胞瘤(GBM)小鼠异种移植模型中,研究通过免疫荧光染色标记肿瘤组织中的CD3(CAR-T细胞标志物)和CD31(血管标志物),并利用 TissueFAXS 系统在20×放大倍数下采集图像。该技术能够清晰呈现CAR‑T细胞在肿瘤局部的分布特征,直接证明**FOS过表达联合NR4A3敲低(FOS OE/NR4A3 KD)的CAR-T细胞具有更广泛的肿瘤浸润范围**,为其增强的 antitumor活性提供了形态学证据。
2. 支持肿瘤微环境中细胞相互作用的可视化
TissueFAXS的高分辨率成像能力可区分肿瘤细胞、CAR-T细胞及血管结构的空间关系,帮助研究者观察CAR-T细胞是否成功穿透肿瘤组织并靠近靶细胞,为“CAR-T细胞浸润不足是实体瘤治疗瓶颈”这一核心问题提供了直接观察依据,也验证了基因修饰策略对改善浸润的作用。
3. 提供定量分析的可靠图像基础
研究中对9个不同组别的肿瘤组织切片进行成像分析,通过该技术获取的标准化图像可用于后续定量统计(如CAR-T细胞浸润密度、血管分布密度等),为各组别间的疗效差异提供客观的形态学量化支持,确保实验结果的可重复性和说服力。

相关文章
更多 >

