文献解读:mIHC多色病理分析助力发现肝癌免疫治疗新靶点
2024-08-15 来源:本站 点击次数:1910肝细胞癌(HCC)是临床常见的恶性肿瘤,发病机制尚未完全明确,其治疗手段也有限。目前肝癌的系统治疗可分为多激酶抑制剂和免疫治疗两大类,然而,由于激酶抑制剂的不良反应和免疫治疗的低应答率,迫切需要开发更有效的肝癌治疗方法。
肝脏是人体的主要代谢器官,而3-氧酸辅酶a转移酶1 (OXCT1)作为酮解的关键酶,在成人肝细胞中表达不足。据之前的研究发现,OXCT1在肝癌细胞中高表达,促进其在营养受限条件下的存活。此外,程序性肿瘤相关巨噬细胞(programmed tumor-associated macrophages,TAM) 在HCC肿瘤微环境中的发育对肿瘤的发生和生长均具有重要意义。然而,OXCT1在肿瘤免疫微环境(TIME)中的表达模式以及OXCT1在TAMs中的功能仍不清楚。

广东省人民医院廉哲雄教授及高平教授团队于2024年5月15日在Journal of Hepatology(IF:26.8)上发表了题为“Targeting OXCT1-mediated ketone metabolism reprograms macrophages to promote antitumor immunity via CD8+ T cells in hepatocellular carcinoma”的研究成果。
该研究通过mIHC多色病理分析发现抑制肿瘤相关巨噬细胞中OXCT1异常表达,可通过琥珀酸-H3K4me3-Arg1轴减少CD8+ T细胞的耗竭,从而抑制肝癌进程。佰诺全景为本项研究提供了全景病理检测试剂盒PPD520和PPD690 (Cat# 0004100100)。

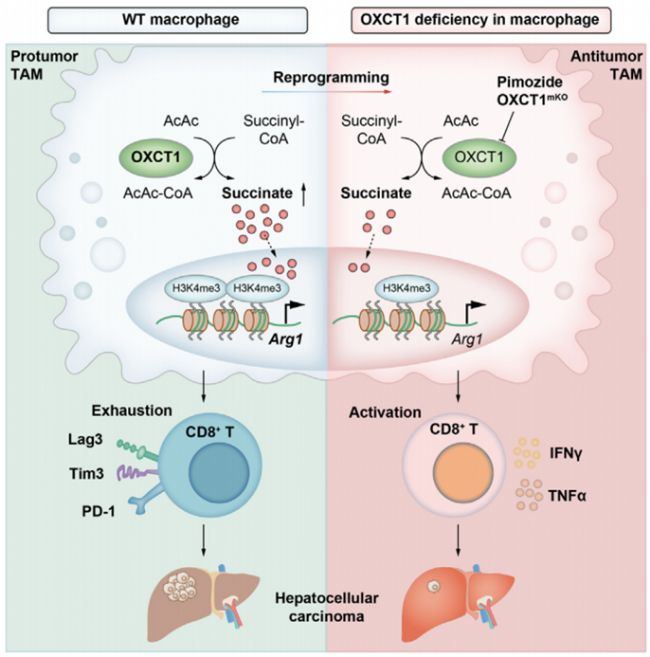
通过研究机制发现,OXCT1高表达诱导TAMs中酮体代谢的副产物琥珀酸的积累,通过增加Arg1启动子中H3K4三甲基化(H3K4me3)水平促进Arg1转录。此外,Pimozide(匹莫扎特)作为OXCT1的抑制剂,抑制Arg1的表达以及TAM向肿瘤表型的极化,导致CD8+ T细胞耗竭减少,肿瘤生长减慢,而且巨噬细胞中OXCT1的高表达与HCC患者的低生存率呈正相关。据研究结果表明OXCT1在表观上抑制抗肿瘤免疫,提示在TAMs中抑制OXCT1活性是治疗肝癌的潜在新靶点。
为了研究OXCT1在体内HCC中的表达模式,该研究对人HCC标本进行了mIHC多色病理分析检测(Panel:CD68、OXCT1),结果显示,OXCT1在HCC巨噬细胞中的表达高于正常肝巨噬细胞。此外,巨噬细胞OXCT1的高表达与HCC患者预后不良相关。

为了验证上述结果,探索OXCT1在小鼠HCC中TAMs中的表达水平,再构建巨噬细胞特异性缺失OXCT1的小鼠模型。这些结果表明,敲除TAMs中的OXCT1可促进CD8+ T细胞的增殖,这意味着巨噬细胞OXCT1通过调节CD8+ T细胞促进HCC进展,并且流式细胞术数据进一步证实了这些结论。

综合全文,此研究强调了OXCT1在TAMs介导的免疫抑制及其对HCC进展的影响中的关键作用。通过阐明TAMs介导的免疫逃避的分子机制和抑制OXCT1在TAMs中的潜在治疗益处,该研究为开发增强抗肿瘤免疫反应和改善HCC治疗结果的新策略提供了有价值的见解。
参考文献:
Zhe-Xiong Lian, Ping Gao, Chu-Xu Zhu, et al. Targeting OXCT1-mediated ketone metabolism reprograms macrophages to promote antitumor immunity via CD8+ T cells in hepatocellular carcinoma. J Hepatol. 2024 May 15:S0168-8278 (24) 00342-8.


