单细胞打印加速In Vivo CAR-T抗癌新疗法
2025-10-11 来源:本站 点击次数:843随着细胞治疗领域的快速发展,In Vivo CAR-T(体内CAR-T)疗法成为行业新焦点。与传统体外制备CAR-T不同,这项技术只需向患者体内注射携带CAR基因的病毒载体,便能直接在体内“就地”改造T细胞,大大简化治疗流程,为患者争取宝贵时间。
01 巨头押注,In Vivo CAR-T站上风口
2025年,In Vivo CAR-T领域捷报频传:阿斯利康以总价10亿美元收购EsoBiotec,将其工程化纳米抗体慢病毒平台收入囊中;艾伯维则以高达21亿美元全现金收购了专注于该领域的Capstan Therapeutics。
巨头的巨额押注,凸显了In Vivo CAR-T的巨大潜力。相比传统体外CAR-T,其优势显著:
1 流程简化
摆脱复杂的个体化生产流程,患者无需经历细胞采集、体外改造、扩增回输等漫长过程。
2 成本降低
治疗成本有望大幅下降,让更多患者受益。
专家观点:易慕峰生物研发中心负责人郝瑞栋博士指出:“我们的全新In Vivo技术平台,成功打破了国外企业在关键元件上的专利壁垒。”
临床层面,易慕峰基于慢病毒载体的平台已在临床前展现出出色性能。而EsoBiotec的ESO-T01作为第1个进入人体试验的体内BCMA CAR-T候选药物,在复发/难治性多发性骨髓瘤患者中实现了100%的客观缓解率,成果令人鼓舞。
表1:In Vivo与Allo CAR-T核心特点与临床进展对比表
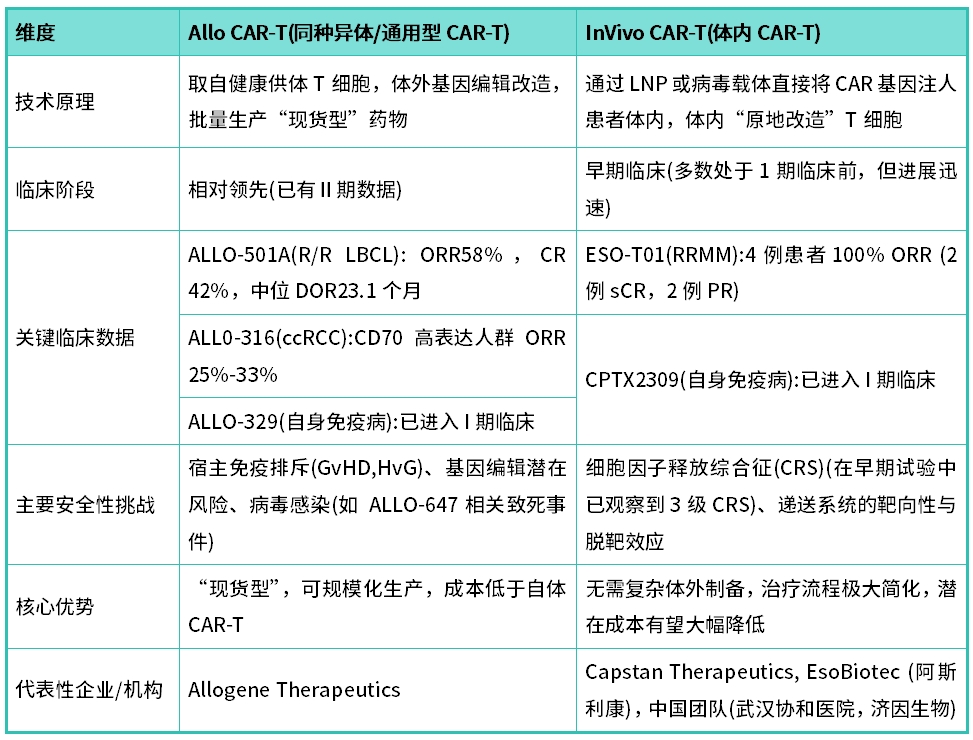
02 慢病毒载体:体内CAR-T的“基因快递员”
在In Vivo CAR-T开发中,递送系统的选择至关重要。目前,慢病毒载体因其可实现单次给药、靶向性强、免疫原性低且临床经验丰富,成为主流选择。然而,传统的慢病毒生产工艺面临滴度波动大、成本高、批次一致性差等挑战,难以满足体内治疗的大规模生产需求。
破解这一瓶颈的关键在于稳定细胞系的开发。以深研生物的EuLV稳转细胞系生产系统为例,通过使用可诱导的稳定生产细胞系,在化学成分确定的培养基中生产,实现了病毒产量提升近百倍、生产成本降低80%的巨大飞跃,为产业化奠定了坚实基础。
稳转细胞系构建通常分为三步:
构建包装细胞系:将慢病毒包装基因稳定插入宿主细胞基因组。
插入目标基因:将CAR基因稳定插入包装细胞系,筛选出高产、稳定的单克隆。
规模化生产:在化学成分限定培养基中进行高密度悬浮培养,诱导生产慢病毒载体。
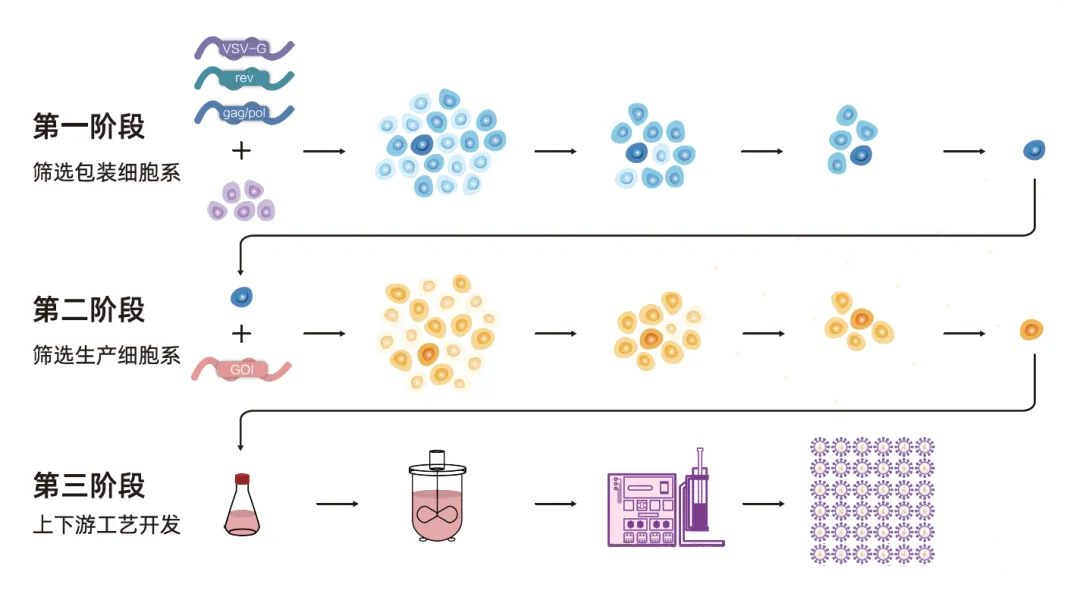 图1:稳转细胞系构建路线图
图1:稳转细胞系构建路线图03 单细胞打印机:筛选高产细胞系的“神助攻”
在构建稳定细胞系的过程中,最关键的一步是筛选出高产、高稳定性的单克隆细胞。而单细胞打印技术正是在这一环节发挥着“神助攻”的关键作用。
这项技术已在产业界得到成功验证。例如,国际药企葛兰素史克(GSK)在其发表于《Molecular Therapy Methods & Clinical Development》(2020)的研究中,详细阐述了如何利用Cytena单细胞打印机,高效构建用于慢病毒载体生产的稳转细胞系。
该研究通过单细胞打印筛选出的高产单克隆,在摇瓶规模下生产的未浓缩慢病毒载体功能性滴度即可稳定超过1×10⁷ TU/mL,与高效瞬时转染的产量相当(图2)。
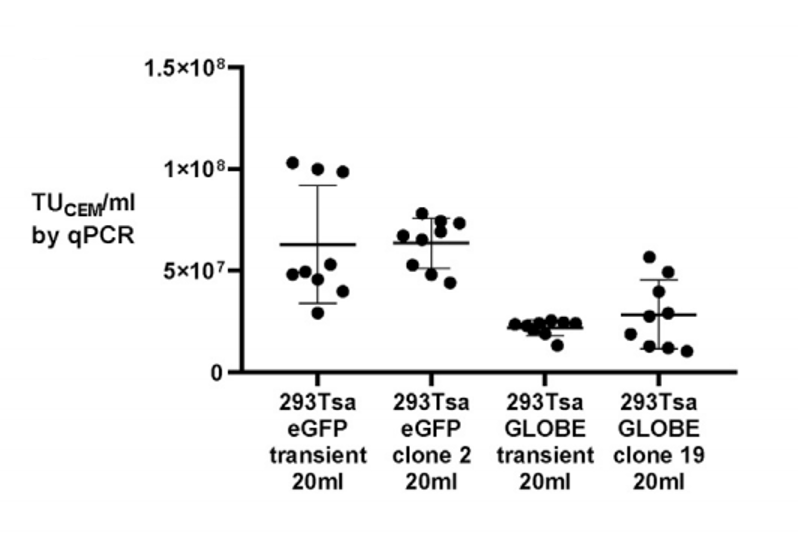 图2:在摇瓶中通过瞬时转染和稳定生产细胞系获得慢病毒载体滴度图。各点表示9个摇瓶中每个的滴度
图2:在摇瓶中通过瞬时转染和稳定生产细胞系获得慢病毒载体滴度图。各点表示9个摇瓶中每个的滴度更重要的是,这些由单克隆衍生的细胞系展现出卓越的遗传稳定性——在连续传代培养超过20个代次后,其载体滴度和整合的载体基因拷贝数均未发生显著衰减(图3)。
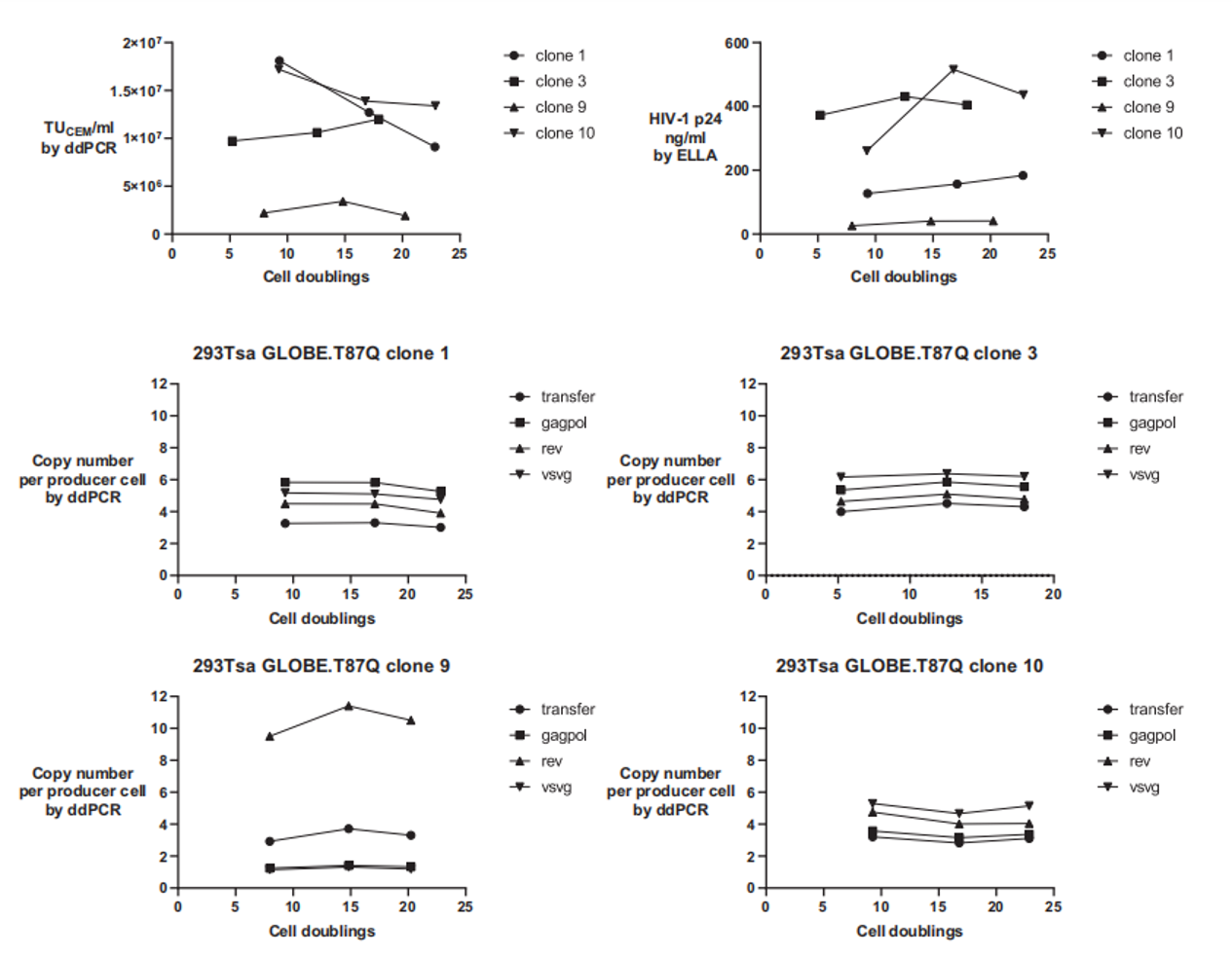 图3:克隆在超过20个细胞倍增的过程中,功能滴度(TU/mL)和物理滴度(p24)保持稳定。
图3:克隆在超过20个细胞倍增的过程中,功能滴度(TU/mL)和物理滴度(p24)保持稳定。最终,该研究成功将筛选出的克隆放大至50升一次性搅拌罐生物反应器进行生产,单个批次即可收获高达2×10¹¹总功能性TU的慢病毒载体(图4),理论上足以满足10名患者的治疗需求。这一案例充分证明了基于单细胞打印的克隆筛选策略,是实现稳定、高产、可规模化慢病毒生产工艺的基石。
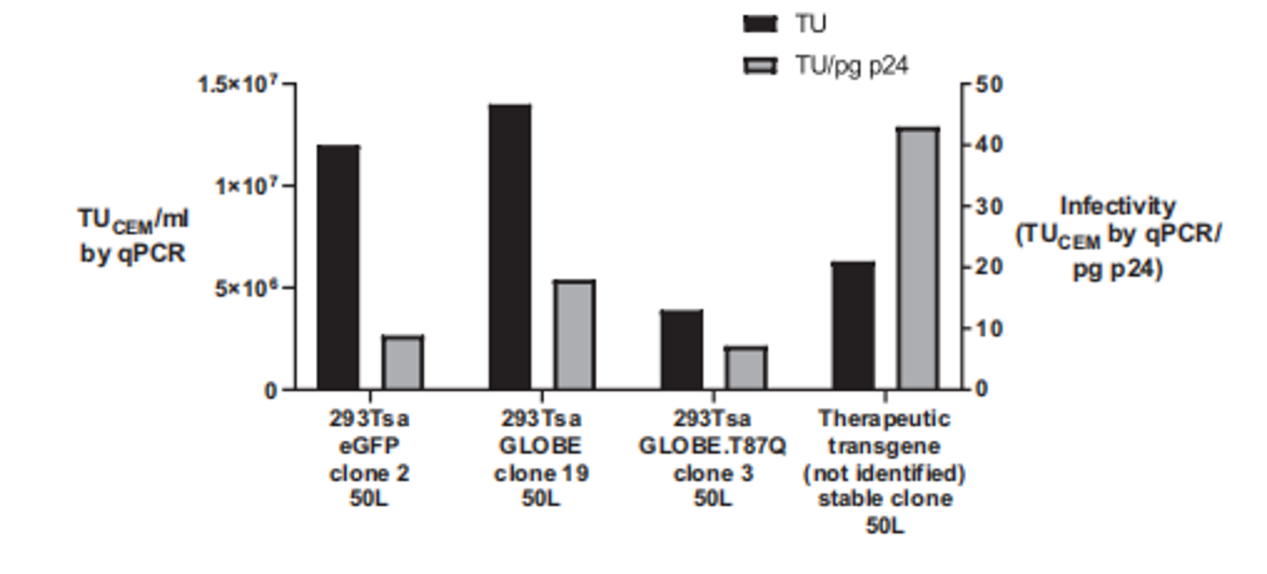
图4:48小时后收获50L批次的结果图。未浓缩载体的功能滴度范围为0.4 ~ 1.4 107 TUCEM/mL,感染性范围为7 ~ 43 TUCEM/pg p24。
单细胞打印技术的核心优势如下:
智能筛选
可设定细胞直径、圆度、荧光强度等多参数,真正筛选出“强壮合格”的细胞,提高单克隆形成率。
高效快速
分选一个96孔板仅需1-2分钟,单细胞率大于95%。
操作简便
设备无需复杂维护清洗,采用一次性无菌打印芯片,杜绝交叉污染。
精准定位
可调整液滴位置,确保液滴滴入孔板中央,细胞沉降到孔底后能轻松拍到Day0的单细胞图片,避免ghost well问题。
证据追溯
分选过程自动拍摄多张喷嘴图片,完整记录单克隆来源,满足监管机构对单克隆源性的严苛要求。
04 未来可期:技术融合加速CAR-T产业化
随着生物制药行业对细胞系单克隆性的要求日益严格,单细胞打印技术的重要性将愈发凸显。从GSK等企业的成功实践可以看出,单细胞打印技术是产业化工艺中确保克隆源性、合规性与一致性的关键环节。它与慢病毒生产技术的深度融合,正推动细胞治疗工艺向更高效、规范、可追溯的方向发展。未来,我们有望见证更多基于In Vivo CAR-T的治疗方案获批上市,为全球癌症患者带来新的希望。而单细胞打印技术,将继续作为幕后功臣,在这一进程中扮演不可或缺的角色。
参考资料:
- 2025 ASGCT | 易慕峰In Vivo体内CAR-T技术平台重磅亮相
- In Vivo与Allo CAR-T:谁先攻克商业化堡垒?
- 体内细胞疗法工艺新突破:EuLV稳转细胞系慢病毒载体系统高效突破LVV生产瓶颈
- Chen, Y.H., et al. (2020). Rapid Lentiviral Vector Producer Cell Line Generation Using a Single DNA Construct. Mol Ther Methods Clin Dev.
相关文章
更多 >

