共表达提高CHO细胞的克隆效率和蛋白质产量
2026-01-20 来源:本站 点击次数:408中国仓鼠卵巢 (CHO) 细胞系广泛应用于生物制药行业,特别是用于生产单克隆抗体和重组蛋白药物。重组细胞系通常来源于单细胞克隆,以确保产品的一致性和稳定性。然而,难以表达的重组蛋白可能会抑制单细胞增殖,从而显著降低克隆效率。如何提高“难表达蛋白”的单克隆化效率和重组蛋白产量呢,齐鲁制药新发表在《Protein Expression and Purification》上的文章提供了新思路。

研究内容
1. 问题背景:
CHO细胞是生产治疗性蛋白(如单克隆抗体)的关键平台,但表达“难表达蛋白”时会显著抑制细胞增殖,导致单克隆化效率低(即单细胞形成克隆的成功率低),延缓细胞株开发进程。
2. 创新策略:构建共表达载体 pCGS3.0-IGF1-P04,将胰岛素样生长因子-1(IGF-1,其可促进细胞周期进程并抑制凋亡。)基因通过内部核糖体进入位点(IRES)与目标难表达蛋白 P04 串联,转染至 CHOZN® GS-/-细胞中。IGF-1共表达通过显著提高克隆效率并实现难以表达蛋白的稳定生产,代表了一种有效的单细胞克隆策略。
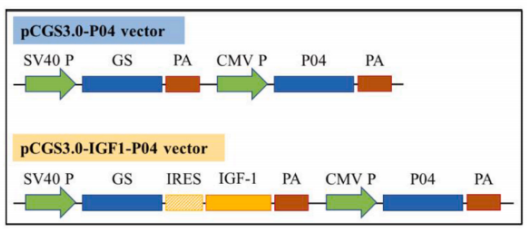
3. 关键技术:
使用 Cytena Single-Cell Printer™ 进行全自动单细胞分选,确保单克隆源性。
- 通过成像系统追踪单细胞增殖,定量克隆效率。
- 在两种培养基(A/B)中评估细胞生长、蛋白产量及代谢参数。
1.克隆效率显著提升:
IGF-1共表达使细胞的单克隆效率在Medium A中为53.3%,较对照组提高了196%;在Medium B中为89%,较对照组提高了53%。
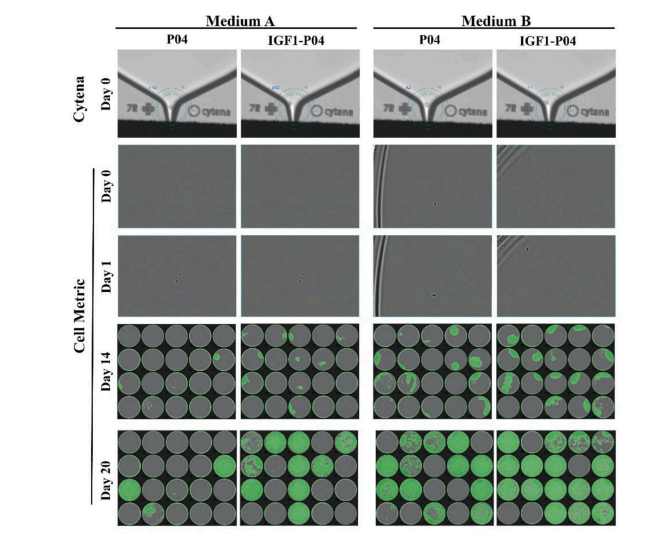
首先,使用 Cytena Single-Cell Printer进行自动单细胞分选。随后,使用成像仪监测单克隆细胞的铺板效率和生长。到第14天,在两种培养基中,IGF-1共表达克隆细胞表现出比对照细胞显著更高的汇合度和增殖能力。
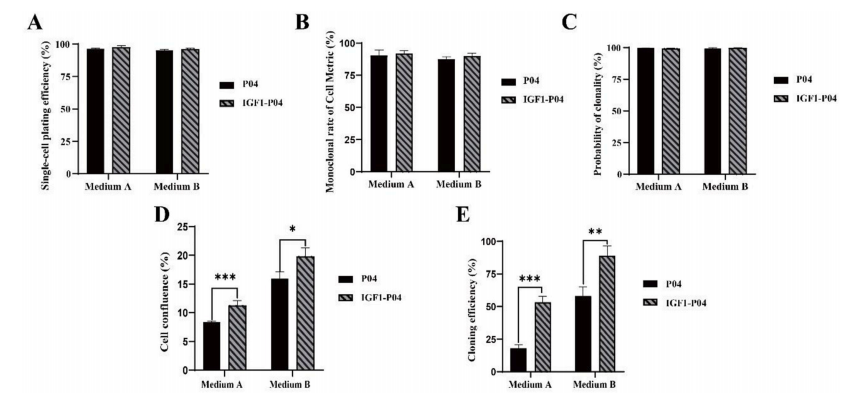
在分选当天(第 0 天),所有组的单细胞铺板效率在95%到97%之间(图A)。根据第0天和第1天收集的成像数据,证实了所有组的单细胞铺板效率约为90%(图B)。根据Cytena Single-Cell Printer与成像仪的图像数据,计算出所有组均达到 >99% 的单克隆源性(图C)。这些结果表明所有组的分选效率高且相当。到第14天,在培养基A和B中,IGF-1共表达细胞的汇合度分别比对照高出35%和24%(图D)。培养20天后,IGF-1共表达细胞的克隆效率显著高于对照细胞:在培养基A中为53.3%(相对于对照增加了 196%,p< 0.001),在培养基B中为 89%(增加了 53%,p< 0.01)(图E)。总的来说,这些结果表明IGF-1共表达显著增强了单细胞增殖和克隆效率,并且在不同培养条件下均表现出稳健的性能。因此,该策略代表了优化生物制药开发中单细胞克隆的一项重大进展。
2.细胞生长与产量增强:- 单克隆细胞密度(VCD)提高29–64%;
- 目标蛋白 P04 产量提升47–89%,主要源于细胞增殖加速而非单位细胞生产率(qP)变化。
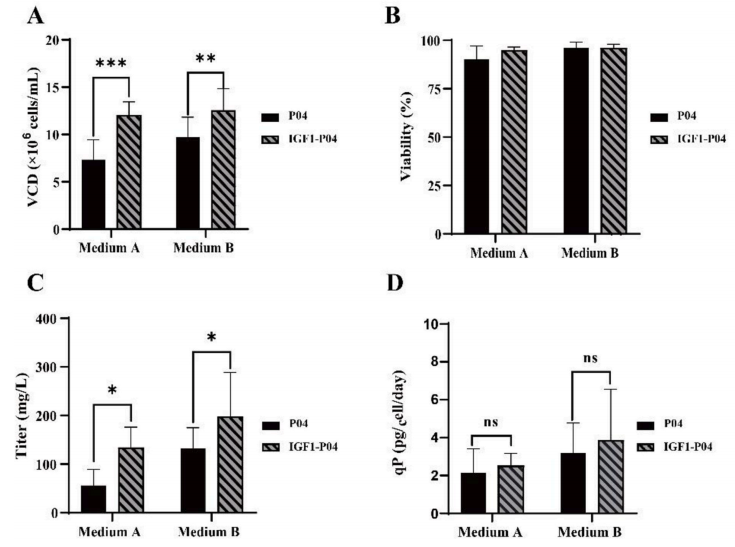
为了研究IGF-1共表达对单克隆细胞生长和蛋白质生产的影响,使用两种培养基(培养基A和培养基B)在125 mL 摇瓶中进行了批次实验。结果表明,在两种培养基中,共表达IGF-1的克隆的平均 VCD 显著高于未共表达IGF-1的克隆,在培养基A中增加了64%(p<0.001),在培养基B中增加了29%(图A, p<0.01)。两组的细胞活力均保持在 >90%(图B),表明IGF-1共表达在维持高活力的同时有效促进了细胞生长。此外,在两种培养基中,共表达IGF-1的克隆的产品产量均显著高于未共表达IGF-1的克隆,在培养基A和B中平均分别增加了89%和47%(图C, p<0.05)。有趣的是,在IGF-1共表达组和非共表达组之间未观察到 qP 的显著差异(图D)。这些结果表明,产品产量的增加可能主要源于细胞生长的增强,而不是 qP 的变化。
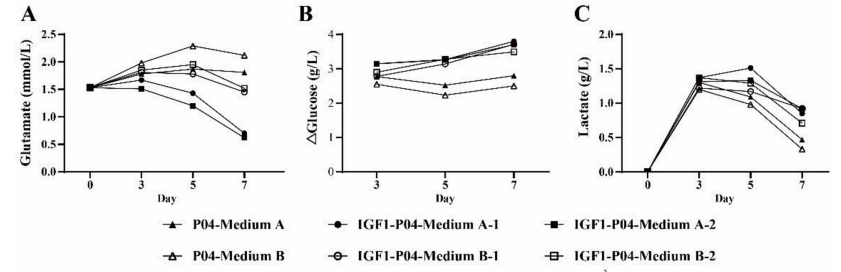
3.代谢优化:共表达克隆的葡萄糖/谷氨酸消耗增加,乳酸积累略有增加(这可能是葡萄糖消耗增加的结果)(见下图),表明IGF-1改善了能量代谢效率。
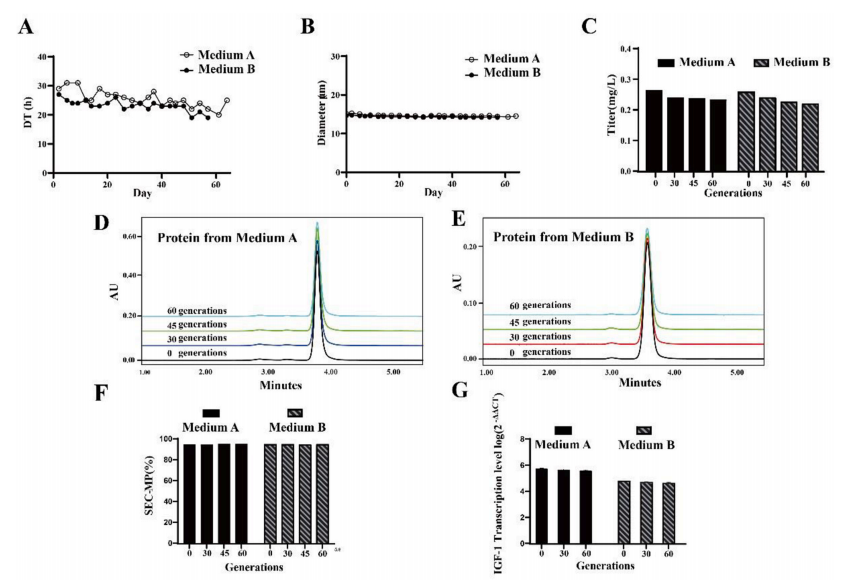
4.长期稳定性:
连续培养60代后,蛋白产量波动<15%,关键质量属性(如SEC纯度)及IGF-1转录水平稳定(见下图),符合工业化生产要求。
结论
IGF-1共表达是一种高效、稳定的单克隆化策略,能显著克服难表达蛋白对CHO细胞增殖的抑制,提升克隆效率与产量,且不影响长期生产稳定性。结合自动化设备(如Cytena单细胞打印机),该方法可加速高产量细胞株的开发,为生物制药提供可靠解决方案。

· 关于艾贝泰 ·
艾贝泰生物科技有限公司(Applitech Biological Technology Co., Ltd.)作为一家集设计、研发、生产、销售和服务于一体的高新技术企业,致力于为生物制药领域提供专业的生产及分析设备、一次性耗材和整体解决方案。从成立至今,我们始终以客户为中心,将“质量为本,服务为先”作为经营方针,立足于生物工艺的优化、放大和生产,不断完善生物制药领域的产品线,为用户提供全方位生物工艺的专业解决方案,助力用户在生物制药领域不断取得新的突破。

