AAV 在肝脏中的递送方式及其优缺点介绍
2026-03-30 来源:本站 点击次数:70肝脏对全身应用AAV有较高的亲合性,AAV在肝脏中的注射方式分为直接传送和外周传送两种(下表所示),其中尾静脉注射和腹腔注射是目前应用比较广泛的注射方式,操作者也可根据实验目的选择合适的注射方式。
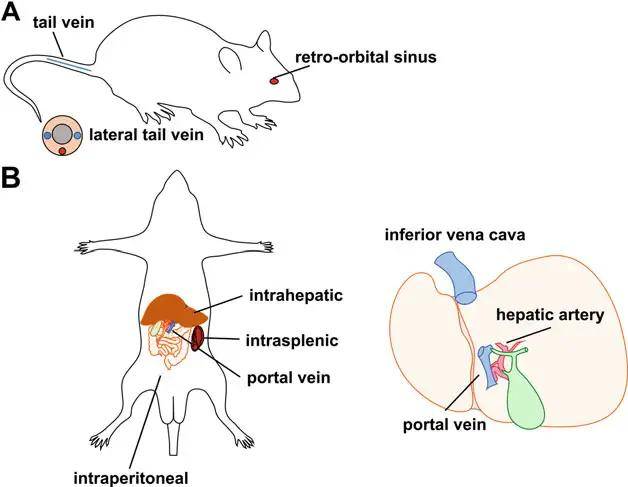 图一:小鼠肝脏中AAV给药途径示意图
图一:小鼠肝脏中AAV给药途径示意图
(A)小鼠侧视图,显示侧尾静脉或眶静脉窦注射路线;(B)小鼠仰卧位图,显示非手术腹膜内和手术肝内、脾内和门静脉输送路径。
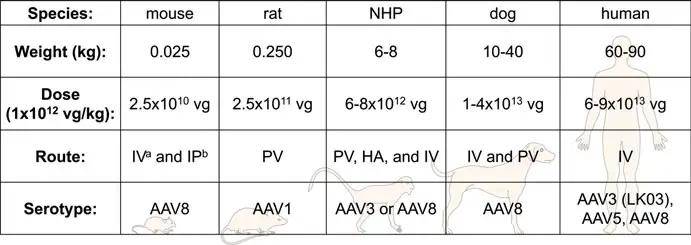 图二:推荐的AAV肝脏注射方式和血清型种间比较
图二:推荐的AAV肝脏注射方式和血清型种间比较
在此,我们介绍一下几种常用的注射方式,肝门静脉注射、肝实质内注射、尾静脉注射以及新生小鼠静脉注射的操作步骤供大家参考。
1. 肝门静脉注射
(1)通过腹腔注射麻醉剂将成年小鼠麻醉,对小鼠腹部局部区域做去毛及消毒处理;
(2)在距剑突软骨下方2-3mm处,做一个2-3cm的中线切口。
(3)暴露门静脉,使用30G针头在1min内均匀缓慢注射0.2 ml病毒悬液。
注:门静脉是一种相对较大的静脉,提起肝前叶一般即可看到门静脉。在手术过程中,用浸泡在生理盐水中的无菌纱布覆盖肠道,保持肠道湿润。
(4)注射后保持针位约10-20秒。取出针后,做好防出血处理;
(5)缝合腹部,将小鼠放置于加热灯下,直至恢复意识。然后将其放回笼子单独饲养,直到伤口完全愈合。
2. 肝内注射
(1)通过腹腔注射麻醉剂将成年小鼠麻醉,对小鼠腹部局部区域做去毛及消毒处理;
(2)在距剑突软骨下方2-3mm,做一个2-3cm的中线切口,以露出肝脏。
(3)用固定在结核菌素注射器上的30G针头将病毒悬液缓慢注入肝实质中。
注:在注射过程中通过手术立体镜监测注射部位,确保无出血或外渗。如果出现上述任何一种情况,需取出针头,轻轻按压止血,然后选择一个新的部位进行注射。
(4)取出针,用无菌纱布轻轻按压止血。
(5)再选择其他部位进行注射。
注:一只成年小鼠一次可选择4 ~ 5个不同的注射位点(40 ~ 50μl/site),总剂量可达200μl。
(6)缝合腹部,将小鼠放置于加热灯下,直至恢复意识。然后将其放回笼子单独饲养,直到伤口完全愈合。
3. 尾静脉注射
(1)将小鼠放在标准限制器中,使注射器能够完全接触到整个尾巴长度。
(2)将一根30G的针头固定在1cc结核菌素注射器上,尽可能远的插入尾部侧面静脉。选择一个远端部位,如果第一次注射失败,可以选择另一个更近端的注射部位。
注:a:小鼠尾巴上较容易接触到的静脉位于尾巴的侧面,且侧静脉非常浅,无需进针很深;小鼠尾部背面的静脉很难常规注射;尾部腹面的血管是动脉,不可注射。
b:注射前用温水轻轻地加热尾巴,可以使血管得到一定程度的舒张,便于注射。
(3)针头到位后,缓慢注射病毒悬液。
注: 如果注射器由于压力增加而难以压下柱塞,此时很可能针头不在静脉中。在这种情况下,应取下针头并选择一个新的位置重新注射。
(4)注射完成后取下针头,轻轻按压止血,然后立即将小鼠放回笼中。
注:使用此方法注射成年小鼠,病毒用量控制在300 - 400μl较佳。
4. 新生小鼠静脉注射
(1)需两个人配合完成,一人固定,一人注射;
(2)注射前将小鼠置于干毛巾上,减少活动及损伤;
(3)一人轻轻固定小鼠,使侧面朝上,暴露眼睛至颈部的颞浅静脉,置于放大镜下;
(4)另一人沿着自头至颈的方向将30G的注射针头插入静脉旁的皮下,慢慢推进静脉(新生鼠皮肤呈现半透明,较易观察);
(5)慢慢注射病毒悬液;(如果注射成功,注射部位远端静脉会呈白色,如果未成功,皮下注射10μl即可看到明显的隆起)
(6)注射完成后,取下针头,轻轻按压静脉,通常2-3分钟会停止出血;
(7)将新生鼠在加热灯下照射后,放回母鼠身边;
(8)如果注射不成功,让小鼠恢复5-10分钟,然后在另一侧尝试第二次注射;
注:使用此方法注射新生小鼠,病毒用量控制在100μl以内较佳。

