分子胶技术的起源与发展、分子胶新药突破及其研发的未来展望
2026-04-03 来源:MCE 中国 点击次数:27Section.01
分子胶技术
起源与发展
沙利度胺:分子胶的偶然起点
分子胶技术发展颇具偶然性,其起源于 20 世纪 50 年代的沙利度胺 —— 该药因致畸性退市后,意外显现多发性骨髓瘤治疗活性。2010 年,日本科学家 Hiroshi Handa 证实,沙利度胺及其衍生物可结合 E3 泛素连接酶底物识别亚基 CRBN,诱导致病蛋白泛素化降解[1],阐明分子胶 “诱导蛋白相互作用” 的核心机制。
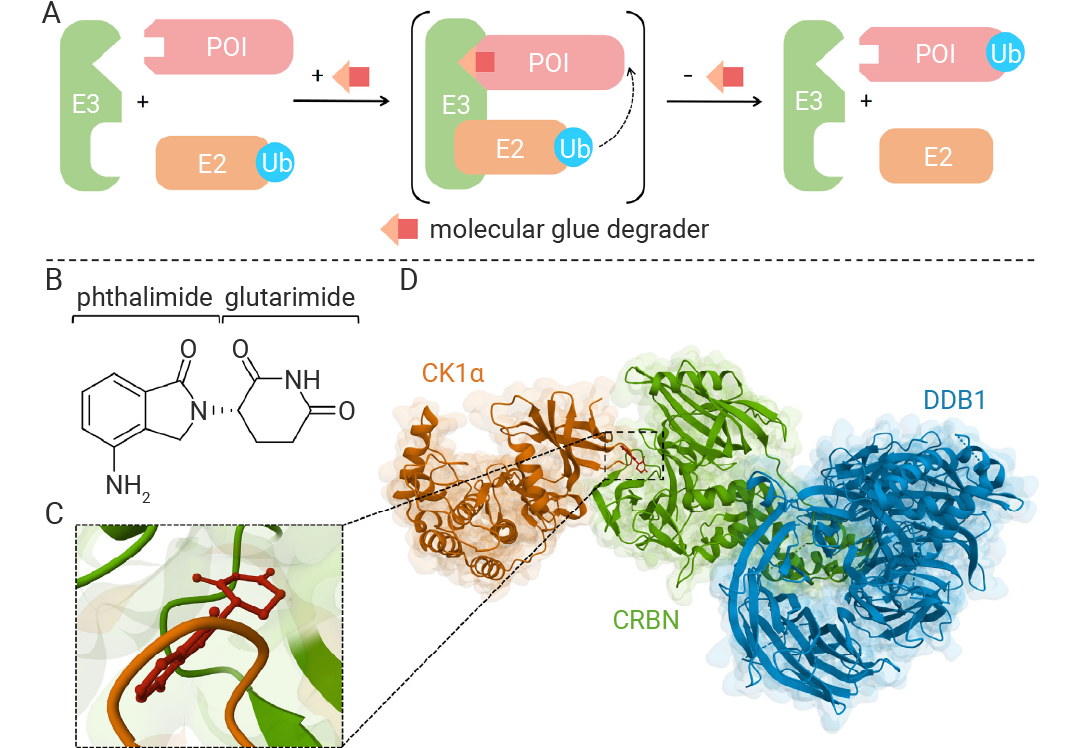
图 1. 分子胶降解剂作用机制[2]。
突破成药局限:分子胶优势
近 5 年,分子胶作为 TPD 核心技术,与传统小分子、PROTAC 优势互补。
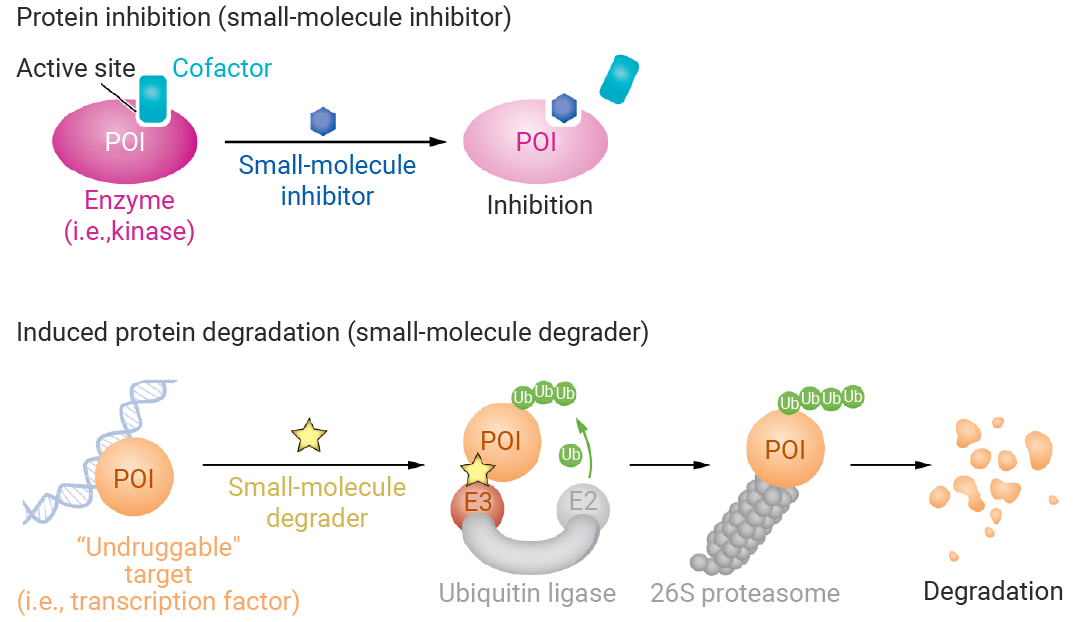
图 2. 传统小分子抑制剂与降解剂的比较[3]。
其具分子量小、膜透性强、口服优的独特优势,机制上无需 E3 连接酶与 POI 高亲和力,诱导三元复合物即可降解靶蛋白,通过靶向 “不可成药” 蛋白极大拓展了药物研发的靶点范围[2]。
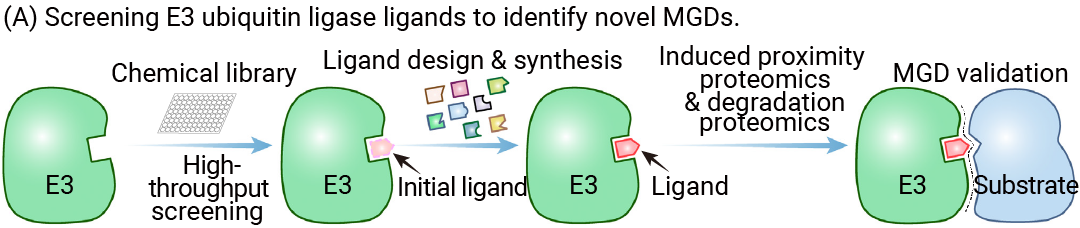
图 3. 通过筛选 E3 泛素连接酶的小分子配体化合物以寻找新型分子胶降解剂[1]
早期分子胶多基于偶然发现,后随着 CRBN 等 E3 泛素连接酶结构解析、作用机制的明确、 AI 辅助设计与化合物库的发展,分子胶研发进入理性设计阶段 ——针对性改造 CRBN 配体骨架、筛选目标蛋白 (POI) 结合片段, 对 CRBN 与新底物蛋白相互作用进行诱导。
分子胶:机遇背后的研发难题
尽管进展显著,分子胶研发仍面临诸多问题和挑战:部分配体结合选择性较差,易脱靶降解导致血液毒性等副作用;诱导非预期蛋白降解影响安全性。同时改造时平衡降解活性与成药性质,避免降解活性提升但药代性质下降的问题。
Section.02
解锁难成药靶点:
分子胶新药突破
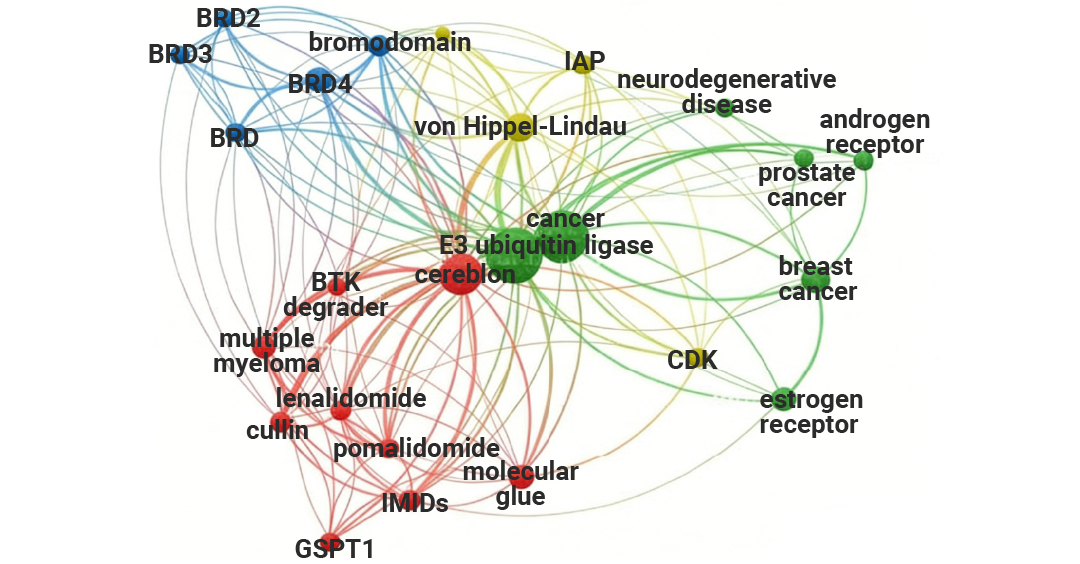
图 4. 分子胶:连接靶向蛋白质降解与临床的粘合剂[4]
GSPT1 分子胶:
GSPT1 是调控细胞周期的关键蛋白,其异常激活与急性髓系白血病等血液瘤密切相关,目前 GSPT1 分子胶研发已进入临床转化关键期,已有多个药物进入临床 I/II 期。
为了减少其他靶点等的脱靶降解,该 CRBN 骨架不再局限于传统邻苯二甲酰亚胺,而引入了苯并三嗪酮、苯并咪唑、肟类等多种新型骨架,以提高靶点选择性和降解活性。同时通过调整苯环、杂环上的取代基,提高与 CRBN 和 GSPT1 的亲和力,增强三元复合物稳定性,提高抗肿瘤增殖活性。
现阶段 GSPT1 分子胶改造策略已聚焦“高选择性+联合疗法”的临床转化与应用。
达歌生物 DEG6498:多类型晚期实体瘤治疗
DEG6498 是 2025 年全球进入临床阶段的 HuR 靶点分子胶降解剂,已进入临床 I 期试验。现阶段临床试验主要针对于结直肠癌、肺癌、肝癌等晚期实体瘤。
该化合物基于 GlueXplorer? 平台开发,对上万余种分子胶化合物库筛选,获得先导化合物。后续改造中重点优化分子的疏水性,引入杂环结构提升口服生物利用度,同时通过构象限制增强靶点选择性。目前患者给药后耐受性良好,未出现剂量限制性毒性,有望填补多种难治性实体瘤的治疗空白。
WIZ 分子胶:血液病口服治疗新策
2024 年由诺华等机构报道了一类靶向 WIZ 转录因子的新型分子胶降解剂。通过表型筛选 CRBN 偏向性化学文库,发现了能够诱导 HbF 表达且不影响红细胞增殖分化的 WIZ 分子胶 dWIZ-1、dWIZ-2[5],可缓解镰状细胞病 (SCD) 和地中海贫血症症状。
该分子胶与CRBN、WIZ 的 ZF7 结构域形成三元复合物,与先前解析的 CRBN 三元复合物特征相似:β- 发夹结构中的甘氨酸 (G876) 可容纳邻苯二甲酰环,结合至三色氨酸口袋。
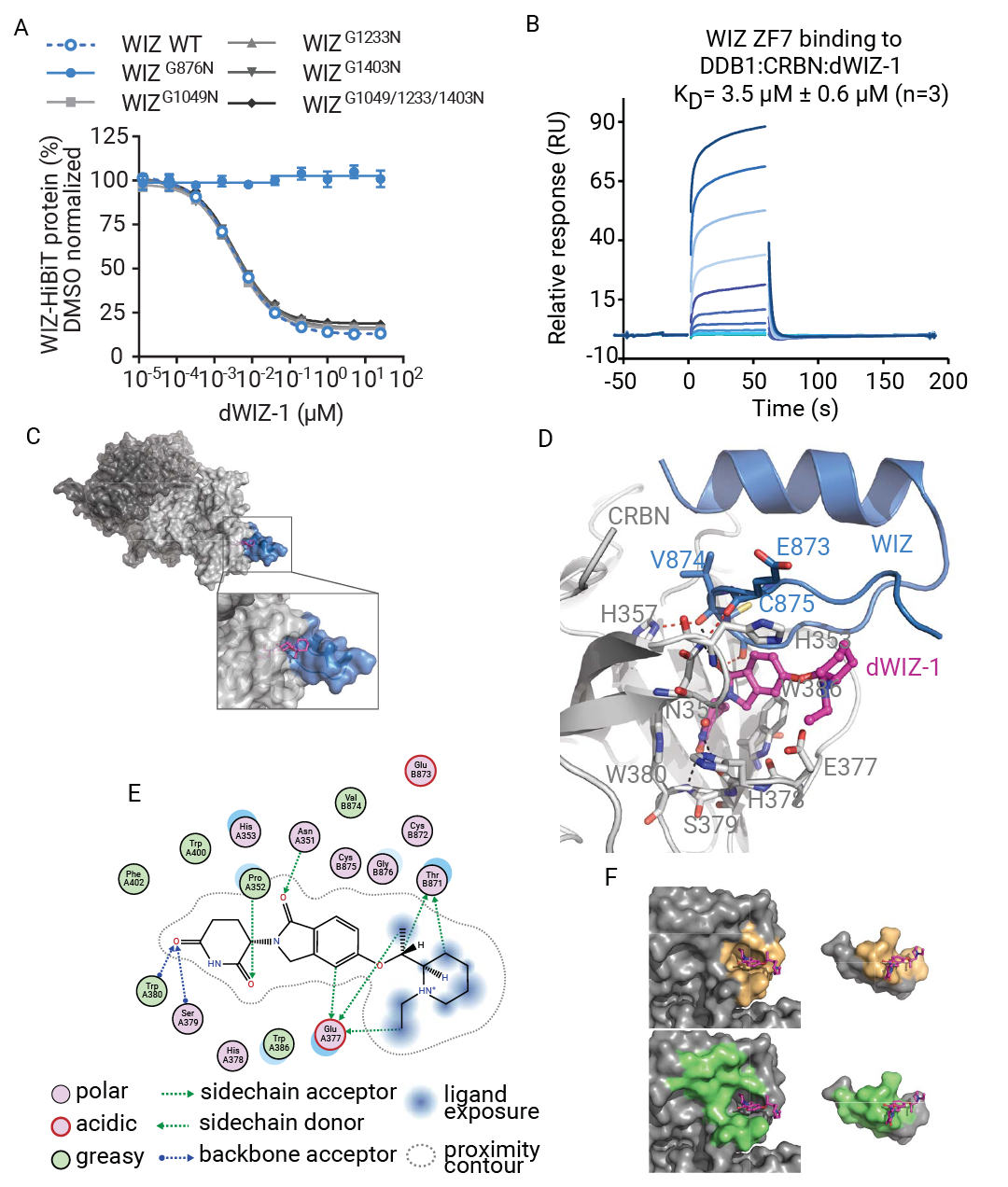
图 5. WIZZF7 与 DDB1:CRBN:dWIZ-1 复合物及 dWIZ-1 配体的作用位点[5]
dWIZ-1 作为分子胶,一方面与 WIZ (ZF7) 的 V874 形成氢键相互作用,另一方面则介导 CRBN 与 WIZ (ZF7) 之间形成额外的氢键相互作用。由于 dWIZ-1 存在手性甲基结构,移除甲基后的 dWIZ-2 可以避免体内代谢异构化、生物利用度低、异构体分离等问题。
通过对 dWIZ-1 初步的构效关系研究,采取环化策略,以 dWIZ-2 的亚甲基作为环化位点,限制构象。同时在上不同位置选择性引入甲基取代基,提升 WIZ 活性并保持与 SALL4 的空间位阻冲突以维持选择性,得到优化后的分子表现出活性提升、高选择性和较好的生物利用度。
目前诺华、BMS 等企业推进相关研发,部分进入临床阶段,为相关血液疾病提供了新型口服治疗策略。
Section.03
分子胶研发:
未来新路径
当前分子胶技术的发展呈现出“多靶点、多适应症、技术融合”的趋势。
在靶点选择上,已从传统的转录因子 (如 IKZF1/3) 延伸至激酶 (CK1α)、RNA 结合蛋白 (HuR)、GTP 酶 (RAS) 等多个类别。适应症从最初的血液瘤逐步转向实体瘤、自身免疫性疾病、神经系统疾病、代谢疾病等多领域。
在分子胶新靶点的发现和 CRBN 新底物开发方面,结合高效筛选方法如 DNA 编码化合物库、亲和筛选质谱 (ASMS) 、高通量筛选 (HTS) 等技术高效发现靶蛋白。同时基于已知化合物库进行深度学习用于预测三元复合物[7],可高效筛选分子胶靶点,大幅缩短分子胶药物的研发周期。
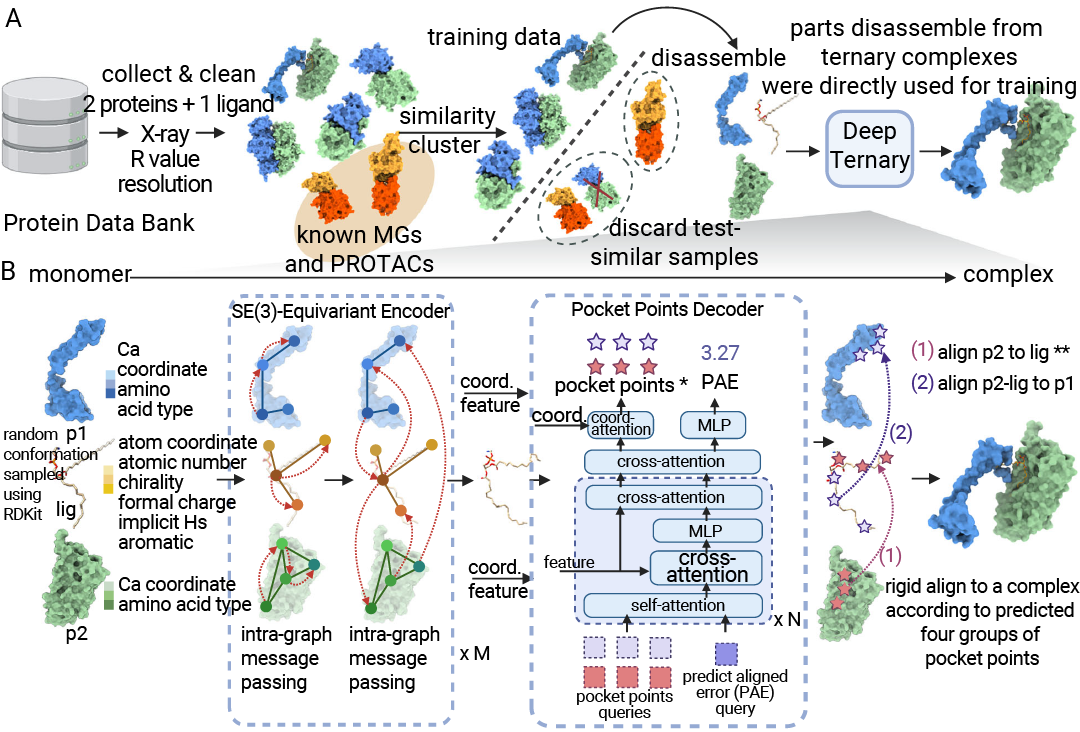
图 6. DeepTernary 是一种深度学习模型,用于预测由 PROTAC 和分子胶诱导形成的三元复合物[7]。
Monte rosa 通过基于结构形状的匹配算法对 CRBN 进行新底物开发,对人类蛋白组中超过数千种 CRBN 兼容的 G-loop 结构进行预测,识别与 CRBN 的新结合模式, 进一步扩大分子胶降解剂的应用范围[6]。
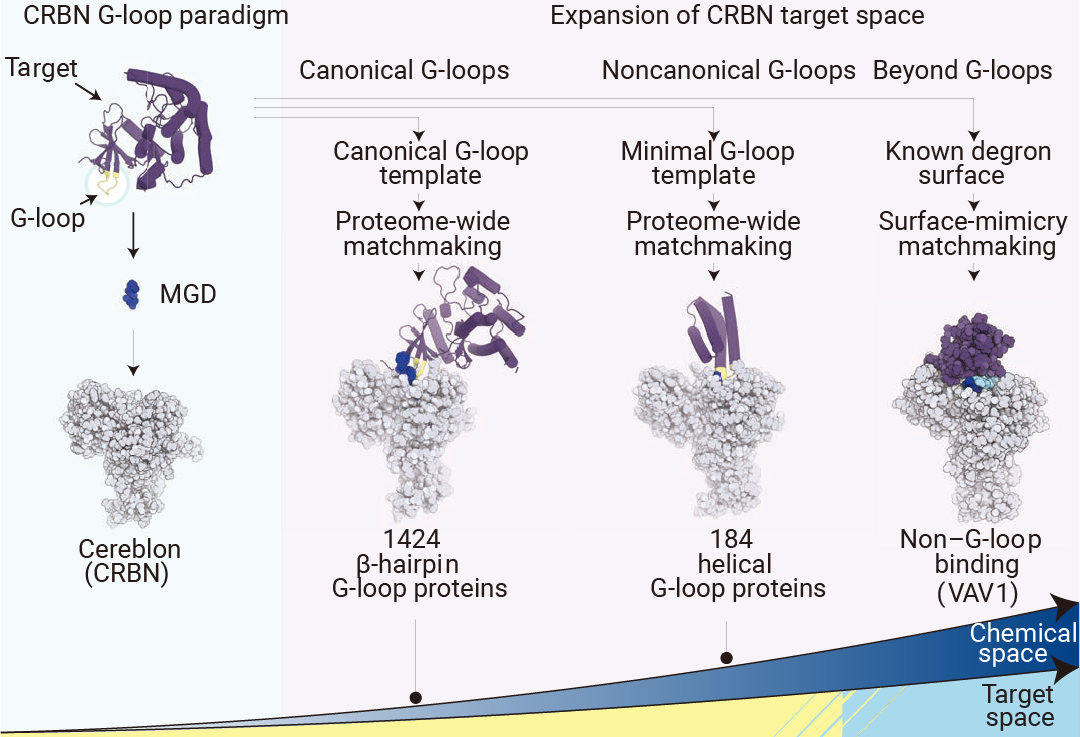
图 7. G-loop 是分子胶募集靶蛋白至 CRBN 的核心识别结构,计算匹配算法预测人体内存在超 1600 种含 CRBN 兼容型 β- 发夹结构或螺旋型 G-loop 基序的蛋白[6]
Section.04
小结
目前分子胶在肿瘤、自身免疫疾病、神经退行性疾病等领域均展现了不俗的治疗潜力。而现阶段关键的分子胶改造大多基于其三元复合物形成,将其拆分为 E3 连接酶结合与靶蛋白 (POI) 结合两大部分,通过构效关系 (SAR) 分析,分别优化相应片段,实现活性、选择性与药代性质的提升。
同时,MCE 可提供分子胶相关化合物库,包括分子胶类似物库、分子胶化合物库、分子胶虚拟库,CRBN 配体库与分子胶 POI 库,和可用于分子胶的模块化合成。

|
MCE 选择了相关的活性分子作为探针分子用于人工智能 (AI) 筛选,再通过分子对接,验证筛选出的分子保持关键的药效团,最终获得 320 个分子胶类似物,这些化合物是研究分子胶的有力工具。 |
|
分子胶化合物库收录了 84 种靶向不同蛋白的分子胶化合物。 |
|
MCE 收集整理 360 个和 CRBN 亲和力较好的片段库,其分子量在 200 - 600 之间。基于库中配体开发的化合物可针对癌症、自身免疫疾病等多种疾病靶点,进一步推动分子胶和 PROTAC 治疗药物研发。 |
|
分子胶目标蛋白结合片段库,MCE 收集整理的分子胶 POI 片段库包含了上百个 POI 配体片段,其分子量在 250 - 360 之间,可广泛应用于分子胶的研发中。 |
|
分子胶虚拟库是依托生成式人工智能技术,整合已知分子胶的结构特征、活性数据及三元复合物 (靶蛋白 - E3 - 分子胶) 的相互作用信息,构建的兼具新颖性、类药性、多样性、可合成性的化合物库。该库适用于基于分子胶的 AI 药物筛选、大型虚拟筛选等。 |
参考文献
[1] Liu Y, et al. Routes to molecular glue degrader discovery. Trends in Biochemical Sciences. 2025;50(2):134-142.
[2] Tan X, et al. Molecular glue-mediated targeted protein degradation: A novel strategy in small-molecule drug development. Science. 2024;27(9):110712
[3] Yoon H, et al. Induced protein degradation for therapeutics: past, present, and future. Journal of Clinical Investigation.2024;134(1):e175265
[4] Sasso J M, et al. Molecular Glues: The Adhesive Connecting Targeted Protein Degradation to the Clinic. Biochemistry. 2023;62(3):601-623.
[5] Ting PY, et al. A molecular glue degrader of the WIZ transcription factor for fetal hemoglobin induction.Science.2024;385(6704):91-99.
[6] Petzold G, et al. Mining the CRBN target space redefines rules for molecular glue-induced neosubstrate recognition. Science. 2025;389(6755):eadt6736.
[7] Xue F, et al. SE(3)-equivariant ternary complex prediction towards target protein degradation. Nat Commun.2025;16(1):5514.



