细胞聚团的主要原因、解决方案及预防方法汇总
2026-04-17 来源:本站 点击次数:69细胞又双叒叕聚团了?看完这篇再也不头疼
养细胞最崩溃的瞬间,莫过于第二天一早去看,原本分散均匀的细胞,居然抱团成了 “小葡萄”,吹也吹不散,计数不准、传代失败,甚至越养状态越差…
其实不用慌!细胞聚团不是 “绝症”。今天就从「为什么聚团」「怎么解决」「如何预防」,一次性讲透,新手也能直接抄作业,再也不用为细胞聚团熬夜发愁~
一、先搞懂:细胞为啥会 “抱团取暖”?
想要解决问题,先找根源!细胞聚团不是凭空出现的,大概率是这6个原因,对照自查,快速定位问题。
1. 细胞本身特性(天生 “爱抱团”)
不是所有细胞都能养成 “单细胞”!有些细胞系 / 原代细胞天生具有聚集性,这是由细胞自身的生物学特性决定的:
- THP-1:细胞低密度时,细胞聚团,呈葡萄状样,细胞密度高,细胞就分散开;
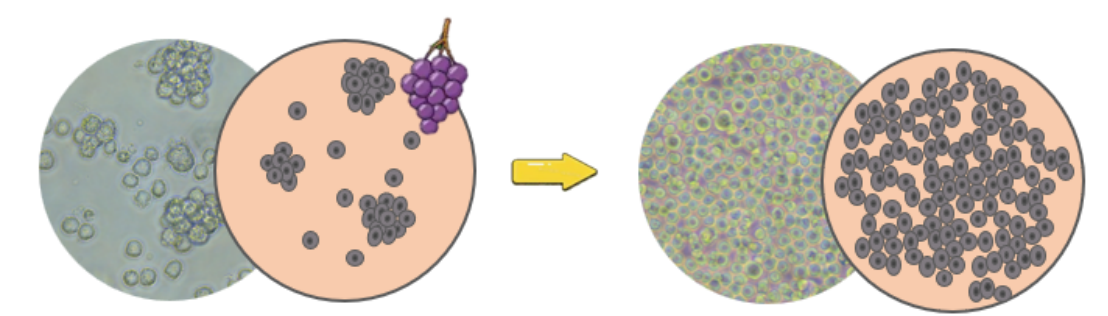
THP-1细胞低密度 THP-1细胞高密度
- Jurkat:Jurkat 为淋巴母细胞样悬浮细胞,本身倾向于成簇生长,而非完全单个分散。
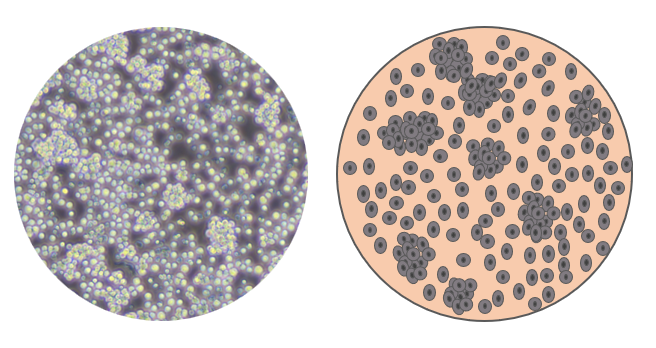
Jurkat细胞
这类细胞的聚团是正常现象,只要形态正常、活力好,无需刻意打散!
2. 吹打不到位(最常见!人为原因)
传代时吹打太轻、次数太少,细胞没有完全吹散,形成肉眼看不见的小团块,后续培养中会慢慢聚集,越抱越大;反之,吹打太剧烈,会损伤细胞,死细胞碎片粘连,也会诱发聚团。
3. 消化 “踩雷” 了(关键诱因)胰酶细胞消化液0.25%货号:CSP046

- 消化不足:细胞没完全脱壁,成片脱落,自然会抱团;使用的胰酶量过少,消化不到位。
- 消化过度:细胞表面受损、死亡,释放出黏性物质,互相粘连成团,甚至会出现 “拉丝”状。
4. 离心条件不对
离心转速太高(超过 500g)、时间太长,会把细胞压成致密的团块,就像被 “压成了饼”,后续再怎么吹打也很难散开。
5. 细胞状态本身不佳
培养基血清含量不足、pH 值偏酸性或偏碱性(培养环境异常),或者细胞本身状态差、大量死亡,会释放出 DNA 等黏性物质,让存活的细胞互相 “粘在一起”,形成聚团。
6. 污染因素:隐形杀手诱发异常聚团 青霉素- 链霉素- 两性霉素B 混合溶液(三抗),货号:CSP007
细菌、真菌、支原体等污染,是容易被忽略的聚团诱因:污染后,微生物会分泌黏附因子,或改变培养基成分,导致细胞异常聚集,通常还会伴随培养基浑浊、细胞大量死亡,这种情况一定要及时处理,避免污染扩散。
二、重点来了!细胞聚团,这样解决最高效
优化操作,从源头预防聚团
- 最省钱、最有效的方法,就是规范操作,避免人为导致的聚团:温和离心:根据细胞类型调整参数,通用100-150g、3-5分钟,离心后立即轻柔重悬,避免细胞挤压粘连。
- 轻柔吹打:用大口径吸头,沿管壁缓慢吹打,避免产生气泡,吹打20次左右至单细胞悬液即可,切勿暴力吹打损伤细胞。
- 及时处理:细胞悬液制备后,尽快进行传代、铺板或检测,减少静置时间;贴壁细胞汇合度达70%-80%及时传代,避免过度生长聚团。
优化培养环境,减少聚团诱因
给细胞一个“舒适的家”,才能减少它们“抱团”的想法:
- 选对培养基,按需加抗聚集剂:悬浮细胞选专用无血清悬浮培养基,贴壁细胞选含适量血清的培养基(血清浓度不宜过高);易聚集细胞可添加抗聚集剂(严格控浓度,防细胞毒性):EDTA(0.05% EDTA溶液, 货号:CSP100)、Pluronic F-68(0.1%-0.2%,适配HEK293、CHO等悬浮细胞)、硫酸葡聚糖(0.1-0.5g/L,低分子量适用于多数细胞,高分子量适配CHO细胞)。
- 控制接种密度:贴壁细胞5×10⁴~1×10⁵细胞/mL,悬浮细胞3–5×10⁵ cells/mL,密度过高易拥挤聚团,过低也会自发聚集。
- 稳定培养条件:培养箱维持37℃±0.5℃、CO₂浓度5%、湿度95%以上;悬浮细胞摇床转速适配(如HEK293细胞120-130rpm),避免转速异常引发聚团。
- 及时处理污染:细菌、真菌、支原体污染会诱导细胞聚集,需定期观察,发现培养基浑浊、细胞异常聚团伴随死亡,及时丢弃污染细胞,严格无菌操作。
物理过滤,快速去除大团块
对于已经形成的较大聚团,用30-70μm孔径的细胞滤网轻柔过滤,可快速去除团块,获得单细胞悬液,注意选择合适孔径,避免损伤细胞。
三、预防大于治疗!这 5 个习惯,避免细胞再聚团
解决完当下的聚团问题,更重要的是做好预防,后续养细胞才能少走弯路,省心又省力!
- 区分细胞特性:提前了解所养细胞的生长特性,天生聚团的细胞不强行打散,常规细胞则保证吹打充分;
- 传代必充分吹打:常规细胞传代时,吹打做到 “轻柔、充分、无气泡”,确保细胞完全分散成单细胞悬液;
- 消化宁短勿长:严格观察细胞消化状态,“刚变圆、将脱壁” 就终止,宁愿消化不足补加一次胰酶,也不盲目延长消化时间;
- 离心宁慢勿久:常规离心条件控制在 100-150g、3-5 分钟,避免高转速、长时间离心;
- 及时过滤 + 换液:细胞状态不佳时,优先过滤去除团块和碎片,同时及时更换新鲜培养基,保证血清含量充足、pH 值正常。
最后总结
细胞聚团并不可怕,关键是先分清原因:天生聚团的细胞 “顺其自然”,操作 / 状态问题导致的聚团,抓住「消化、吹打、过滤、离心」这四个关键步骤,操作温柔、细节到位,就能轻松解决。养细胞多一点耐心、多了解特性,少一点暴力操作,细胞自然会保持好状态,让你的实验少走弯路、事半功倍~

相关文章
更多 >

