单细胞长读长测序揭秘阿尔茨海默病大脑中RNA isoform剪接密码
2026-04-30 来源:怡美通德微信公众号 点击次数:54阿尔茨海默病(AD)是最常见的痴呆类型之一,据统计,全球有超过3000万人患有阿尔茨海默病,其病理特征如大脑中淀粉类斑块和蛋白缠结早已被写入教科书,但一个最根本的问题却始终悬而未决:究竟是什么分子开关,在不知不觉中推倒了疾病的多米诺骨牌。传统单细胞短读长RNA测序让我们看清了大脑中不同细胞类型的基因表达谱,却因长度限制难以解析全长转录本异构体。事实上,人类神经系统的转录本多样性远超想象,有的基因甚至可以通过可变剪接产生成百上千种转录本,而异常剪接已被发现与AD等神经疾病密切相关。此外,逆转录酶介导的体细胞基因重组(RT-SGR)可产生多种新RNA,甚至携带致病突变。
近期Sanford Burnham Prebys医学研究所神经疾病中心研究团队发表了题为“RNA isoform diversity, splicing variants and switching in single cells of the Alzheimer’s disease brain”的文章,研究人员使用PacBio Kinnex长读长测序,通过16x cDNA串联显著提升了测序通量,结合10x Genomics单细胞转录组技术,对AD及对照人脑前额叶皮层进行了细胞类型分辨率的转录异构体分析,结果表明那些短读长测序难以检测的“暗物质”RNA,正是理解AD细胞类型特异性致病机制的关键拼图。
1
阿尔茨海默病大脑中细胞类型特异性基因表达
在这项研究中,研究人员对8例阿尔茨海默(AD)患者和7例非病变(ND)样本的前额叶皮层进行单细胞核转录组测序。实验使用10x Genomics单细胞3′ Kit进行cDNA生成,并使用扩增后的cDNA分别进行短读长文库和PacBio Kinnex长读长文库构建。质控后获得超过70,000个细胞核,注释出兴奋/抑制性神经元、少突胶质细胞、星形胶质细胞、小胶质细胞等主要细胞类型,并进行了差异基因表达分析,显示在星形胶质细胞和少突胶质细胞中最多。GO分析显示出细胞类型特异性富集,包括兴奋性神经元富集突触组织与谷氨酸信号,小胶质细胞富集神经炎症与II型干扰素反应,星形胶质细胞富集胶质增生,少突胶质细胞富集淀粉类蛋白代谢等,与既往snRNA-seq研究一致,验证了样本与测序数据的可靠性。
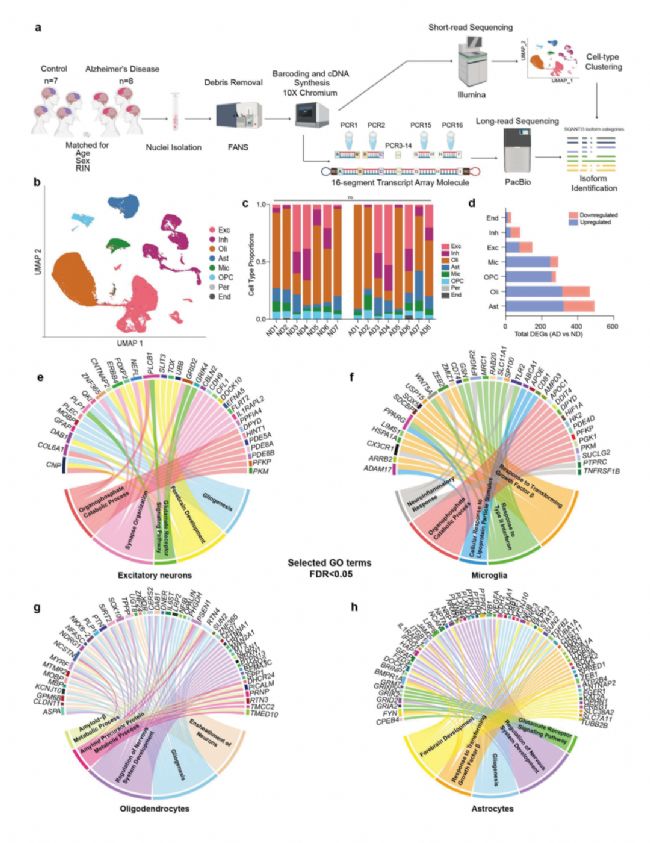 图1 单细胞核转录组短读长测序和Kinnex长读长测序实验设计流程及细胞类型特异性分析
图1 单细胞核转录组短读长测序和Kinnex长读长测序实验设计流程及细胞类型特异性分析
2
AD致病和风险基因中异构体特征解析
研究者通过单细胞核长读长测序平均每样本获得2.1 M HiFi reads(拆分后得到32.5 M reads),共检测到858,171个异构体,包含大量低丰度异构体可能源于细胞类型特异性剪接或逆转录酶介导的体细胞基因重组(RT‑SGR),并检测到外显子内连接(IEJs)的APP和TARDBP等异构体。
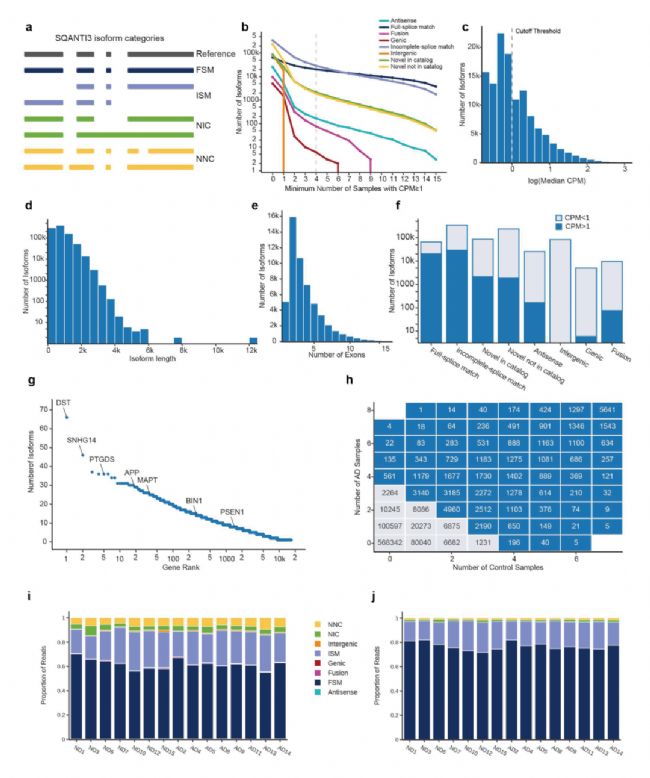 图2 Kinnex长读长测序解析转录本异构体
图2 Kinnex长读长测序解析转录本异构体
研究分析了AD相关致病和风险基因,其中检测到BIN1的5个全长剪接匹配(FSM)异构体和1个含新外显子(经RT‑PCR验证)及5′端截短的新异构体,BIN1不同异构体表达在AD和ND样本之间存在显著差异,而短读长测序没有检测到其样本间的显著差异。此外,还检测出APOE的1个FSM和1个缺失多个外显子的低表达新异构体(经RT‑PCR验证),表达分析显示APOE在AD小胶质细胞中表达升高,而在星形胶质细胞中降低。
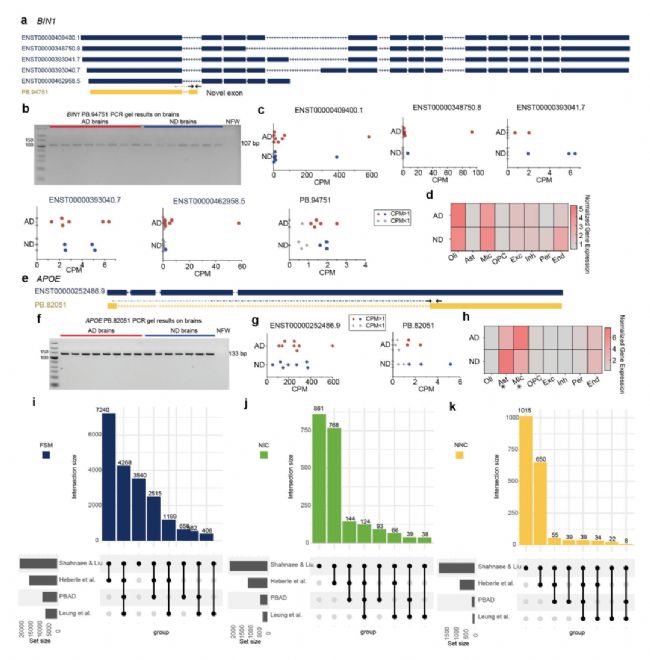 图3 Kinnex长读长测序鉴定AD相关基因新转录本
图3 Kinnex长读长测序鉴定AD相关基因新转录本
3
AD大脑中差异表达转录本切换及细胞类型特异性异构体表达模式
研究鉴定了AD中多个差异表达转录本(DETs)和异构体切换事件。AD中显著上调的DETs包括TNFRSF25的5’端截短及内含子保留的FSM和CHI3L1的内含子保留的NIC(具有已知剪接位点的新型连接)异构体,前者预测为非编码但可能参与调控功能,后者则可能为驱动CHI3L1基因表达水平升高的主要异构体,而CHI3L1的其他转录本在表达水平上没有表现出明显差异。下调的DETs包括HMGN1的FSM和BASP1使用可变5′UTR的NNC(具有至少一个未注释的剪接位点类型)异构体,新5′UTR可能会影响其稳定性和翻译效率。
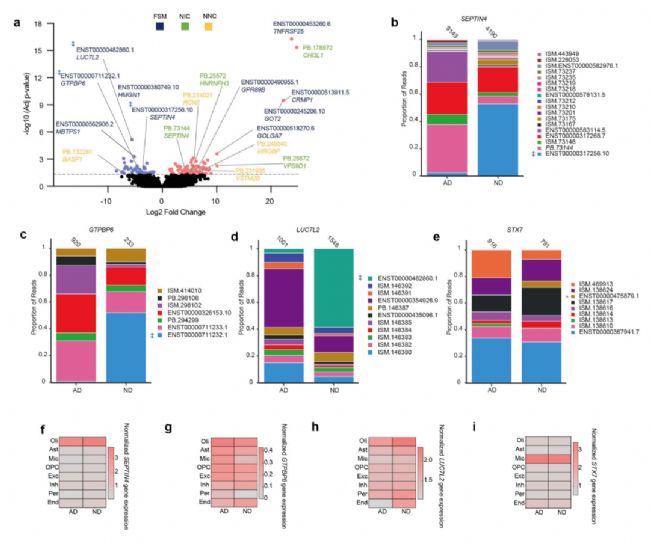 图4 疾病相关新异构体表达及AD中转录本切换
图4 疾病相关新异构体表达及AD中转录本切换
研究发现SEPTIN4在AD中存在多个DETs,包括一个下调且切换表达的FSM和一个上调的NIC异构体,且二者均通过RT‑PCR验证。结合细胞类型分析显示AD相关基因表现出细胞类型特异性表达,例如APP‑695在AD兴奋性神经元中富集,而APP‑751在ND兴奋性神经元中富集;APOE新异构体(PB.82051)在ND少突胶质细胞中缺失,而CLU异构体(PB.149064)在AD少突胶质细胞中缺失等,揭示了不同细胞类型和AD 状态之间不同的转录本多样性。
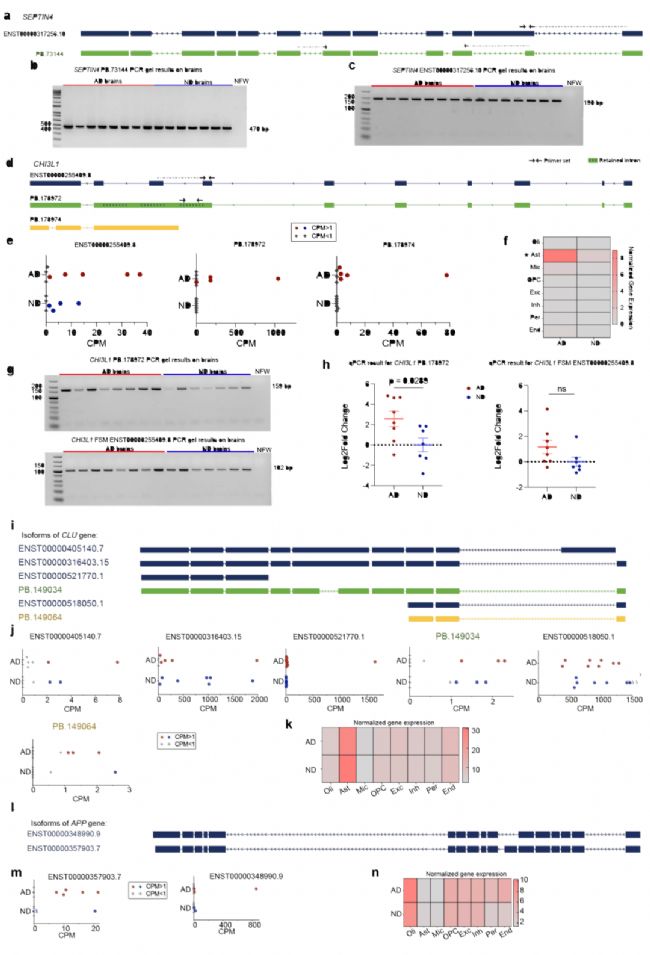 图5 AD相关基因转录本及异构体差异表达模式
图5 AD相关基因转录本及异构体差异表达模式
这项研究向我们揭示了一个不容忽视的事实:当我们只看基因表达水平的变化时,很可能错过了那些隐藏在剪接版本中的关键信息。同一个基因,通过不同的剪接方式,可以在不同细胞类型、不同疾病状态下,甚至在同一细胞内上演着截然不同的“异构体变奏曲”。未来,看清这些剪接事件及其与疾病相关的转录本转换模式,或许才是找到治疗靶点的关键。PacBio Kinnex技术的突破,为单细胞转录组研究打开了一扇通往“全长异构体时代”的大门,揭秘生命更深层次的复杂性。
Contact
北京怡美通德科技发展有限公司
是10x Genomics和PacBio的官方授权代理商
进一步了解产品详情
欢迎通过如下方式联系我们
电话:010-84409661
官网:www.emtd.com.cn
Email: marketing@emtd.com.cn
微信公众号/ 微信视频号:怡美通德EMTD

参考文献
-
Shahnaee, A., Liu, C.S., Ngo, T. et al. RNA isoform diversity, splicing variants and switching in single cells of the Alzheimer’s disease brain. Commun Biol (2026). https://doi.org/10.1038/s42003-026-09759-9.

