使用EVIDENT共聚焦显微镜对血管化肿瘤细胞球芯片进行观察研究
2025-03-07 来源:本站 点击次数:1717
研究显示,肿瘤可通过诱导血管生长来支持其旺盛的活性。这些血管作为肿瘤的生命线,在肿瘤微环境(TME)中对于其活性起到了相当重要的作用。到目前为止,对肿瘤在生化和生物力学刺激的反应,大多是在静态条件下进行评估,并没有考虑到血流对肿瘤的影响。本篇文章,我们提供了一个肿瘤-芯片平台,通过流经可灌注血管网络的介质流来评估肿瘤微环境,并测量血流中的给药效应。
肿瘤细胞球在微流控设备中的3D观察结果
本研究中,我们在微流控设备中将人脐静脉内皮细胞(HUVEC)与含有人乳腺癌细胞(MCF-7)的肿瘤细胞球进行共同培养,以重现包括血管网络在内的肿瘤微环境。为了确认微流控设备中血管网络的可灌注性,我们使用FLUOVIEW共聚焦显微镜观察荧光微球(绿色)是否能够连续通过血管网络和球细胞。因细胞球较厚,我们很难获得培养样本的三维图像。通常需要较高的激发光强度才能产生足以能够检测到的荧光信号强度。但是,较高的激发光强度也会增大光毒性,从而导致细胞损伤。为了解决这一问题,我们使用集成了TruSpectral全真光谱检测技术和高灵敏度GaAsP探测器的FLUOVIEW共聚焦显微镜,捕获微弱的荧光信号,同时尽量降低激光器的功率。
使用共振扫描振镜进行血流快速成像
我们还利用荧光微球(绿色,直径3.1 μm)检查了肿瘤细胞球血管网络内的血流。在观察快速血流时,常规扫描振镜的扫描速度可能不够。本实验中,我们使用配有高速共振扫描振镜的FLUOVIEW共聚焦显微镜采集图像。结果表明,在将荧光微球注入到微流控设备的通道3时,微球流经肿瘤细胞球的中空腔并到达通道1,说明我们所设计的血管网络可接受灌注。确认人工肿瘤细胞球模型用于研究血流对TME影响的有效性后,我们在随后的实验中明确了,在包括血管网络的TME中,药物的疗效因血管内是否存在血流而异。我们希望这款三维模型能够在今后被用作经血管给药模型,以协助药物的开发。

这项研究的新颖之处在于,在肿瘤细胞球内,人工构建的可灌注血管网络。可视化血管网络如何连接细胞球和微流控通道非常重要。此外,可以同时观察血管管腔和流经血管结构的血流,对于证明其可灌注性来说也很关键。FLUOVIEW共聚焦显微镜上安装的高速共振扫描振镜,能够对血管网络(RFP标记)和微球(绿色)动态流进行成像。
肿瘤学研究和药物研发对显微成像的要求非常高,需要有高速的三维成像能力,在体的研究还需要低光度性的深层成像,Evident全新激光扫描共聚焦显微镜和多光子显微镜FV4000(MPE)配备全新的高灵敏硅基半导体检测器,具有更高的灵敏度,降低了光毒性,同时高分辨率的共振扫描振镜可提供视频级采集速率,帮助获取肿瘤微环境或药物代谢的动态变化过程。

更多使用Evident共聚焦和多光子显微技术推进肿瘤学研究和药物研发的应用示例,欢迎识别以下二维码,下载干货满满的电子书了解详情!
参考文献
Nashimoto Y, Okada R, Hanada S, Arima Y, Nishiyama K, Miura T, Yokokawa R.Biomaterials.
2020, Jan;229:119547“. Vascularized cancer on a chip: The effect of perfusion on growth
and drug delivery of tumor spheroid.” DOI: 10.1016/j.biomaterials.2019.119547
更多精彩内容,敬请关注我们的视频号:


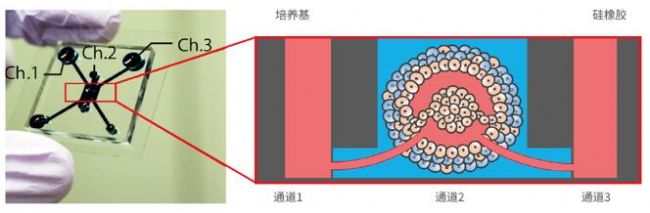
图1.微流控设备和肿瘤模型。(左)微流控设备图;(右)具有可灌注血管网络的肿瘤模型。
肿瘤细胞球在微流控设备中的3D观察结果
本研究中,我们在微流控设备中将人脐静脉内皮细胞(HUVEC)与含有人乳腺癌细胞(MCF-7)的肿瘤细胞球进行共同培养,以重现包括血管网络在内的肿瘤微环境。为了确认微流控设备中血管网络的可灌注性,我们使用FLUOVIEW共聚焦显微镜观察荧光微球(绿色)是否能够连续通过血管网络和球细胞。因细胞球较厚,我们很难获得培养样本的三维图像。通常需要较高的激发光强度才能产生足以能够检测到的荧光信号强度。但是,较高的激发光强度也会增大光毒性,从而导致细胞损伤。为了解决这一问题,我们使用集成了TruSpectral全真光谱检测技术和高灵敏度GaAsP探测器的FLUOVIEW共聚焦显微镜,捕获微弱的荧光信号,同时尽量降低激光器的功率。

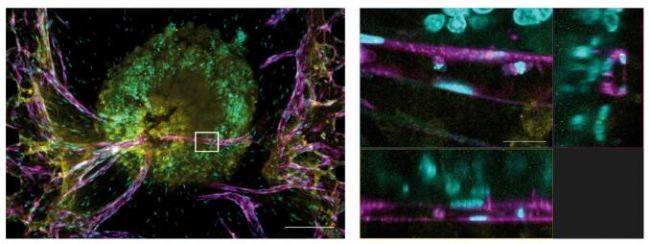
图2.肿瘤细胞球及其血管网络。细胞核:青色(405 nm,Hoechst 33342),RFP-HUVEC:紫红色(561 nm,RFP),E-钙粘蛋白:黄色(640 nm,Alexa Fluor 633)。
(a) 肿瘤细胞球的投影图。比例尺:200 μm,物镜:UPLSAPO10X2。(b)(a)中白色框架的3平面图像(x-y、x-z、y-z)。比例尺:20 μm,物镜:UPLSAPO40X2。
(a) 肿瘤细胞球的投影图。比例尺:200 μm,物镜:UPLSAPO10X2。(b)(a)中白色框架的3平面图像(x-y、x-z、y-z)。比例尺:20 μm,物镜:UPLSAPO40X2。
使用共振扫描振镜进行血流快速成像
我们还利用荧光微球(绿色,直径3.1 μm)检查了肿瘤细胞球血管网络内的血流。在观察快速血流时,常规扫描振镜的扫描速度可能不够。本实验中,我们使用配有高速共振扫描振镜的FLUOVIEW共聚焦显微镜采集图像。结果表明,在将荧光微球注入到微流控设备的通道3时,微球流经肿瘤细胞球的中空腔并到达通道1,说明我们所设计的血管网络可接受灌注。确认人工肿瘤细胞球模型用于研究血流对TME影响的有效性后,我们在随后的实验中明确了,在包括血管网络的TME中,药物的疗效因血管内是否存在血流而异。我们希望这款三维模型能够在今后被用作经血管给药模型,以协助药物的开发。

视频:微流控设备上人造血管和肿瘤细胞球内荧光微球的流动。成像条件:65 毫秒/帧。比例尺:100 μm。
这项研究的新颖之处在于,在肿瘤细胞球内,人工构建的可灌注血管网络。可视化血管网络如何连接细胞球和微流控通道非常重要。此外,可以同时观察血管管腔和流经血管结构的血流,对于证明其可灌注性来说也很关键。FLUOVIEW共聚焦显微镜上安装的高速共振扫描振镜,能够对血管网络(RFP标记)和微球(绿色)动态流进行成像。
——Ryuji Yokokawa博士
日本京都大学微工程系
日本京都大学微工程系
肿瘤学研究和药物研发对显微成像的要求非常高,需要有高速的三维成像能力,在体的研究还需要低光度性的深层成像,Evident全新激光扫描共聚焦显微镜和多光子显微镜FV4000(MPE)配备全新的高灵敏硅基半导体检测器,具有更高的灵敏度,降低了光毒性,同时高分辨率的共振扫描振镜可提供视频级采集速率,帮助获取肿瘤微环境或药物代谢的动态变化过程。

左图:FV4000激光扫描共聚焦显微镜;右图:FV4000MPE多光子显微镜
更多使用Evident共聚焦和多光子显微技术推进肿瘤学研究和药物研发的应用示例,欢迎识别以下二维码,下载干货满满的电子书了解详情!

参考文献
Nashimoto Y, Okada R, Hanada S, Arima Y, Nishiyama K, Miura T, Yokokawa R.Biomaterials.
2020, Jan;229:119547“. Vascularized cancer on a chip: The effect of perfusion on growth
and drug delivery of tumor spheroid.” DOI: 10.1016/j.biomaterials.2019.119547
更多精彩内容,敬请关注我们的视频号:

相关文章
更多 >

