哮喘相关动物模型的介绍及其在探究哮喘新疗法中的应用
2025-05-06 来源:本站 点击次数:131支气管哮喘(简称哮喘)是一种由多种细胞(如嗜酸性粒细胞、肥大细胞、T淋巴细胞等)及细胞组分参与的慢性气道炎症性疾病,具有异质性和气道高反应性特征。其核心病理表现为气道炎症、气道重塑及可变性气流受限,临床以反复发作的喘息、胸闷、咳嗽等症状为主,常在夜间或凌晨加重,多数患者可经治疗缓解[1]。
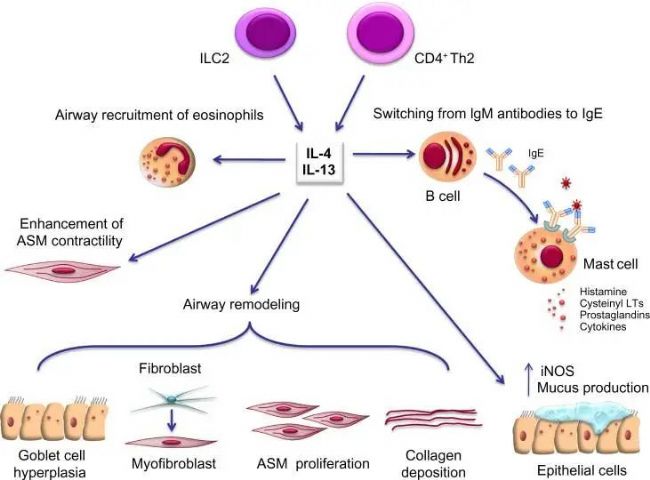
图1. IL-4和IL-13在哮喘病生理学中的多重作用[2]
哮喘核心发病机制涉及嗜酸性粒细胞异常活化释放阳离子蛋白、肥大细胞脱颗粒,以及气道上皮细胞、T淋巴细胞亚群等免疫活性细胞介导的级联反应,形成以IL-4/IL-5/IL-13为主导的Th2型免疫应答,最终引发粘液高分泌、气道重塑及IgE合成等典型病理改变。遗传易感性(超过100个易感基因位点)、表观遗传调控(DNA甲基化修饰)与环境暴露(过敏原/污染物/呼吸道感染)构成哮喘的"三重互作网络"。特别值得关注的是,气道重塑引发的不可逆性气流阻塞已成为当前临床治疗难点——现有药物对气道基底膜增厚、平滑肌增生等结构性改变的干预效果有限,这驱动着针对TSLP、IL-33等新型生物靶点的药物研发[3]。
南模生物哮喘相关动物模型
优质的哮喘疾病模型是药物评价的良好工具,常用的造模方式是采用屋尘螨提取物(HDM)、卵清蛋白(OVA)等构建小鼠哮喘模型。南模生物炎症/自身免疫疾病评价平台自主研发了多种哮喘小鼠模型,在不同品系(C57BL/6,hIL4/hIL4R mice,BALB/c)中进行了验证,可用于哮喘治疗药物的药效评价。部分数据如下:
/ 基于hIL4/hIL4R人源化小鼠的哮喘模型及Dupilumab单抗的药效研究 /
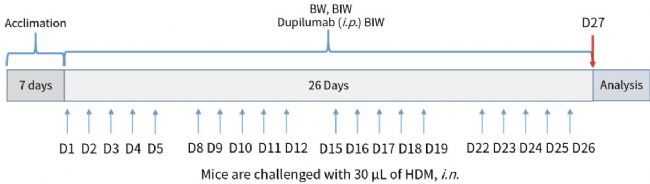
图1. 基于hIL4/hIL4R小鼠构建HDM诱导的哮喘模型。
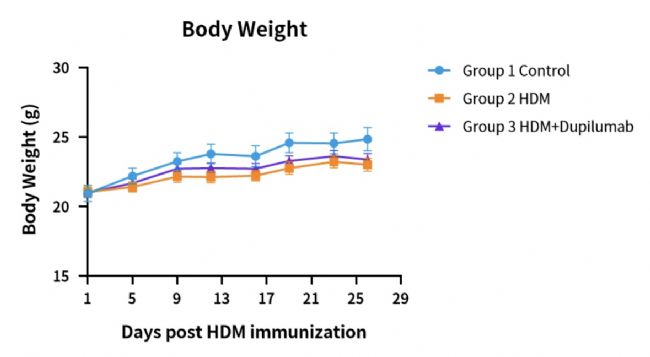
图2. HDM诱导的hIL4/hIL4R小鼠哮喘模型的体重。
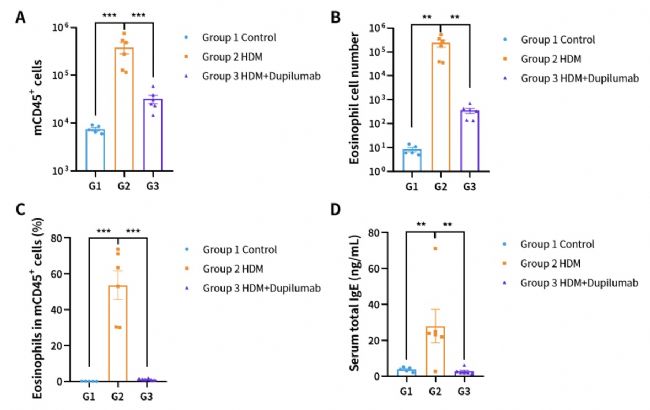
图3. HDM诱导的hIL4/hIL4R小鼠哮喘模型肺泡灌洗液(BALF)中免疫细胞的数量。(A)BALF中的CD45+细胞的数量;(B)BALF中的嗜酸性粒细胞;(C)嗜酸性粒细胞占CD45+细胞的比例;(D)血清总IgE浓度。
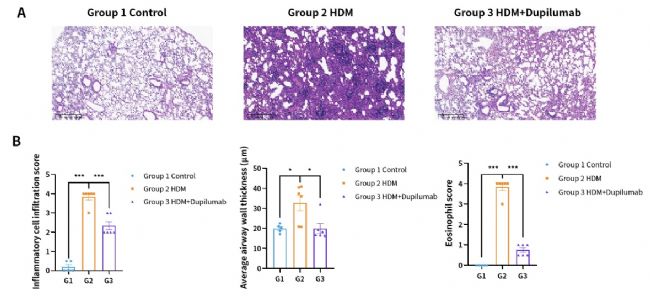
图4. HDM诱导的hIL4/hIL4R小鼠哮喘模型。(A)H&E染色代表图。(B)病理评分结果。
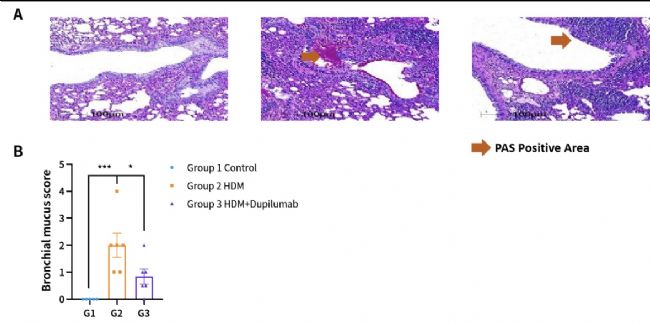
图5. HDM诱导的hIL4/hIL4R小鼠哮喘模型。(A)PAS染色代表图。(B)支气管黏液评分。
/ OVA诱导的BALB/c小鼠哮喘模型及Dexamethasone药效研究/
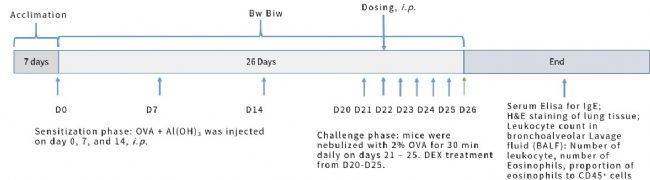
图6. OVA诱导的BALB/c小鼠哮喘模型。
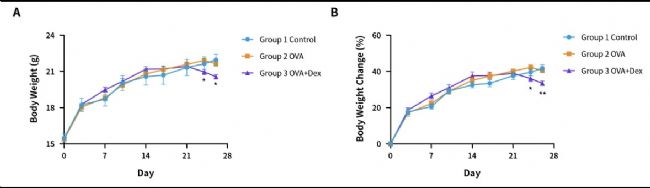
图7. OVA诱导的BALB/c小鼠哮喘模型。(A)体重;(B)体重变化。
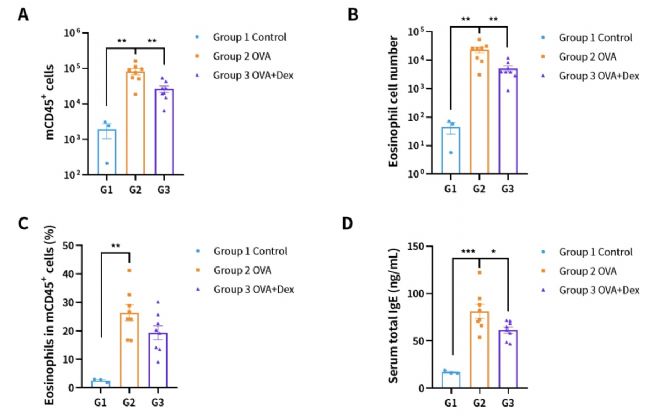
图8. OVA诱导的BALB/c小鼠哮喘模型肺泡灌洗液(BALF)中免疫细胞的数量。(A)BALF中的CD45+细胞的数量;(B)BALF中的嗜酸性粒细胞;(C)嗜酸性粒细胞占CD45+细胞的比例;(D)血清总IgE浓度。
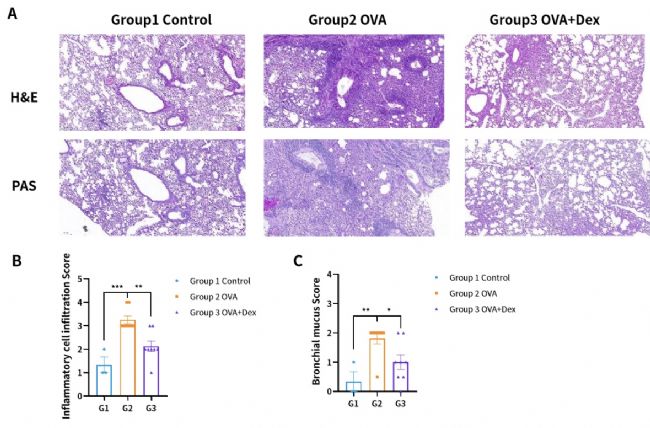
图9. OVA诱导的BALB/c小鼠哮喘模型。(A)肺部H&E及PAS染色;(B)炎症细胞浸润评分;(C)支气管黏液评分。
如您有相关需求,欢迎拨打400-728-0660或者关注微信公众号点击在线咨询,我们的专业团队将竭诚为您服务!
Reference:
[1] Martinez FJ, Collard HR, Pardo A, et al. Idiopathic pulmonary fibrosis. Nat Rev Dis Primers. 2017;3:17074. Published 2017 Oct 20. doi:10.1038/nrdp.2017.74
[2] Vatrella A, Fabozzi I, Calabrese C, Maselli R, Pelaia G. Dupilumab: a novel treatment for asthma. J Asthma Allergy. 2014;7:123-130. Published 2014 Sep 4. doi:10.2147/JAA.S52387
[3] Durrant, D.M.and D.W.Metzger,Emerging roles of T helper subsets in the pathogenesis of asthma. Immunol Invest, 2010.39(4-5):p.526-49
关于我们
上海南方模式生物科技股份有限公司(Shanghai Model Organisms Center, Inc.,简称"南模生物"),成立于2000年9月,是一家上交所科创板上市高科技生物公司(股票代码:688265),始终以编辑基因、解码生命为己任,专注于模式生物领域,打造了以基因修饰动物模型研发为核心,涵盖多物种模型构建、饲养繁育、表型分析、药物临床前评价等多个技术平台,致力于为全球高校、科研院所、制药企业等客户提供全方位、一体化的基因修饰动物模型产品解决方案。

