活细胞成像揭秘免疫抑制:创伤后感染的新突破
2025-05-08 来源:本站 点击次数:56
一、研究思路
核心目标
探究创伤释放DANGER信号(如线粒体DNA(mtDNA)、线粒体形式肽(mtFP))如何通过激活G蛋白受体激酶2 (GRK2) 抑制中性粒细胞功能,导致创伤后感染风险增加。
技术路线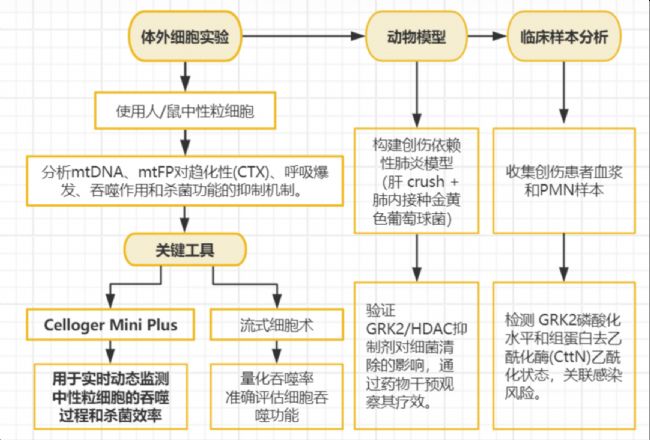
二、核心结论
1. mtDNA与mtFP的作用机制
- mtDNA:
- 通过 TLR9 非经典途径激活GRK2,抑制 F-actin聚合和CTTN乙酰化,导致中性粒细胞 趋化性丧失和吞噬功能下降。
- GRK2抑制剂(如Paroxetine) 或 HDAC抑制剂(Valproate) 可恢复功能。
- mtFP:
- 通过 GPCR(如FPR1) 经典途径激活GRK2,诱导GPCR内化,抑制趋化性。
2. GRK2的双重调控路径
- 经典路径:mtFP → GPCR内化 → GRK2磷酸化 → β-arrestin介导信号终止。
- 非经典路径:mtDNA → TLR9 → GRK2磷酸化 → HDAC6激活 → CttN去乙酰化 → 抑制F-actin聚合。
3. 临床相关性
- 创伤患者血浆 mtDNA水平和PMN pGRK2表达 显著升高,且与感染风险正相关。
三、研究意义
1. 机制创新
- 揭示 DANGER信号通过GRK2双通路(GPCR依赖性和TLR9非依赖性) 抑制中性粒细胞功能的分子机制。
- 提出 GRK2/HDAC双重抑制是恢复免疫功能的潜在策略。
2. 临床转化
- Paroxetine(GRK2抑制剂) 和 Valproate(HDAC抑制剂) 的联合应用可有效降低创伤后感染风险,为开发新型抗感染药物提供依据。
四、Celloger Mini Plus 的详细应用
实验设计
1. 吞噬功能检测
- 样本:人/鼠中性粒细胞与 pH-SA(pHrodo Green S. aureus Bioparticles)共孵育。
- 处理组:
- mtDNA/mtFP预处理组;
- GRK2抑制剂(Paroxetine)或HDAC抑制剂(Valproate)干预组。
- 对照组:无处理组或使用 CQ(氯喹) 阻断内吞。
2. 成像参数
- 仪器:Celloger Mini Plus + EVOS Cell Imaging System。
- 时间点:动态监测 15分钟 内的吞噬过程。
- 分辨率:明场成像(观察细胞形态)+ 荧光成像(pHrodo Green信号)。
3. 数据分析
- 杀菌效率:
- 使用 Celloger Mini Plus 检测活菌比例(图1A);
- 补充平板计数法验证结果一致性。
- 吞噬率:通过流式细胞术量化荧光阳性细胞比例(图1B/C)。
关键结果
- mtDNA抑制吞噬:
- 中性粒细胞对S. aureus的吞噬率显著下降;
- Valproate或Paroxetine预处理 可恢复吞噬功能。
- 动态成像证据:
- mtDNA处理组的中性粒细胞无法有效摄入荧光标记的细菌(图1C,红色箭头示未吞噬颗粒)。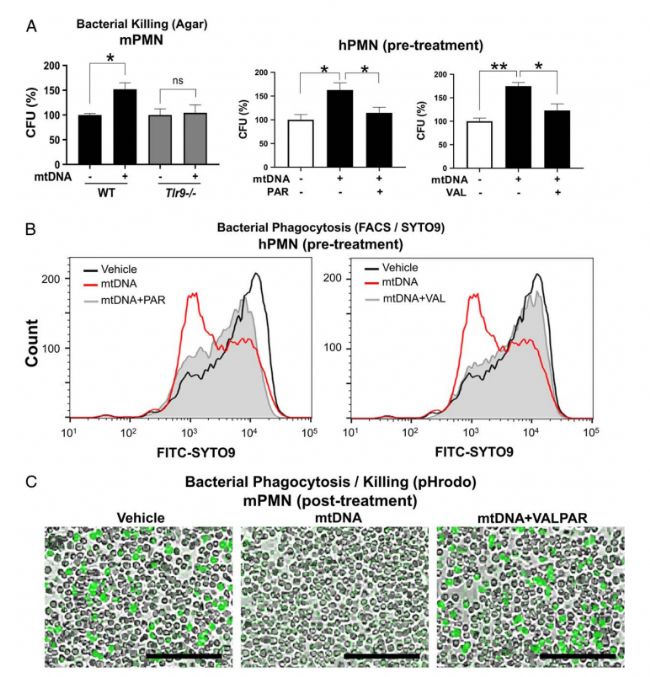
图1.VAL(丙戊酸)和 PAR(帕罗西汀)能够挽救 DAMP(损伤相关分子模式)抑制的 PMN(中性粒细胞)吞噬和杀伤能力。
五、总结
本研究通过 Celloger Mini Plus 实时动态监测中性粒细胞的吞噬行为,揭示了创伤后DANGER信号通过GRK2/HDAC通路抑制免疫功能的分子机制,并为临床防治创伤后感染提供了 双靶点治疗策略(Paroxetine + Valproate)。该技术的应用为研究免疫细胞动态过程和疾病机制提供了重要工具。
为什么选择 Celloger Mini Plus?
核心目标
探究创伤释放DANGER信号(如线粒体DNA(mtDNA)、线粒体形式肽(mtFP))如何通过激活G蛋白受体激酶2 (GRK2) 抑制中性粒细胞功能,导致创伤后感染风险增加。
技术路线

二、核心结论
1. mtDNA与mtFP的作用机制
- mtDNA:
- 通过 TLR9 非经典途径激活GRK2,抑制 F-actin聚合和CTTN乙酰化,导致中性粒细胞 趋化性丧失和吞噬功能下降。
- GRK2抑制剂(如Paroxetine) 或 HDAC抑制剂(Valproate) 可恢复功能。
- mtFP:
- 通过 GPCR(如FPR1) 经典途径激活GRK2,诱导GPCR内化,抑制趋化性。
2. GRK2的双重调控路径
- 经典路径:mtFP → GPCR内化 → GRK2磷酸化 → β-arrestin介导信号终止。
- 非经典路径:mtDNA → TLR9 → GRK2磷酸化 → HDAC6激活 → CttN去乙酰化 → 抑制F-actin聚合。
3. 临床相关性
- 创伤患者血浆 mtDNA水平和PMN pGRK2表达 显著升高,且与感染风险正相关。
三、研究意义
1. 机制创新
- 揭示 DANGER信号通过GRK2双通路(GPCR依赖性和TLR9非依赖性) 抑制中性粒细胞功能的分子机制。
- 提出 GRK2/HDAC双重抑制是恢复免疫功能的潜在策略。
2. 临床转化
- Paroxetine(GRK2抑制剂) 和 Valproate(HDAC抑制剂) 的联合应用可有效降低创伤后感染风险,为开发新型抗感染药物提供依据。
四、Celloger Mini Plus 的详细应用
实验设计
1. 吞噬功能检测
- 样本:人/鼠中性粒细胞与 pH-SA(pHrodo Green S. aureus Bioparticles)共孵育。
- 处理组:
- mtDNA/mtFP预处理组;
- GRK2抑制剂(Paroxetine)或HDAC抑制剂(Valproate)干预组。
- 对照组:无处理组或使用 CQ(氯喹) 阻断内吞。
2. 成像参数
- 仪器:Celloger Mini Plus + EVOS Cell Imaging System。
- 时间点:动态监测 15分钟 内的吞噬过程。
- 分辨率:明场成像(观察细胞形态)+ 荧光成像(pHrodo Green信号)。
3. 数据分析
- 杀菌效率:
- 使用 Celloger Mini Plus 检测活菌比例(图1A);
- 补充平板计数法验证结果一致性。
- 吞噬率:通过流式细胞术量化荧光阳性细胞比例(图1B/C)。
关键结果
- mtDNA抑制吞噬:
- 中性粒细胞对S. aureus的吞噬率显著下降;
- Valproate或Paroxetine预处理 可恢复吞噬功能。
- 动态成像证据:
- mtDNA处理组的中性粒细胞无法有效摄入荧光标记的细菌(图1C,红色箭头示未吞噬颗粒)。

图1.VAL(丙戊酸)和 PAR(帕罗西汀)能够挽救 DAMP(损伤相关分子模式)抑制的 PMN(中性粒细胞)吞噬和杀伤能力。
本研究通过 Celloger Mini Plus 实时动态监测中性粒细胞的吞噬行为,揭示了创伤后DANGER信号通过GRK2/HDAC通路抑制免疫功能的分子机制,并为临床防治创伤后感染提供了 双靶点治疗策略(Paroxetine + Valproate)。该技术的应用为研究免疫细胞动态过程和疾病机制提供了重要工具。
为什么选择 Celloger Mini Plus?
- 动态成像,细节无遗
传统方法只能“死后分析”,而 Celloger Mini Plus 让你“活捉”细胞行为。明场看形态,荧光测功能,吞噬效率、杀菌能力一目了然。 - 高效实验,省时省力
15分钟内完成动态监测,搭配流式细胞术验证,数据可靠又快速。无论是基础研究还是药物筛选,它都能加速你的发现。 - 专业级表现,触手可及
从中性粒细胞的 F-actin 聚合到细菌清除效率,Celloger Mini Plus 的成像结果直接支撑了 GRK2/HDAC 双通路机制的提出,专业度毋庸置疑。 - 科研转化新引擎
这项研究不仅解锁了免疫抑制的秘密,还为抗感染药物开发指路。而这一切,离不开 Celloger Mini Plus 的精准助力。
相关文章
更多 >

