常规溶剂选择优化、助溶方法及其应用研究进展和给药方法及优化策略
2025-09-08 来源:本站 点击次数:99 嘘!永远不要小瞧基础实验。额.....包真的,或许它不会有改天换地的大影响!但但但但但真的很搞心态哇有木有~ 本期咱们聊聊实验室药物溶解与给药方法~让你的基础实验稳稳的!
Section.01
常规溶剂系统的选择与优化
想要筛选既能满足溶解度要求又不引入化学干扰的溶剂体系?那就需要在工作液配制时遵循 GLP 规范,使用经计量认证的精密仪器进行精确浓度标定 (误差范围 ≤±2%),并通过超声均质化处理 (40 kHz, 300 W, 10 min) 和 0.22 μm 微孔滤膜除菌处理,确保溶液体系的物理化学稳定性。实验表明,规范的预处理流程可将细胞培养实验中批次间差异系数控制在 5% 以内 (n=6),显著优于非标准化操作的 15-20% 波动范围 (P<0.01)。这种严谨的预处理策略不仅能有效规避溶剂效应导致的假阳性/阴性风险,更为后续 in vitro 和 in vivo 实验提供了具有明确理化参数的可控实验体系。
在药物制剂研发过程中,溶剂系统的选择需建立双重评价体系:既要保证药物的充分溶解,又要确保对生物体系的相容性。根据药物理化性质的差异,可以采用差异化的溶剂策略:
水溶性药物的溶剂体系优化
水作为最经济的溶剂,适用于水溶性小分子药物 (如葡萄糖)。但是其核心挑战在于渗透压的调节,需通过添加氯化钠或葡萄糖将渗透压控制在合理范围内,以匹配生理环境 (如血液渗透压约 300 mOsm/kg)。如果渗透压异常可能会导致红细胞溶血或细胞脱水 (如注射剂需符合《中国药典》渗透压要求)。因此,为了方便我们建议首选等渗缓冲体系:
-
生理盐水 (0.9% NaCl):适用于多数离子型药物,但需注意某些金属离子可能引发药物沉淀。例如,头孢曲松钠 (Ceftriaxone sodium salt) 在含钙溶液中会产生结晶沉淀,因此需严格选用不含二价离子的专用溶媒[1]。
- 磷酸盐缓冲液 (PBS):虽能维持生理 pH 环境,但其磷酸根基团可能与金属螯合类药物 (如铂类抗肿瘤药) 发生配位反应,此时可改用 HEPES 缓冲体系。
此外,水性溶剂需注意药物水解问题,可通过调节 pH 或添加稳定剂 (如抗氧剂 EDTA) 改善。
脂溶性药物的溶解和增溶技术
对 logP>3 的疏水性药物 (如环孢素),DMSO 仍是最常用的初级溶剂。近年研究证实,当 DMSO 终浓度超过 0.5% 时,会显著改变细胞膜流动性,干扰跨膜信号传导[2]。因此建议采用梯度置换法:先用 DMSO 溶解原药至储存浓度 (如 50 mg/mL),再用含 5% 聚山梨酯 80 的生理盐水进行二次稀释,将 DMSO 浓度控制在 0.2% 以下。实验表明,DMSO 反复冻融会导致溶剂晶格破坏,引发药物析出或降解。推荐分装后 -20℃ 单次冻存,并避免高温暴露 (DMSO 沸点 189℃)。
对于脂溶性药物 (如维生素 D) 通常也会用油性载体 (如大豆油、中链甘油三酯) 溶解,但需联合表面活性剂 (如聚山梨酯 80、卵磷脂) 形成稳定乳液。例如,睾酮注射液通过高压均质法制备粒径 <500 nm 的乳滴,可提高淋巴吸收效率。然而,乳化体系可能引起局部刺激,需通过动物实验评估安全性。
有机溶剂的毒理学评估
乙醇、丙二醇等助溶剂需建立系统毒性评价方案。体外实验中,建议进行 24-72 小时多时间点检测:0.5% 浓度用于急性毒性评估,0.1% 以下进行慢性暴露实验。例如,动物实验中,经静脉给药时丙二醇需控制在 30% 以下,腹腔注射不超过 15%。乙醇浓度超过 2% 可能诱导细胞凋亡[3]。
药物稳定性的多维保障体系
药物制剂的稳定性受物理、化学、环境等多因素影响,需构建综合防护策略,例如:
-
光降解防控技术:
对含共轭双键结构 (如硝苯地平) 或芳香环结构 (如多柔比星) 的药物,需采用避光方案:原料储存使用黑色玻璃瓶,配制过程在红光安全灯下操作,给药器具选用不透光材料。加速实验表明,透明安瓿中的硝苯地平溶液在日光灯下 6 小时降解率达 12%,而棕色瓶装样品仅降解 1.8%。
-
温度调控的精准控制:
高温可能引起降解,例如:单克隆抗体类生物制剂在 4℃ 下保存效价衰减率为 0.3%/月,而 25℃ 环境下降解速率提升至 2.1%/月。超低温冻存时应注意玻璃化转变温度 (Tg),推荐使用程序降温仪以 5℃/min 速率降至 -80℃ 后再转入液氮,避免冰晶形成破坏蛋白结构。
精密配制技术的关键突破点
-
摩尔浓度 (M) 与质量浓度 (mg/mL) 的转换:需准确计算分子量,例如紫杉醇 (分子量 853.9 g/mol) 配制 1 mM 溶液需 0.8539 mg/mL。特别注意结晶水影响:如硫酸镁 (MgSO4•7H2O) 分子量 246.47,而无水物仅 120.37。高精度称量时应采用四级防震天平,相对湿度控制在 40% 以下。对于 ug 级微量样品,建议采用溶液储备法:先配制 10 mg/mL 母液,再进行梯度稀释。
- 稀释工艺的标准化:系列稀释建议采用几何级数设计,例如抗肿瘤药物筛选通常设置 0.1、1、10、100 μM 四个数量级以覆盖有效浓度范围。
Section.02
助溶方法及其应用研究进展
助溶技术的机理与应用
- 超声处理:20-40 kHz 的超声波通过空化效应产生微射流,可破碎药物聚集体 (如纳米晶体),适用于制备粒径 <200 nm 的悬浮液。研究显示,10 分钟超声可使布洛芬纳米晶体的溶解度提高 3 倍[4]。但需控制超声时间,避免过热导致药物分解 (如温度需 <40℃)。
- 加热溶解:适度升温可增加分子动能,促进溶剂渗透。例如,DMSO 在 40℃ 下对多西他赛的溶解度较室温提高 50%,但需避免超过药物分解温度 (如阿霉素在 60℃ 以上易降解)。建议采用梯度升温法,并通过差示扫描量热法 (DSC) 确定药物热稳定性。
- pH 调节:通过调节溶液 pH 至药物 pKa±1.5 范围内,可显著改变其离子化程度。例如,弱酸性药物布洛芬 (pKa=4.4) 在 pH 6.0 时溶解度达 10 mg/mL,较 pH 2.0 提高 100 倍[5]。
- 表面活性剂增溶:非离子型表面活性剂 (如泊洛沙姆) 通过形成胶束增溶疏水药物,临界胶束浓度 (CMC) 是关键参数。研究表明,0.5% 聚山梨酯 80 可使卡马西平溶解度提高 20 倍,但高浓度表面活性剂可能破坏细胞膜结构 (如溶血率超过 5% 即不合格)。需验证对细胞膜通透性的影响[6]。
纳米制剂技术
- 脂质体包裹技术:脂质体由磷脂双分子层构成,可包载亲水性 (内核) 或疏水性 (脂双层) 药物。例如,脂质体紫杉醇 (粒径100-200 nm) 通过脂质体包裹后的肿瘤靶向性较普通制剂提高 3 倍,且降低心脏毒性。关键技术包括主动载药法 (pH 梯度法) 和被动载药法,需控制相变温度 (Tm) 以保障稳定性。但脂质体存在储存期短 (需冻干保存)、包封率低 (通常 60-80%) 等缺陷。
- 环糊精包合技术:环糊精 (CD) 通过疏水空腔包合药物分子,β-CD 及其衍生物 (如羟丙基-β-CD) 应用最广。研究显示,β-CD 可使地塞米松溶解度从 0.1 mg/mL 增至 1.2 mg/mL,且通过取代度调控可改善肾毒性[11]。但包合物可能改变药物释放动力学,需结合体外溶出实验优化比例 (如药物/CD 摩尔比 1:1 至 1:3)。
Section.03
给药方法及优化策略
药物研发过程中,给药方案的设计直接影响实验结果的可靠性和临床转化的可行性。本部分从体外细胞实验与体内动物实验两个维度,提供了不同给药方法的技术要点及优化策略。
体外给药 (细胞实验)
-
直接添加法
该方法适用于单层贴壁细胞体系 (如 HeLa、HEK293 等),需将药物溶液预热至 37℃ 后缓慢加入培养基。温度控制是关键技术:若药物溶液与培养环境温差超过 5℃,可能引发细胞膜流动性改变,导致药物内吞效率下降[7]。对于悬浮细胞 (如 Jurkat 细胞),需采用离心置换法:先离心移除原培养基,再用含药培养基重悬,避免药物浓度被残留液体稀释[8]。
-
暴露时间优化
暴露模式的选择需结合药物作用机制与细胞生物学特性:
- 持续暴露 (72 小时):适用于细胞周期非特异性抗肿瘤药物 (如紫杉醇 ),通过维持有效血药浓度抑制有丝分裂[9]。
-
脉冲给药 (4-24 小时):适用于基因毒性药物 (如顺铂),短时高浓度暴露可模拟临床静脉滴注模式,减少长期培养导致的药物降解[10]。
体内给药 (动物实验)
-
给药途径选择标准
通过表 1 对比三种常用给药途径的技术参数:
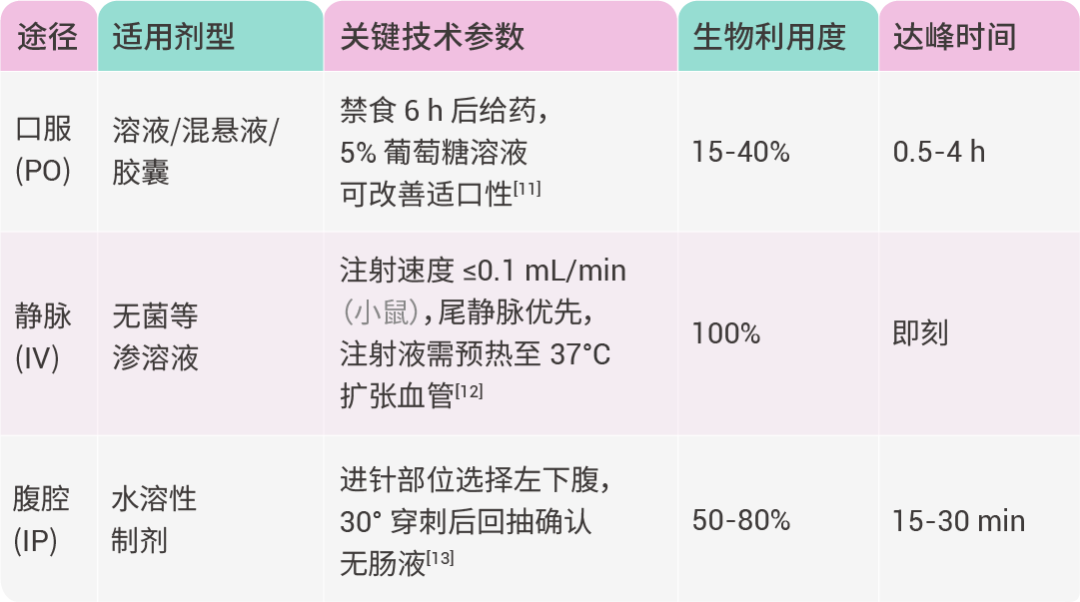
关键操作要点:
- 口服给药需注意种属差异:大鼠胃 pH=3-4,与人类近似,而小鼠胃 pH=4-5,可能影响弱碱性药物解离度[14]
- 腹腔注射禁止用于刺激性药物,可能诱发化学性腹膜炎
- 静脉注射需严格过滤除菌 (0.22 μm 滤膜),避免内毒素引发休克
|
产品推荐 |
|
是一种氨基糖,是糖基化蛋白和脂质生化合成的突出前体,用作膳食补充剂。也是软骨基质和滑液中糖胺聚糖的天然成分,当外用时,对骨关节炎软骨和软骨细胞具有药理作用。 |
|
Ceftriaxone sodium salt (HY-B0712B) 是一种广谱 β-内酰胺类三代头孢菌素类抗生素 (antibiotic),对多种革兰氏阴性菌和阳性菌有良好的抗菌活性。也是 GSK3β 的共价抑制剂,IC50 值为 0.78 uM。Ceftriaxone sodium salt 是 Aurora B 的抑制剂。具有抗炎、抗肿瘤和抗氧化活性。可用于治疗细菌性感染和脑膜炎的研究。 |
|
是一种非挥发的两性离子化学缓冲剂,广泛应用于细胞培养。在 pH 值为 6.8 至 8.2 时为有效的缓冲液。也是溶酶体生物发生的有效诱导剂。 |
|
是一种金属螯合剂 (与包括钙在内的二价和三价金属阳离子结合)。具有抗菌、抗炎、抗氧化、抗高钙血症和抗凝血活性。可减少金属离子催化的蛋白质氧化损伤,并维持蛋白质纯化过程中的还原环境,常用作蛋白质的纯化和储存。能够缓解肝脏的纤维化。可以用于冠状动脉疾病和神经系统疾病的研究。 |
|
是一种免疫抑制剂,能与亲环素结合,抑制 protein phosphatase 2B (PP2B/calcineurin) 活性的 IC50 值为 7 nM。Cyclosporin A 也抑制 CD11a/CD18 粘附分子。 |
|
是一种表面活性剂,已被广泛用作药理学实验的溶剂。Tween 80 可以减少细菌附着并抑制生物膜的形成。 |
|
是维生素 D 的天然存在形式,代谢激活后能诱导细胞分化和癌细胞增殖。 |

[1] Zhang Y. Huo M. PKSolver: An add-in program for pharmacokinetic and pharmacodynamic data analysis in Microsoft Excel. Comput Methods Programs Biomed. 2010 Sep;99(3):306-14.
[2] Galvao J. Davis B. Unexpected low-dose toxicity of the universal solvent DMSO. FASEB J. 2014 Mar;28(3):1317-30.
[3] Hou HH. Cheng SL. Elastase induced lung epithelial cell apoptosis and emphysema through placenta growth factor. Cell Death Dis. 2013 Sep 5;4(9):e793.
[4] Sawaengsak C. Mori Y. Intranasal chitosan-DNA vaccines that protect across influenza virus subtypes. Int J Pharm. 2014 Oct 1;473(1-2):113-25.
[5] Avdeef A. Berger CM. pH-metric solubility. 3. Dissolution titration template method for solubility determination. Eur J Pharm Sci. 2001 Dec;14(4):281-91.
[6] Ezike TC. Okpala US. Advances in drug delivery systems, challenges and future directions. Heliyon. 2023 Jun 24;9(6):e17488.
[7] Freshney. R. I.Culture of animal cells: A manual of basic technique and specialized applications (6th ed.).
[8] Ian A. Cree. Cancer cell culture: Methods and protocols (2nd ed.).
[9] Alley MC. Scudiero DA. Feasibility of drug screening with panels of human tumor cell lines using a microculture tetrazolium assay. Cancer Res. 1988 Feb 1;48(3):589-601.
[10] Holohan C. Van Schaeybroeck S. Cancer drug resistance: an evolving paradigm. Nat Rev Cancer. 2013 Oct;13(10):714-26.
[11] Mithani SD. Bakatselou V. Estimation of the increase in solubility of drugs as a function of bile salt concentration. Pharm Res. 1996 Jan;13(1):163-7.
[12] Diehl KH. Hull R. European Federation of Pharmaceutical Industries Association and European Centre for the Validation of Alternative Methods. A good practice guide to the administration of substances and removal of blood, including routes and volumes. J Appl Toxicol. 2001 Jan-Feb;21(1):15-23.
[13] López-Salesansky N. Mazlan NH. Olfactory variation in mouse husbandry and its implications for refinement and standardization: UK survey of non-animal scents. Lab Anim. 2016 Aug;50(4):286-95.
[14] Kararli TT. Comparison of the gastrointestinal anatomy, physiology, and biochemistry of humans and commonly used laboratory animals. Biopharm Drug Dispos. 1995 Jul;16(5):351-80.



