华中科技大学同济医学院研究团队揭示肺动脉高压潜在治疗靶点
2025-11-10 来源:本站 点击次数:450文章标题:Binding of Hypoxia-Induced Mitogenic Factor/RELM-β to Bone Morphogenetic Protein Receptor 2 Complex Promotes Pulmonary Hypertension
发表期刊:Arteriosclerosis, Thrombosis, and Vascular Biology (IF 7.4)
合作客户:华中科技大学同济医学院基础医学院胡清华/肖瑞研究团队
维真助力:
病毒产品:AAV6-HIMF、AAV6-BMP2
注射方式:气管插管术(SD大鼠)
病毒用量:5×10^11 or 1×10^12 vg/rat
发表期刊:Arteriosclerosis, Thrombosis, and Vascular Biology (IF 7.4)
合作客户:华中科技大学同济医学院基础医学院胡清华/肖瑞研究团队
维真助力:
病毒产品:AAV6-HIMF、AAV6-BMP2
注射方式:气管插管术(SD大鼠)
病毒用量:5×10^11 or 1×10^12 vg/rat
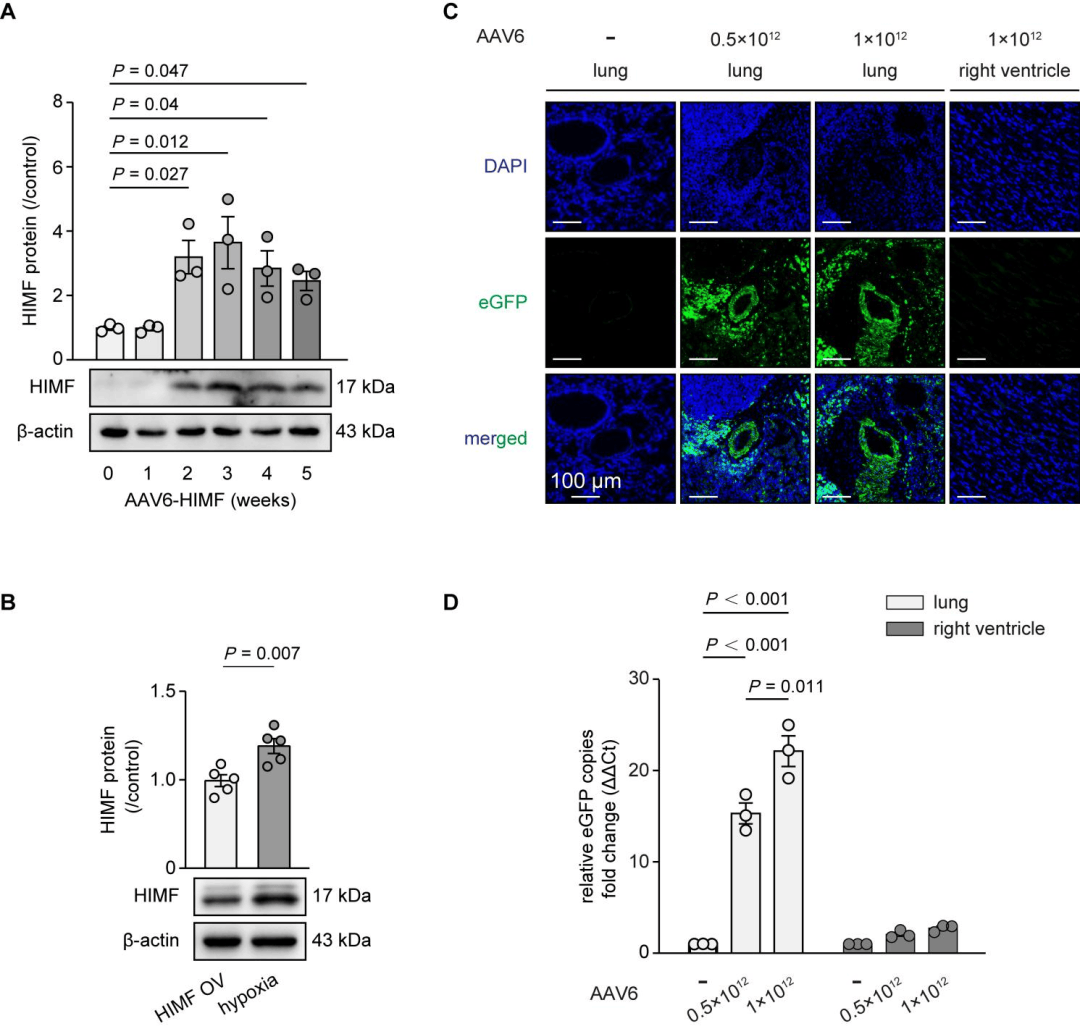
AAV6在大鼠肺组织中的递送效率检测
研究背景
缺氧诱导有丝分裂因子(HIMF)是一种由慢性缺氧诱导的分泌型细胞因子,可促进肺动脉高压,但其细胞外膜受体的分子特性尚不清楚。骨形态发生蛋白受体2(BMPR2)是TGF-β/BMP家族成员,其基因突变、表达降低或功能异常,在遗传性、特发性及慢性缺氧诱导的肺动脉高压中均起关键作用,且BMPR2的激活依赖其与BMPR1家族(如BMPR1A)形成异二聚体复合物。本研究旨在筛选并鉴定HIMF的胞外受体,阐明 HIMF通过该受体调控肺动脉高压的分子机制,探索潜在治疗靶点。
缺氧诱导有丝分裂因子(HIMF)是一种由慢性缺氧诱导的分泌型细胞因子,可促进肺动脉高压,但其细胞外膜受体的分子特性尚不清楚。骨形态发生蛋白受体2(BMPR2)是TGF-β/BMP家族成员,其基因突变、表达降低或功能异常,在遗传性、特发性及慢性缺氧诱导的肺动脉高压中均起关键作用,且BMPR2的激活依赖其与BMPR1家族(如BMPR1A)形成异二聚体复合物。本研究旨在筛选并鉴定HIMF的胞外受体,阐明 HIMF通过该受体调控肺动脉高压的分子机制,探索潜在治疗靶点。
研究结果
1.HIMF与BMPR2相互作用介导肺动脉高压
研究团队首先通过序列比对筛选GPR98、CaSR等候选受体,再通过HIMF抗体沉淀肺动脉膜蛋白裂解物并进行蛋白质组学分析,初筛出8个候选受体,交叉免疫沉淀和免疫印迹等证实BMPR2与HIMF存在相互作用,并且HIMF与BMPR2相关复合物的相互作用会对BMPR2活性产生负向调控,抑制其下游信号传导,进而解除BMPR2对PASMC增殖的抑制作用,最终推动肺动脉高压进展。随后利用AAV6-HIMF构建大鼠HIMF过表达模型,结果显示HIMF表达显著升高,同时BMPR2信号通路活性降低,并伴随肺动脉高压典型病理表型。此外,HIMF过表达还会诱导TGF-β1表达升高和Smad2/3磷酸化增强,而BMP2过表达或FK506干预可逆转这些效应。最后,研究人员还证实在缺氧诱导的肺动脉高压模型中,相比于低剂量组,高剂量AAV6-BMP2可显著减轻肺动脉高压病理表型,并有效恢复肺动脉中BMPR2信号。安全性评估显示,高剂量AAV6-BMP2对大鼠肝肾功能无显著影响,且通过检测肺和右心室中报告基因的表达,证实AAV6可特异性靶向肺组织,验证了该基因递送系统的特异性和安全性。
1.HIMF与BMPR2相互作用介导肺动脉高压
研究团队首先通过序列比对筛选GPR98、CaSR等候选受体,再通过HIMF抗体沉淀肺动脉膜蛋白裂解物并进行蛋白质组学分析,初筛出8个候选受体,交叉免疫沉淀和免疫印迹等证实BMPR2与HIMF存在相互作用,并且HIMF与BMPR2相关复合物的相互作用会对BMPR2活性产生负向调控,抑制其下游信号传导,进而解除BMPR2对PASMC增殖的抑制作用,最终推动肺动脉高压进展。随后利用AAV6-HIMF构建大鼠HIMF过表达模型,结果显示HIMF表达显著升高,同时BMPR2信号通路活性降低,并伴随肺动脉高压典型病理表型。此外,HIMF过表达还会诱导TGF-β1表达升高和Smad2/3磷酸化增强,而BMP2过表达或FK506干预可逆转这些效应。最后,研究人员还证实在缺氧诱导的肺动脉高压模型中,相比于低剂量组,高剂量AAV6-BMP2可显著减轻肺动脉高压病理表型,并有效恢复肺动脉中BMPR2信号。安全性评估显示,高剂量AAV6-BMP2对大鼠肝肾功能无显著影响,且通过检测肺和右心室中报告基因的表达,证实AAV6可特异性靶向肺组织,验证了该基因递送系统的特异性和安全性。
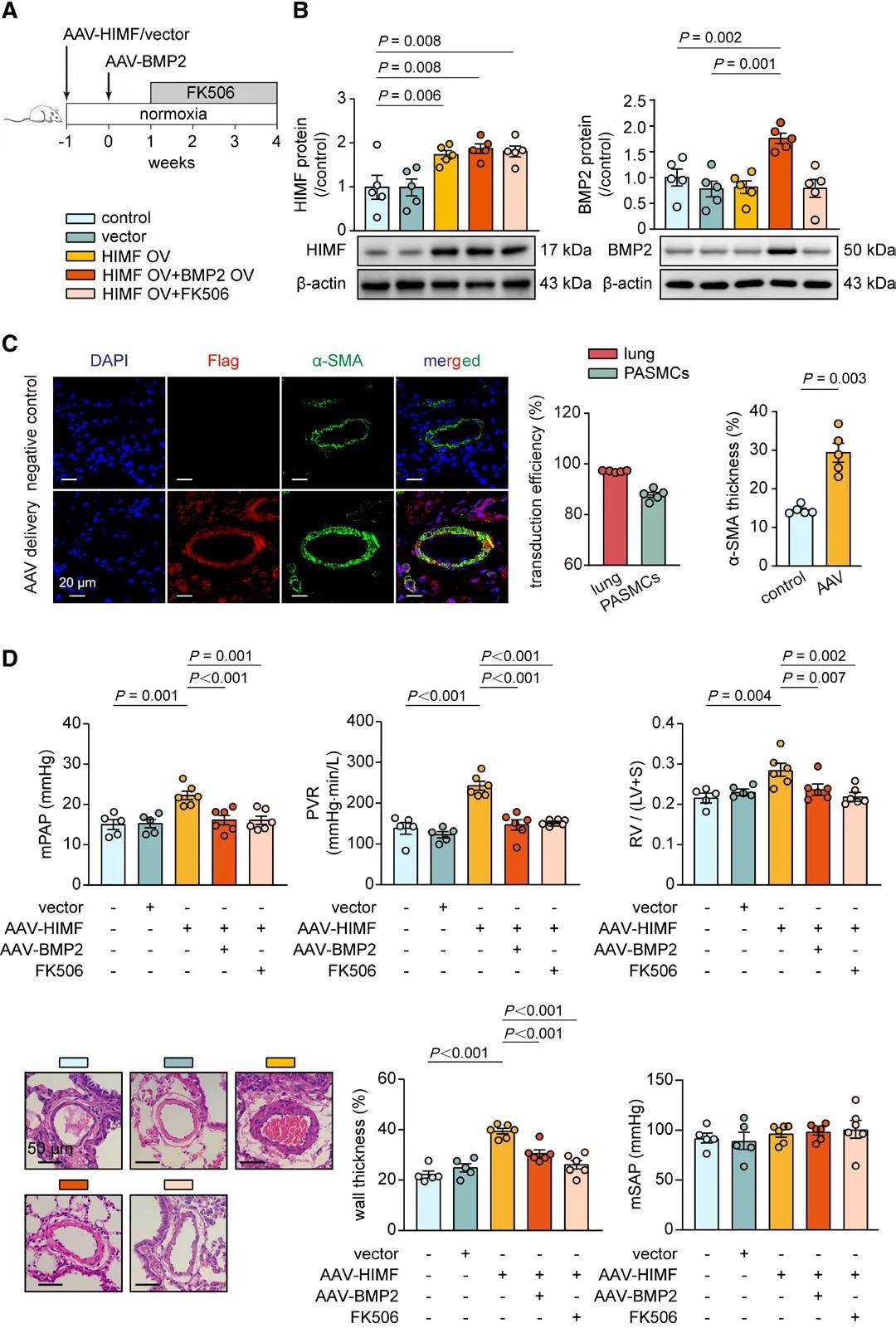
BMPR2激动剂BMP2和FK506减轻由HIMF过表达诱导的肺动脉高压
2.阻断HIMF-BMPR1A相互作用可减缓肺动脉高压的发展
通过进一步的探索,研究团队证实HIMF通过直接结合BMPR1A的DTLPF基序,竞争性破坏BMPR1A/BMPR2复合物形成,进而导致BMPR2活性降低和BMPR2表达减少。接下来,研究团队构建了BMPR1A突变大鼠,将其胞外域54-58位的HIMF结合关键基序DTLPF替换为AAAAA。与野生型大鼠相比,突变大鼠在慢性缺氧条件下肺动脉高压病理表型显著改善,BMPR2活性得以恢复。随后通过设计3种靶向BMPR1A DTLPF基序的阻断肽并在原代PASMC中验证效果,鉴定肽3在破坏HIMF与BMPR1A结合方面具有更高效率,恢复了BMPR2活性并抑制细胞增殖;此外,阻断肽3在体内慢性缺氧及Sugen/缺氧模型中均有效缓解了肺动脉高压。
通过进一步的探索,研究团队证实HIMF通过直接结合BMPR1A的DTLPF基序,竞争性破坏BMPR1A/BMPR2复合物形成,进而导致BMPR2活性降低和BMPR2表达减少。接下来,研究团队构建了BMPR1A突变大鼠,将其胞外域54-58位的HIMF结合关键基序DTLPF替换为AAAAA。与野生型大鼠相比,突变大鼠在慢性缺氧条件下肺动脉高压病理表型显著改善,BMPR2活性得以恢复。随后通过设计3种靶向BMPR1A DTLPF基序的阻断肽并在原代PASMC中验证效果,鉴定肽3在破坏HIMF与BMPR1A结合方面具有更高效率,恢复了BMPR2活性并抑制细胞增殖;此外,阻断肽3在体内慢性缺氧及Sugen/缺氧模型中均有效缓解了肺动脉高压。
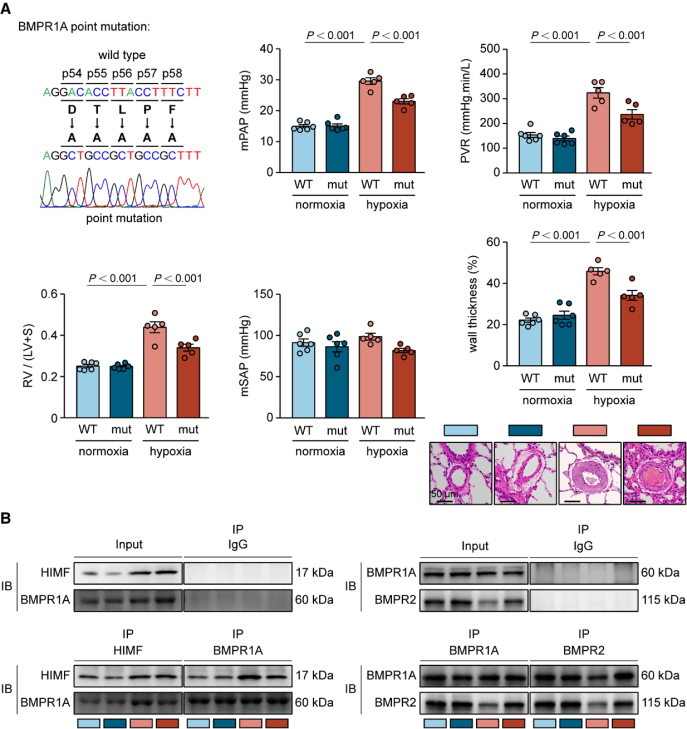
阻断HIMF-BMPR1A相互作用可减缓肺动脉高压的发展
研究结论
本研究表明BMPR1A是HIMF的受体,其胞外区54-58个氨基酸的结合导致BMPR1A/BMPR2异聚体复合物的破坏和BMPR2活性的降低。研究结果揭示了HIMF和BMPR1A/BMPR2信号复合物在肺动脉高压中的病理生理作用,通过阻断HIMF与BMPR1A的结合,提供了一种新的治疗途径来拯救BMPR2信号传导。
本研究表明BMPR1A是HIMF的受体,其胞外区54-58个氨基酸的结合导致BMPR1A/BMPR2异聚体复合物的破坏和BMPR2活性的降低。研究结果揭示了HIMF和BMPR1A/BMPR2信号复合物在肺动脉高压中的病理生理作用,通过阻断HIMF与BMPR1A的结合,提供了一种新的治疗途径来拯救BMPR2信号传导。
相关文章
更多 >

