肺癌化疗耐药性产生机制及解决途径
2026-01-12 来源:本站 点击次数:342研究背景
肺癌化疗耐药性的产生与增殖、转移及干细胞性等多种恶性表型密切相关。长链非编码RNA(lncRNA)会导致肺癌的耐药性,但相关机制尚不清楚。近期滨州医学院附属医院杜静团队联合林茨大学Clemens A. Schmitt团队在CELLULAR & MOLECULAR BIOLOGY LETTERS (IF 10.2)上发表文章“lncRNA IGFL2‑AS1 mediates NSCLC chemoresistance via YBX1‑induced HSPA1A/RAP1 activation”,发现IGFL2-AS1/YBX1/HSPA1A轴在促进NSCLC(非小细胞肺癌)化疗耐药和转移中的关键作用,为逆转NSCLC耐药提供了极具潜力的新型治疗靶点。
· 维真助力 - 慢病毒和质粒·
实验细胞:肺癌细胞A549和H520
慢病毒及质粒产品:Lv-CMV-IGFL2-AS1、Lv-U6-shRNA-IGFL2-AS1;
CEBP-β、YBX1、shYBX1、HSPA1A和shHSPA1A质粒
结果展示
1. IGFL2-AS1调节肺癌细胞增殖、转移、干细胞性和耐药性
作者发现IGFL2-AS1在耐药肺癌细胞中表达上调,并与肺癌患者的生存率较差相关。通过基因功能获得和丧失分析,评估IGFL2-AS1对肺癌的作用,发现在A549和H520中,IGFL2-AS1过表达显著增加了肺癌细胞的增殖能力,并上调EMT相关标记物。此外肺癌细胞中过表达外源IGFL2-AS1促进干细胞样细胞增殖并上调干细胞特异性标志物。CCK8检测发现,A549和H520细胞中IGFL2-AS1过表达显著增加了DDP和5-FU的IC50值,但没有增加吉非替尼和奥西替尼的IC50值,表明IGFL2-AS1表达与肺癌细胞的化疗耐药性呈正相关。相反IGFL2-AS1敲低则显著抑制肺癌细胞的增殖,降低其迁移能力,并下调EMT相关标志物的表达,同时抑制肺肿瘤干细胞球的生长,增加肺癌细胞对DDP和5-FU的敏感性。
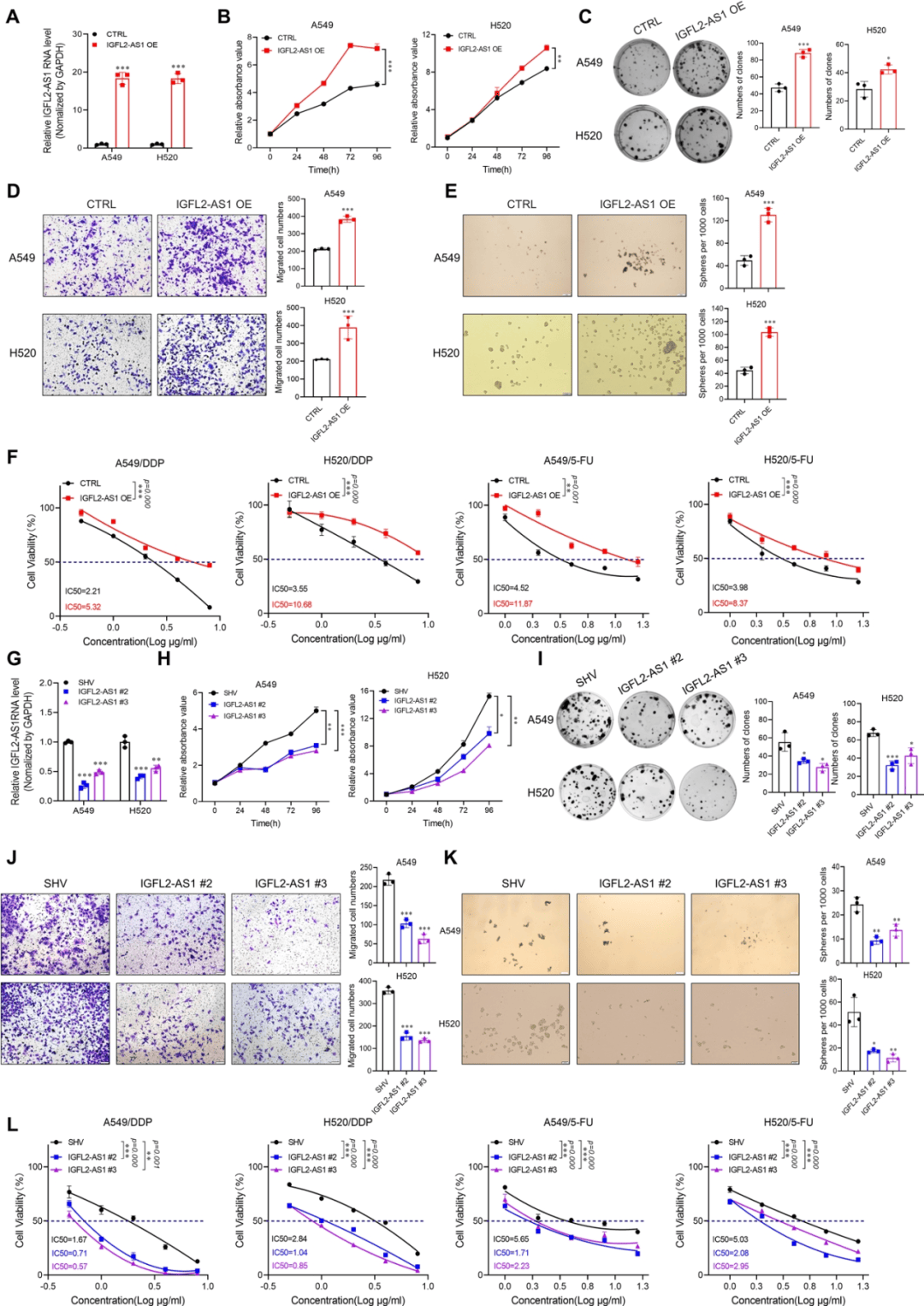 图1 IGFL2-AS1调节肺癌细胞增殖、转移、干细胞性和耐药性
图1 IGFL2-AS1调节肺癌细胞增殖、转移、干细胞性和耐药性
2. IGFL2-AS1调节肺癌肿瘤的体内增殖和药物敏感性
作者将荧光素酶标记的A549和IGFL2-AS1敲低A549皮下植入免疫缺陷小鼠体内,然后给予DDP或5-FU,发现IGFL2-AS1敲低A549细胞相较于对照细胞对DDP或5-FU疗法更敏感。肿瘤生长曲线表明,敲低IGFL2-AS1可抑制肿瘤增殖,并显著提高DDP和5-FU联合治疗的疗效。肿瘤整体成像和重量定量证实了IGFL2-AS1作为肺癌刺激剂的功能,有助于耐药性。病理染色证实IGFL2-AS1敲低会减少增殖和干性相关基因表达。作者还建立了肺转移模型,以评估IGFL2-AS1对肺癌远端转移的影响,发现IGFL2-AS1促进A549转移至肺和脑,但IGFL2-AS1敲低减少了远端转移。H&E染色和肺部转移灶的定量进一步揭示了IGFL2-AS1对远端转移的强烈调节作用。这些数据表明IGFL2-AS1在体内促进肺癌增殖、耐药性和转移,表明其在肺癌的发病和进展中发挥着关键作用。机制研究发现IGFL2-AS1将YBX1招募到HSPA1A启动子上,促进HSPA1A转录和表达,进而促进肺癌增殖、转移、耐药性和干细胞性。
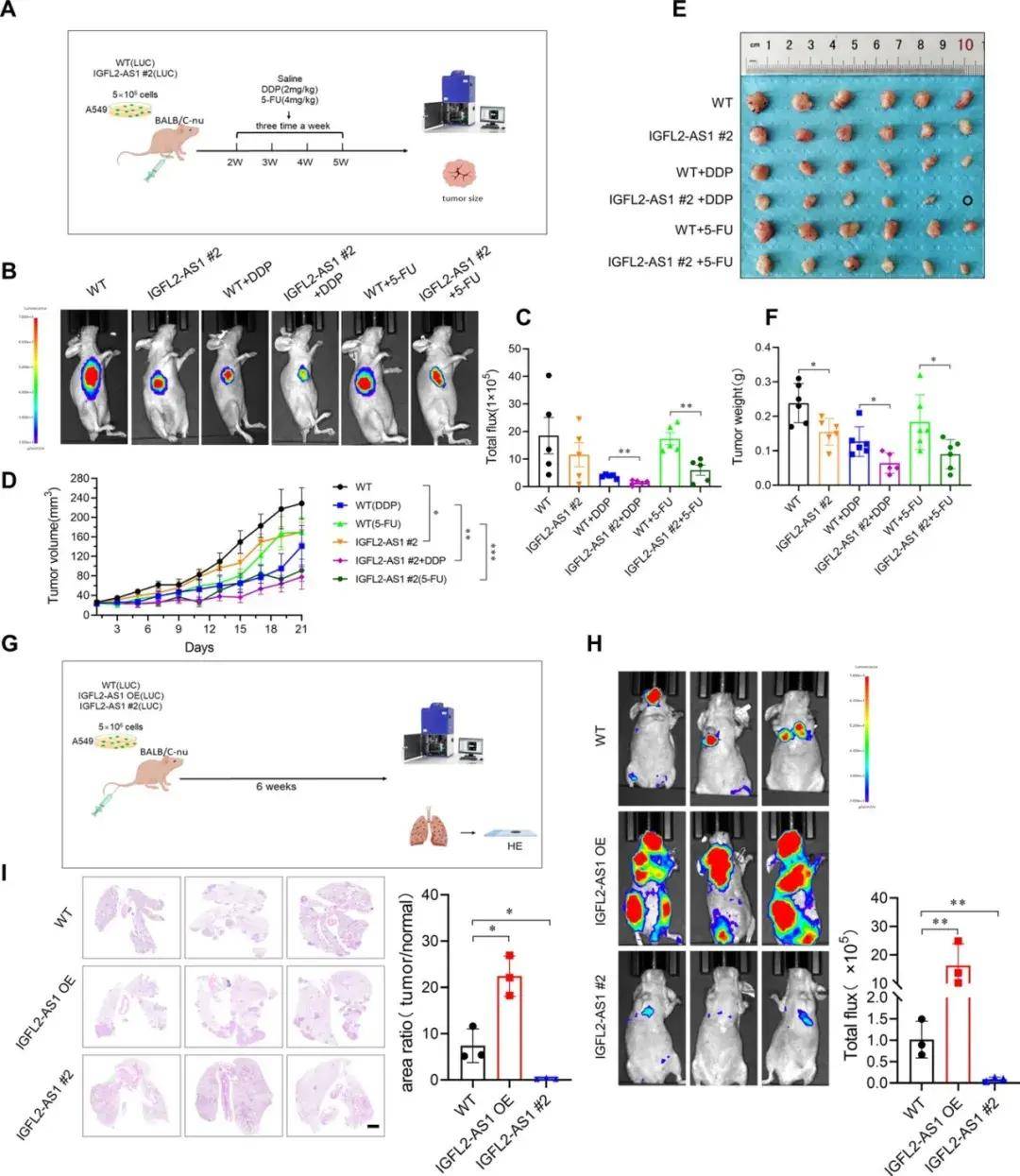 图2 IGFL2-AS1调节肺癌肿瘤的体内增殖和药物敏感性
图2 IGFL2-AS1调节肺癌肿瘤的体内增殖和药物敏感性
3. HSPA1A的药理学抑制可恢复化疗敏感性并减弱体内肺癌细胞转移
由于HSPA1A是IGFL2-AS1/YBX1/HSPA1A轴的关键执行子,作者在小鼠模型中通过单独使用HSPA1A抑制剂(VER155008)以及HSPA1A抑制剂与化疗药物联合使用的方式,验证HSPA1A的功能。发现VER155008增强了低剂量DDP对皮下肿瘤生长的轻微抑制作用。肿瘤体积和重量证实,VER155008增强低剂量DDP和5-FU在皮下植入肺癌模型中的抗肿瘤功效。IHC染色表明,与单一疗法或对照组相比,VER155008和DDP或5-FU组合导致肿瘤增殖能力最低。单独使用VER155008可减少远端器官的A549转移,并进一步增强DDP和5-FU的抗转移功效。HE染色显示VER155008单药治疗组的肺部转移灶显著减少,而联合治疗组则消除肺部转移灶。这些结果表明HSPA1A抑制有效抑制肺转移并增强肺癌细胞对体内化疗药物的敏感性。
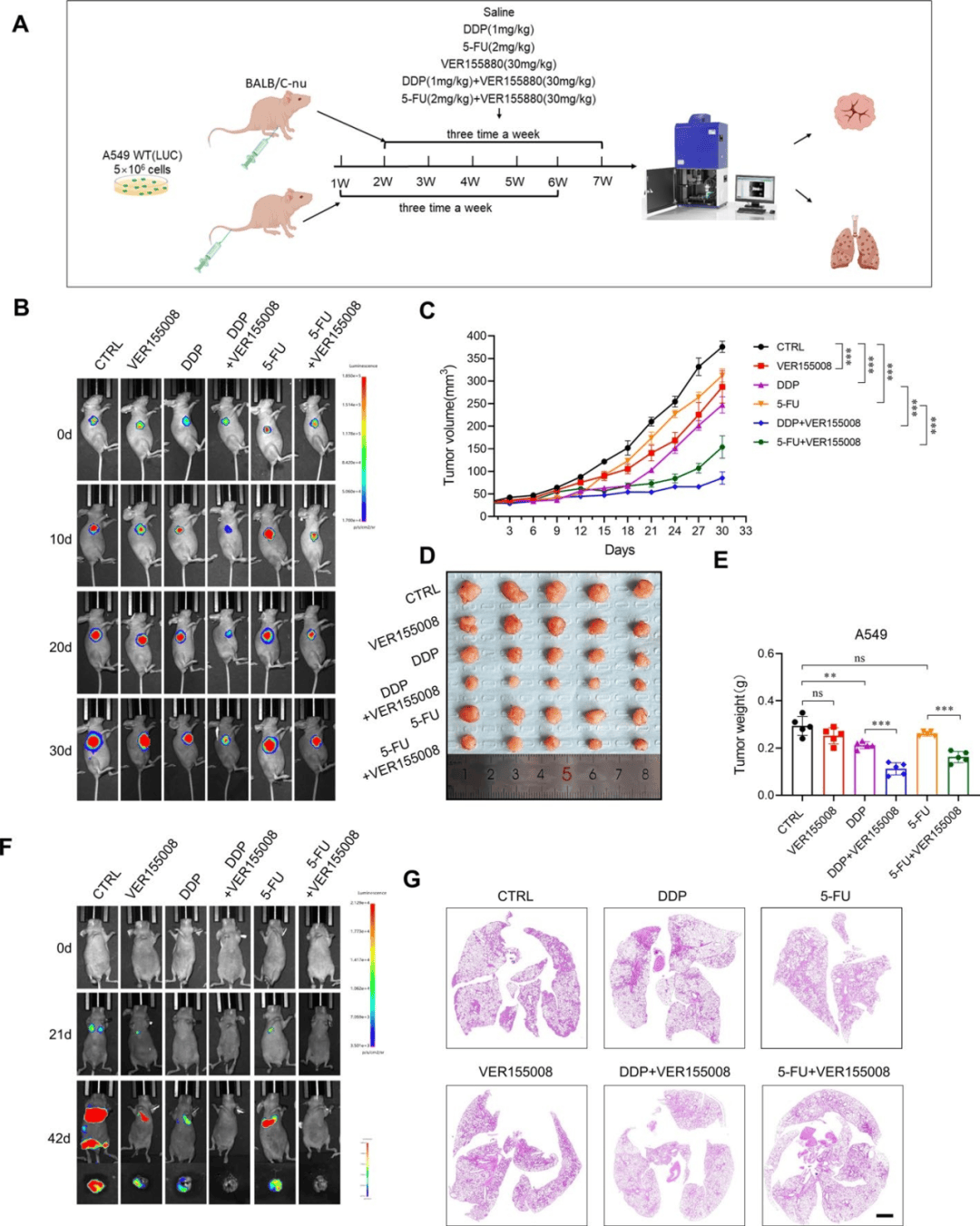 图3 HSPA1A药理学抑制可恢复化疗敏感性并减弱体内肺癌细胞转移
图3 HSPA1A药理学抑制可恢复化疗敏感性并减弱体内肺癌细胞转移
实验结论
本研究发现IGFL2-AS1/HSPA1A/RAP1轴在肺癌细胞中异常激活,并与不良预后相关,强调了IGFL2-AS1/YBX1/HSPA1A轴在促进NSCLC化疗耐药和转移中的关键作用,表明靶向该轴可以克服肺癌的耐药性并改善患者的预后。

