腺相关病毒/AAV包装系统的介绍与腺相关病毒包装流程
2026-01-19 来源:本站 点击次数:339腺相关病毒(Adeno-associated virus)属于细小病毒科,Dependoparvovirus属,是目前发现的一类结构简单、无包膜的单链DNA缺陷型病毒,它的生命周期依赖于复制病毒的参与,如腺病毒和单纯疱疹病毒。野生型的腺相关病毒可以定点整合到人类第19号染色体的AAVS1位点,而重组腺相关病毒由于缺少整合和复制必需的两个基因而无法整合。因此,重组腺相关病毒主要以游离于染色体的附加体形式存在,并可长时间存在于非分裂细胞中。另外,腺相关病毒具有高组织特异性、良好的扩散性、低免疫原性、高安全性和稳定性。基于以上特点,重组腺相关病毒已经成为科研和基因治疗中具市场前景的病毒载体之一。
腺相关病毒/AAV包装系统
AAV无辅助病毒系统(AAV Helper-Free System)可以在无辅助病毒的条件下生产出重组腺相关病毒。这种系统利用已经明确与调节AAV复制和表达的腺病毒基因产物,并且将这些基因产物通过转染引进宿主细胞。重组腺相关病毒(rAAV)由多个质粒(Cis质粒、辅助质粒、Rep/Cap质粒)组成,利用三质粒共转染方法进行rAAV的生产。包装细胞反式提供AAV的结构蛋白Cap及功能蛋白Rep,在包装辅助质粒Adv-Helper的帮助下,高效地将带有ITR的目的DNA片段包装到rAAV病毒颗粒中。
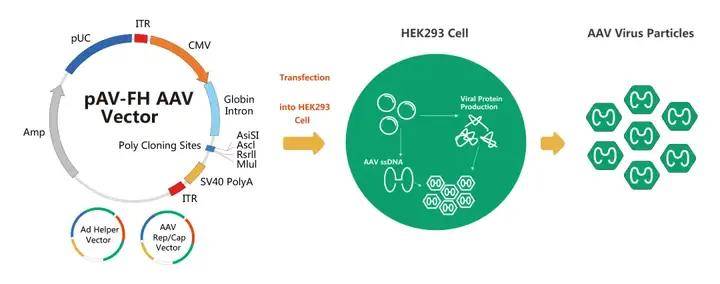 图1. AAV无辅助病毒系统
图1. AAV无辅助病毒系统
腺相关病毒/AAV包装流程
首先,将外源基因克隆进入腺相关病毒载体,将携带外源基因的重组质粒与辅助质粒Ad Helper Vector和pAAV-rep/capVector共转染包装细胞HEK293T,转染72h后细胞内会产生大量的重组病毒。分别收获培养基上清与细胞沉淀,用PEG8000沉淀培养基上清中的病毒,裂解细胞沉淀收毒,合并从细胞沉淀和上清中得到的病毒。接下来,对收集的病毒进行纯化浓缩,滴度、纯度检测。
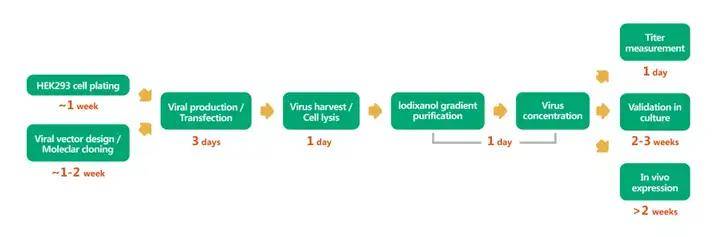 图2. AAV从头合成流程
图2. AAV从头合成流程
腺相关病毒/AAV纯化
采用碘克沙醇密度梯度超速离心法对AAV病毒进行纯化。碘克沙醇是一种造影剂,已接受了临床检验。它具有非离子型、对细胞无毒和代谢惰性等优点。现在在病毒纯化方面应用广泛。它利用不同颗粒之间存在的沉降系数差,在一定离心力作用下,颗粒各自以一定速度沉降,在密度梯度不同区域上形成区带。
 图3. AAV病毒纯化前后的示意图
图3. AAV病毒纯化前后的示意图
腺相关病毒/AAV滴度检测
通过QPCR的方法来检测AAV病毒滴度,得到的结果为包装得到的病毒颗粒数。其原理是用腺相关病毒基因组特异性引物进行实时定量PCR。在定量曲线的线性范围内,Ct值与已知拷贝数质粒的Ct值的比值即为病毒基因组的初始拷贝数。
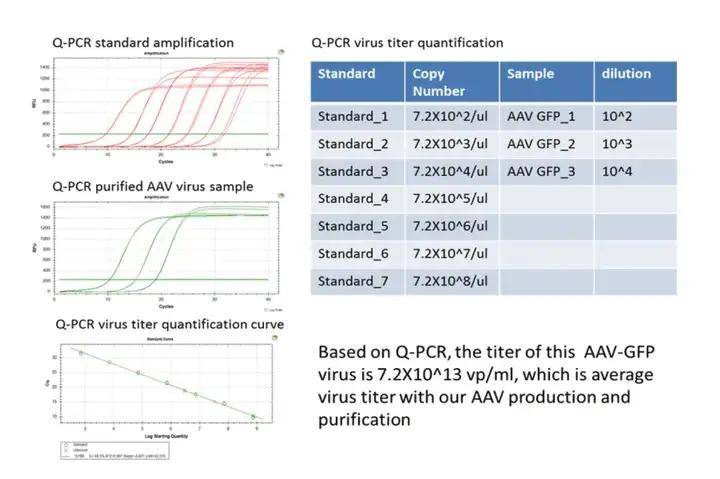 图4. AAV-GFP滴度的检测结果
图4. AAV-GFP滴度的检测结果
腺相关病毒/AAV纯度检测
AAV纯度可以通过灵敏的银染方法进行检测。AAV衣壳蛋白含有3种亚基VP1(82kDa)、VP2(72kDa)、VP3(62kDa),且所占比例为VP1:VP2:VP3=1:1:10。因此,一个纯度高的AAV在SDS-PAGE分析时仅显示三条带。
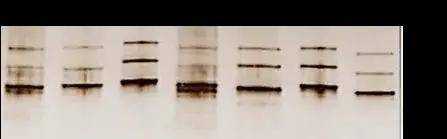
图5. 纯化后AAVs的银染结果

