中大张弩/北大白凡团队解锁胶质母细胞瘤免疫新机制
2026-03-02 来源:本站 点击次数:54胶质母细胞瘤(GBM)是最致命的原发性中枢神经系统(CNS)肿瘤,其肿瘤微环境(TME)具有强免疫抑制性,缺乏有效肿瘤特异性细胞毒性T淋巴细胞(CTLs),现有免疫治疗响应率低。硬脑膜作为CNS免疫监视的关键界面,其在GBM抗肿瘤免疫中的作用及调控机制尚未明确,亟须开发靶向脑膜免疫的治疗策略。2026年2月4日,中山大学附属第一医院张弩教授、北京大学白凡教授共同通讯在国际顶尖学术期刊Cell(IF 42.5)在线发表题为“Meningeal blood vessel blockage enhances anti-glioblastoma immunity”的研究论文。研究表明脑膜血管阻断有效地抑制了GBM在小鼠模型中的进展。在临床前模型中,该手术通过选择性扩增硬脑膜驻留边界相关巨噬细胞(rBAM)——这类细胞具有增强的抗原提呈功能且可高效激活T细胞——从而强化抗肿瘤免疫。该研究提出了一种通过手术干预增强GBM免疫治疗的新策略。

· 维真助力 - AAV·
病毒产品:rAAV9-CD206-EGFP-CD86shRNA(2.54×10^13 VG/mL);rAAV9-CD206-EGFP-CD80shRNA(2.42×10^13 VG/mL);rAAV9-CD206-EGFP-Scramble-shRNA(2.32×10^13 VG/mL);
实验动物:C57BL/6 小鼠
注射方式及靶向细胞:硬膜外注射,靶向边界相关巨噬细胞
注射体积:10μL
研究结果
1、脑膜血管闭塞(MBB)增强GBM微环境中的抗肿瘤免疫作用
研究团队利用硬脑膜与脑实质血管供血分离的解剖特点,通过双侧颈外动脉结扎构建MBB模型。评估发现MBB特异性调节硬脑膜血管系统,而不会对大脑或系统免疫细胞亚群的血液供应和功能产生显著影响。研究团队在多种GBM模型中验证了MBB的疗效,但其在免疫缺陷小鼠中无效,表明MBB是一种通过免疫依赖机制对抗中枢神经系统恶性肿瘤的有效策略。为了阐明MBB在GBM TME中的免疫调节作用,研究人员对肿瘤组织进行了scRNA-seq测序分析,MBB组T细胞活化和增殖的正向调节通路显著富集。MBB组CD8+T细胞中细胞因子生成(如Il2rg、Il2rb、Il9r等)增强、细胞毒性(如Gzmb、Prf1、Ifng等)增强以及T细胞受体(TCR)信号传导(如Cd3e、Cd3g、Lck等)增强,同时伴随着耗竭标志物(如 Havcr2、Pdcd1、Lag3 等)表达增加,表明MBB可能增强对免疫检查点疗法的反应性。此外,MBB还能诱导肿瘤相关巨噬细胞(TAM)向促炎表型转化,提升抗肿瘤免疫应答。以上结果表明,MBB可以通过恢复抗肿瘤T细胞反应和减弱TAMs的免疫抑制表型来逆转GBM的“免疫排斥”肿瘤微环境。
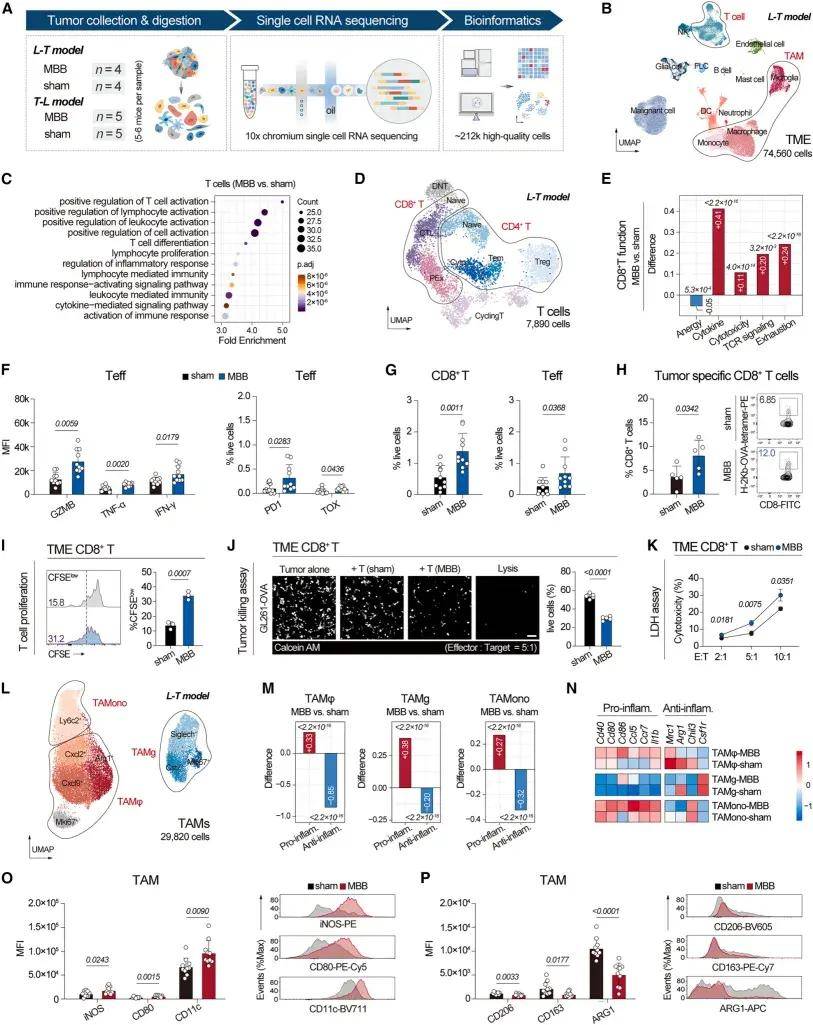 图1. MBB增强GBM微环境中的抗肿瘤免疫作用
图1. MBB增强GBM微环境中的抗肿瘤免疫作用
2、硬脑膜组织驻留型巨噬细胞(rBAM)是核心免疫效应细胞
研究人员对来自无肿瘤对照组、荷瘤对照组和荷瘤MBB治疗组的小鼠硬脑膜样本进行了scRNA-seq分析,鉴定出两种巨噬细胞亚群:组织驻留型巨噬细胞(rBAM)和循环来源巨噬细胞(cBAM)。通过免疫荧光检测,在人样本中观察到硬脑膜rBAM比例与肿瘤内 CD8+ T细胞数量呈正相关,强调了rBAM在形成抗肿瘤T细胞免疫中的作用。研究人员进一步探究了rBAM和cBAM对实质性肿瘤发生的不同反应的分子机制,发现rBAM特异性高表达新生儿Fc受体(FcRn),在GBM患者脑脊液中存在大量肿瘤相关抗体免疫复合物(ICs)。当暴露于ICs时,来自非荷瘤小鼠的rBAM与cBAM相比显示出显著增强的T细胞激发能力,使用FcRn特异性抑制剂或突变型ICs阻断此通路可消除这一效应,表明FcRn是调节rBAM对ICs反应的关键决定因素。这些发现确立了FcRn介导的IC识别是rBAM在肿瘤发生过程中高效激活T细胞免疫的核心机制。
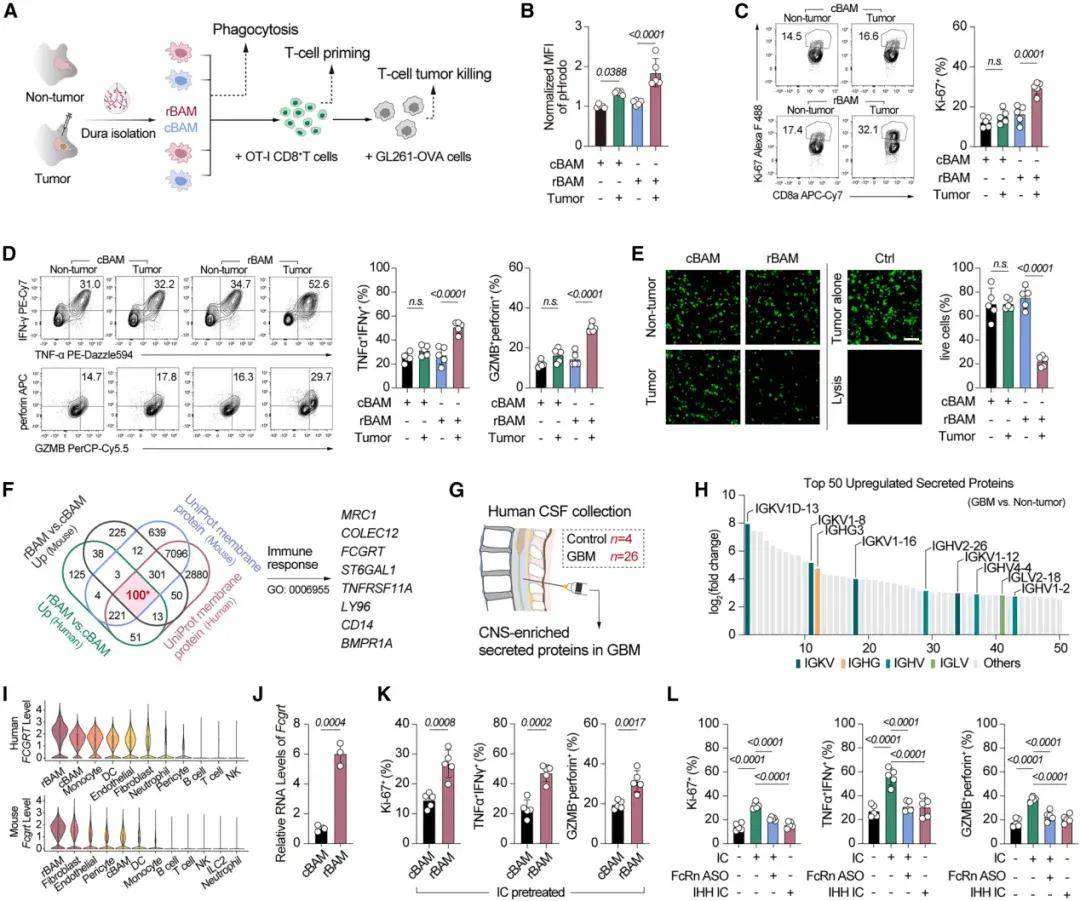 图2. FcRN是rBAM增强肿瘤监测的关键因素
图2. FcRN是rBAM增强肿瘤监测的关键因素
3、MBB 通过限制cBAM对CSF-1的消耗并创造富含CSF-1的微环境来扩增 rBAM
接下来,研究人员探索了MBB如何增强脑膜免疫功能。小鼠硬脑膜的整体IF染色显示,MBB导致rBAM数量显著增加,而cBAM数量减少。MBB通过抑制cBAM的募集,创造了一个富含CSF-1的环境,从而推动了代偿性rBAM的增殖。进一步探究MBB是否影响rBAM和cBAM的功能,scRNA-seq显示MBB增强了rBAM亚群的免疫活性和新抗原摄取能力,在cBAM亚群中也观察到了类似的转录变化。MBB增强了两个BAM亚群的功能,但MBB后cBAM的来源被阻断,其数量因无法被补充而逐渐减少,MBB主要通过rBAM发挥作用。机制研究发现,MBB通过扩大rBAM群体和增强其抗原提呈功能发挥作用。
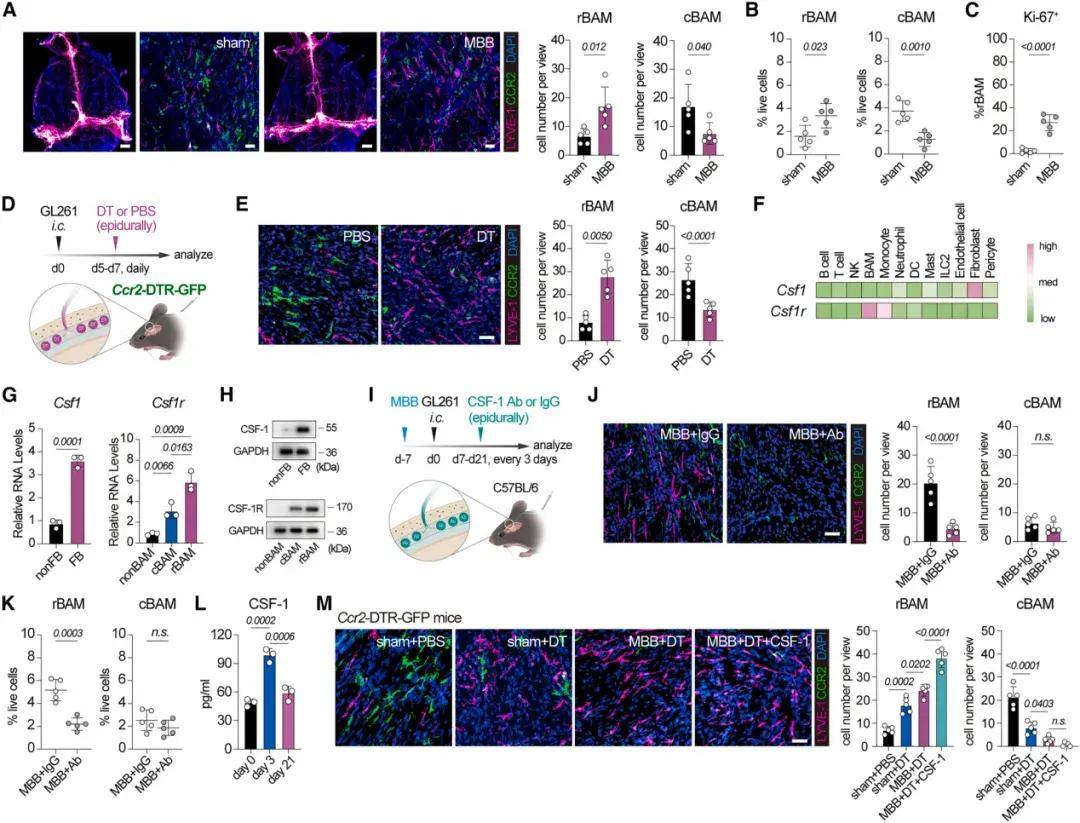 图3. MBB通过限制cBAM对CSF-1的消耗并创造富含CSF-1的微环境来扩展rBAM
图3. MBB通过限制cBAM对CSF-1的消耗并创造富含CSF-1的微环境来扩展rBAM
4、MBB通过硬脑膜-CSF-TME轴增强抗肿瘤T细胞免疫
在中枢神经系统,硬脑膜可以接触含有脑实质衍生抗原的脑脊液和巡逻的T细胞,为直接观察体内抗原摄取过程提供了独特的研究窗口。研究人员通过利用多种体内模型及多光子成像等实验手段,证实硬脑膜rBAM作为关键的抗原呈递细胞,从CSF中捕获肿瘤抗原并将其呈递给巡逻T细胞,从而启动T细胞活化和向TME浸润的级联反应。MBB通过调节rBAM的数量及功能,增强了硬脑膜-CSF-TME轴上的相互作用,从而引发更强的抗肿瘤反应。为了确定rBAM是MBB抗肿瘤效应的主要细胞效应因子,研究人员引入了LYVE1-DTR小鼠。与对照组相比,选择性去除rBAM显著降低了MBB的治疗和免疫刺激作用,表明rBAM是MBB诱导的抗肿瘤免疫反应的必要介质。为了测试BAM-T细胞相互作用的要求,在C57BL/6小鼠体内使用rAAV9-CD206-shCD80/86诱导BAMs中共刺激分子CD80/86的特异性下调,发现MBB的疗效显著减弱。以上发现支持BAMs和T细胞之间的相互作用对于MBB的抗肿瘤作用是必不可少的。
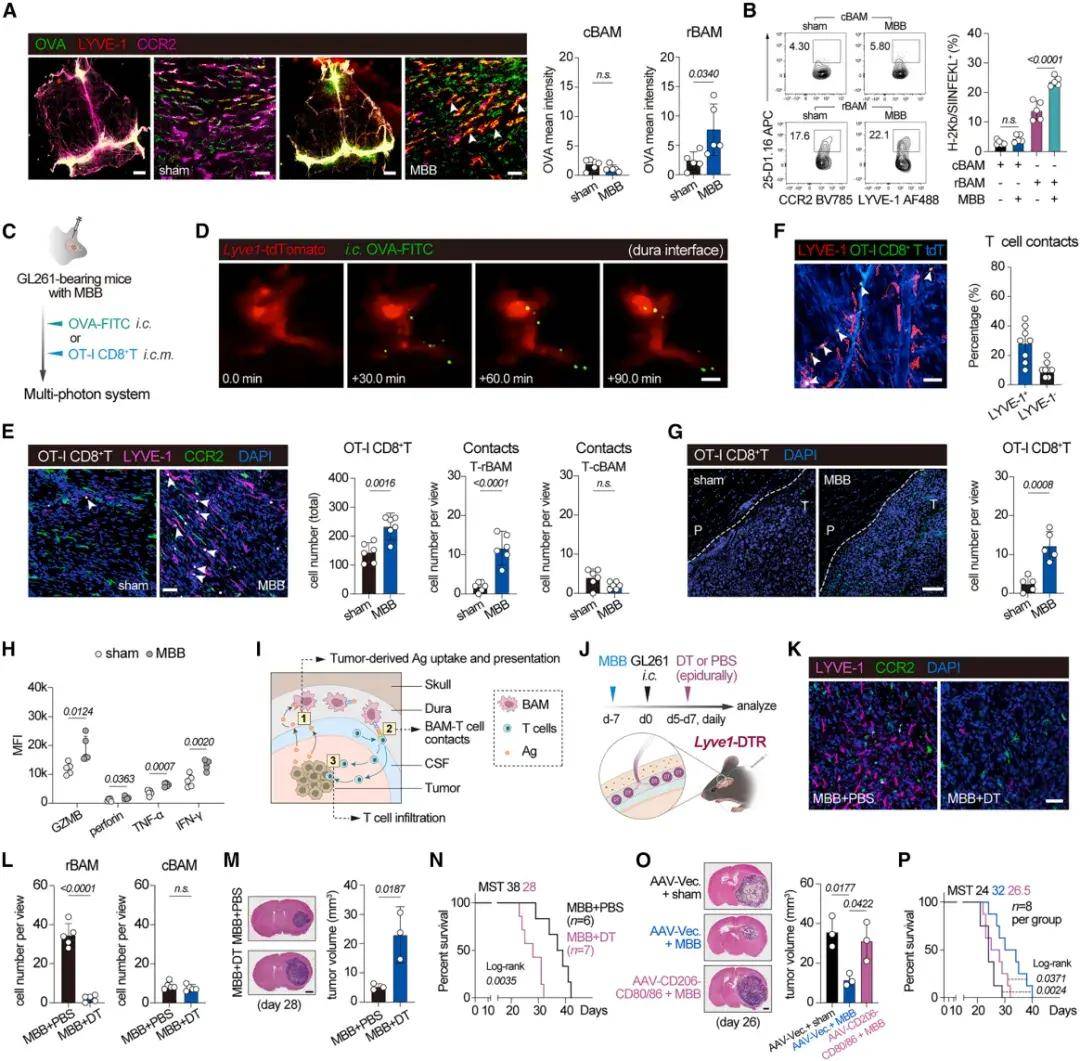 图4. MBB通过硬脑膜-CSF-TME轴增强抗肿瘤T细胞免疫
图4. MBB通过硬脑膜-CSF-TME轴增强抗肿瘤T细胞免疫
结论
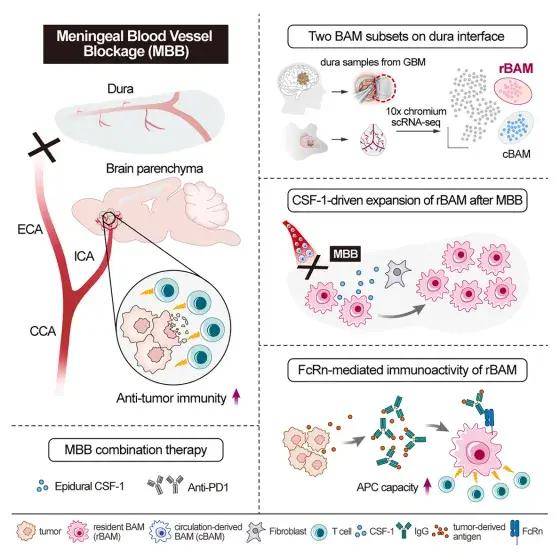
本研究通过揭示硬脑膜作为一个能够影响实质性肿瘤控制的动态免疫界面,扩大了对中枢神经系统肿瘤免疫学的理解。通过将脑膜定位为治疗靶点,这项研究为开发针对中枢神经系统癌症的间隔性免疫疗法开辟了替代途径。

