如何解决AAV 转染实验中由中和抗体引起的效率低
2026-03-16 来源:本站 点击次数:56AAV由于高组织特异性、良好的扩散性、低免疫原性、高安全性和稳定性等特点,已经成为科研和基因治疗中极具市场前景的病毒载体之一。AAV衣壳蛋白种类丰富,其中2型和9型AAV作为基因疗法中的病毒载体研究较多,且已经应用于临床。目前,基于AAV2载体的Luxturna(Spark Therapeutics公司开发,用于治疗Leber先天性黑蒙2型)以及基于AAV9载体的Zolgensma(诺华公司开发,用于治疗脊髓性肌萎缩症)已获批在患者身上使用,并显现出较好的治疗效果。
然而针对AAV衣壳的中和抗体在大多数试验动物和人群中普遍存在,当载体进入血液中时中和抗体可阻断AAV转导。这些中和抗体干扰AAV进入靶细胞,从而导致转基因在靶细胞中的表达减少,并最终降低基因治疗的效率。已有研究表明,即使极低水平(滴度17:1)的NAbs也能完全消除大量病毒载体(2*10E12 vg/kg)。小鼠和非人类灵长类动物的研究表明,1:5滴度的NAbs可以完全阻止肝脏转导。由此可见,体内预存的抗AAV的中和抗体大大限制了AAV的应用。因此,为提高AAV治疗的有效性,提前检测受试者或动物体内是否存在AAV中和抗体十分必要,对临床或临床前试验中AAV血清型的适用性具有指导意义。
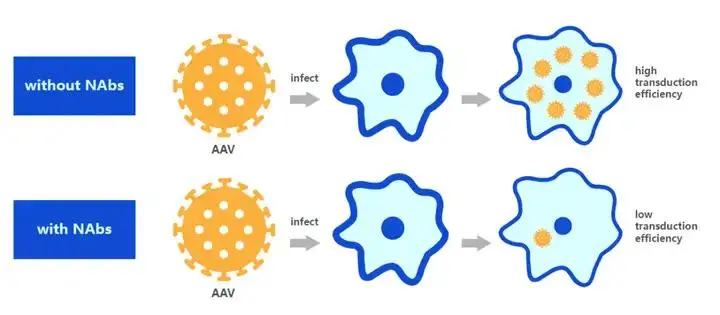 图1. 预存中和抗体大大降低基因转导效率
图1. 预存中和抗体大大降低基因转导效率
为提高AAV治疗的有效性,可提前检测受试者或动物体内是否存在AAV中和抗体。
利用荧光素酶报告系统在体外进行中和抗体的检测,可以检测出受试者体内是否有特定AAV血清型的中和抗体,以方便选择合适的动物模型或血清型,对临床或临床前试验中AAV血清型的适用性具有指导性意义。
通过检测Luciferase发光值RLU,根据发光值计算待检样本中抗AAV病毒的中和抗体是否存在,判断血清/抗体对该血清型的AAV病毒是否具有中和活性。如果受试样品中预存大量抗AAV的中和抗体,那就说明,需要更大剂量的AAV才能起到较好的基因转导效果,那么此种血清型对该动物体来说并非理想选择,需要更换AAV血清型或者动物模型进行下一步的研究或者临床试验。
数据支持
将待测样品按以下梯度进行稀释:30X、60X、120X、240X、 480X、960X,每个梯度取10μL分别与10μL不同血清型的AAV病毒共同孵育,孵育完成后将混合液感染293T细胞,感染24h后用酶标仪检测RLU发光值。综合以上,在血清1:60稀释时,无论AAV2还是AAV9抑制率均能接近100%。
 维真生物现可为您提供AAV1/2/5/6/7/8/9等血清型的中和抗体检测服务,助您选择合适的动物模型和血清型。
维真生物现可为您提供AAV1/2/5/6/7/8/9等血清型的中和抗体检测服务,助您选择合适的动物模型和血清型。

