单细胞测序揭示EGFR突变肺癌耐药机制:线粒体转移搭建肿瘤保命通道
2026-04-15 来源:本站 点击次数:147

期刊:Cancer Research
影响因子:16.6
发表时间:2026年3月
通讯作者:南京医科大学附属肿瘤医院尹荣、刘桐言、谭婧
伯豪生物技术服务:单细胞RNA测序服务
科学问题
EGFR突变型肺腺癌(LUAD)在接受酪氨酸激酶抑制剂(TKI,如奥希替尼,Osimertinib)治疗时,肿瘤细胞如何逃避药物杀伤进入“药物耐受持久性(DTP)”状态?微环境中的特定肿瘤相关成纤维细胞(CAF)如何通过与癌细胞形成物理连接,接收受损细胞器,从而协助癌细胞清除氧化应激并促进肿瘤耐药及复发?
实验材料和方法
患者队列与样本处理:
样本分组:治疗初治的EGFR突变型LUAD患者(n=15),以及奥希替尼耐药复发组织与初治组织对比。
样本类型:手术切除的新鲜组织(用于单细胞测序、原代细胞分离、类器官培养)。
细胞模型:患者来源的类器官(PDO)、原代分离的CAF亚群(RGS5+MYL9+CAFs等)、EGFR突变细胞系(HCC827, PC9)。
多组学数据与功能验证:
单细胞转录组(scRNA-seq):解析EGFR突变LUAD中的成纤维细胞异质性。
转录组测序(Bulk RNA-seq):分析药物耐受persister (DTP)细胞在不同共培养条件下的基因表达差异。
功能实验:
三维类器官共培养药敏测试、线粒体转移示踪(MitoTracker, mitoDsRed)、透射电镜(TEM)、CRISPR/Cas9或shRNA敲低(Miro1, RhoA)、小鼠皮下移植瘤模型及药物干预。
导语
南京医科大学附属肿瘤医院尹荣、刘桐言、谭婧研究团队在 EGFR 突变肺腺癌耐药机制研究中取得重要突破。研究团队借助伯豪生物提供的单细胞转录组测序技术支持,首次在EGFR突变型肺腺癌(LUAD)中鉴定出一类特殊的癌症相关成纤维细胞亚群(RGS5+MYL9+CAFs)。研究发现,这些细胞在TKI药物(如奥希替尼)诱导的压力下,通过隧道纳米管(TNTs)接收来自癌细胞转移的受损线粒体,充当“代谢垃圾桶”,帮助癌细胞清除毒性活性氧(ROS),从而进入休眠耐受状态(DTP)并引发肿瘤复发。该研究不仅揭示了肿瘤细胞与微环境间“代谢共生”的新机制,还证明了联合使用EGFR-TKI与Rho激酶抑制剂(法舒地尔,Fasudil)可有效阻断这一保护路径,显著克服耐药并延缓肿瘤复发,为攻克EGFR-TKI耐药提供了全新靶点与可行方案。

研究结果的示意概述
技术服务
单细胞RNA测序服务
(技术服务伯豪生物提供)
主要研究
1. 单细胞图谱揭示耐药相关的CAF新亚
通过对6例未接受过治疗的EGFR突变LUAD患者样本进行单细胞测序,研究团队绘制了精细的成纤维细胞图谱,鉴定出5个CAF亚群。其中,类器官-CAF共培养显示,RGS5+MYL9+CAFs可显著降低奥希替尼杀伤效果,促进停药后肿瘤快速复发。临床样本分析显示,该亚群在耐药复发组织中的浸润显著增加,且在TCGA数据库中高浸润该亚群的患者生存期更短。
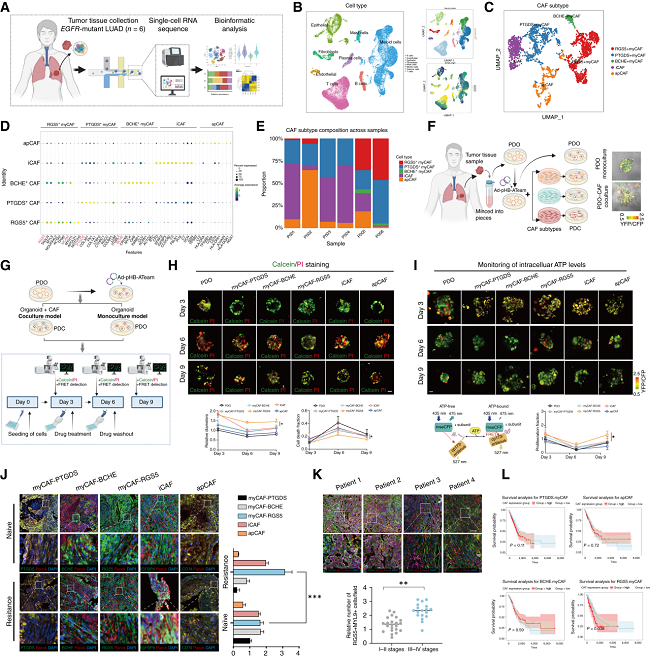
2. RGS5+MYL9+CAFs充当“代谢垃圾桶”,清除癌细胞损伤线粒体
肿瘤细胞是如何在奥希替尼的高压下存活的?研究发现,RGS5+MYL9+CAFs的共培养显著降低了TKI处理下肿瘤细胞的线粒体ROS(mtROS)水平,维持其线粒体膜电位。但RGS5+MYL9+CAFs自身的mtROS水平反而激增,出现线粒体功能障碍。体内小鼠模型同样证实,这群CAF通过“接收”癌细胞的损伤线粒体,帮助肿瘤细胞解毒并维持存活。

图2. RGS5+MYL9+CAFs可缓解EGFR-TKI诱导的线粒体损伤,并促进DTP形成
3. 隧道纳米管(TNT)是线粒体单向转运的核心通道
受损线粒体如何实现跨细胞移动?借助共聚焦显微镜与流式细胞术追踪,研究团队发现,在奥希替尼的处理下,耐药的肿瘤细胞能够生长出由F-肌动蛋白(F-actin)支撑的细长细胞膜突起——隧道纳米管(TNTs),并与RGS5+MYL9+CAFs精准连接。受损(去极化)的线粒体正是沿着该“通道”被输送给CAF。使用细胞松弛素D(阻断肌动蛋白聚合)可直接切断纳米管,完全阻断线粒体的转移,从而恢复肿瘤对TKI的敏感性。

4. mtROS通过激活Miro1和RhoA驱动纳米管的形成
机制探究表明,TKI药物引发的初始mtROS为信号源,上调肿瘤细胞中线粒体Rho GTP酶1(Miro1)的表达,并驱动受损线粒体从核周向细胞膜周缘聚集。同时,mtROS激活关键细胞骨架调节蛋白RhoA。活跃的GTP-RhoA促进了F-肌动蛋白在细胞膜上的局部富集,进而拉伸形成纳米管。敲低Miro1或利用抗氧化剂清除mtROS,均可阻断线粒体转运、逆转肿瘤耐药性。

图4. mtROS上调Miro1以调节DTP细胞受损线粒体的分布

图5. 依赖RhoA的F-肌动蛋白积累介导纳米管的形成和线粒体转移
上述过程共同发挥作用,便可降低癌细胞内的氧化应激,使其转化为药物耐受的慢循环状态(DTP),而接受线粒体的CAF自身则出现线粒体功能受损。
5. 趋化招募:DTP细胞通过CCL11“招兵买马”
ELISA结果显示,处于DTP状态的癌细胞会分泌趋化因子CCL11,特异性招募RGS5+MYL9+CAFs向肿瘤部位迁移(形成极近的空间距离以便于纳米管对接)。空间定位显示:CAF与残留肿瘤细胞紧密接触,形成“耐药保护微环境”。这种“主动招募”机制使得CAF能够及时到达并为癌细胞提供代谢支持。在小鼠模型中,使用CCL11中和抗体可阻断CAF的浸润,显著恢复肿瘤对奥希替尼的敏感性并延缓复发。

图6. DTP细胞通过CCL11分泌招募RGS5+MYL9+CAFs
6. 治疗策略:法舒地尔联合奥希替尼克服耐药、延缓肿瘤复发
基于上述机制,研究团队探索了联合治疗策略。研究人员在动物模型中测试了FDA已批准的Rho激酶抑制剂法舒地尔(Fasudil,已被证明能有效抑制RhoA介导的TNTs形成)与奥希替尼的联合用药。实验结果表明:在人源化小鼠模型中,“奥希替尼+法舒地尔”的联合方案相比单药治疗,显著减少了肿瘤内的CAF互作,增加了癌细胞凋亡,并大幅延长小鼠的生存期。

结论
本研究借助单细胞转录组系统性解析 EGFR 突变肺腺癌 CAF 异质性,首次阐明RGS5+MYL9+ CAF 通过纳米管介导的损伤线粒体转运帮助癌细胞清除氧化应激、形成 DTP 耐药状态的全新机制。研究锁定CCL11、Miro1、RhoA为关键干预靶点,并提出奥希替尼 + 法舒地尔这一极具临床转化潜力的组合疗法,为临床克服 EGFR-TKI 耐药、减少肿瘤复发提供了全新机制与治疗策略。
参考文献:
Liu, Tongyan et al. “Transfer of Damaged Mitochondria from Cancer Cells to Cancer-Associated Fibroblasts Promotes Tyrosine Kinase Inhibitor Tolerance in EGFR-Mutant Lung Cancer.” Cancer research vol. 86,5 (2026): 1215-1231. doi:10.1158/0008-5472.CAN-25-0433

