非侵入性触觉刺激 (TEE) 通过ReExc-BLAInh回路逆转情绪障碍
2026-04-24 来源:MCE (MedChemExpress) 点击次数:69近期,华中科技大学朱铃强、刘丹教授团队在 Neuron 杂志发表了题为“Noninvasive tactile stimulation engaging a thalamic-amygdala circuit ameliorates mood dysfunction in mouse models of depression-like behavior”的研究论文[1]。
高手过招
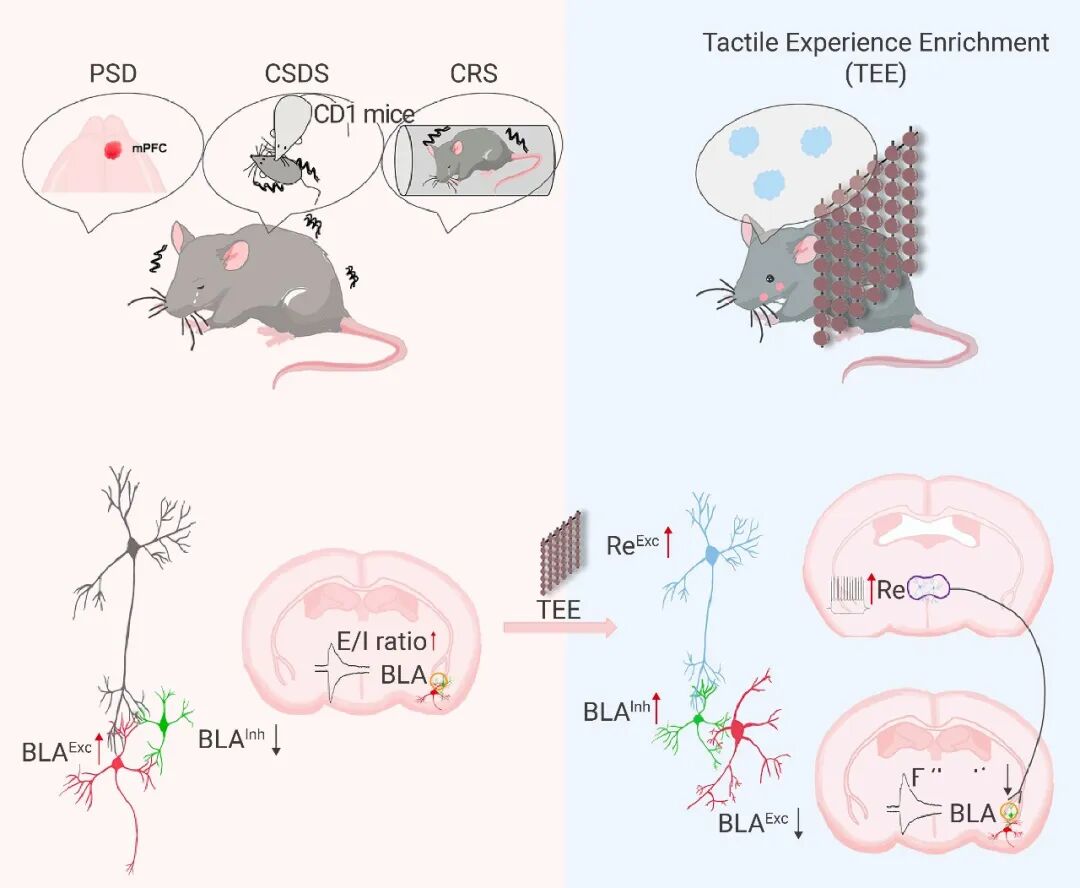
研究人员建立了一种基于触觉的行为范式——触觉体验丰富化 (TEE)——其核心作用是在多种小鼠情绪障碍模型中发挥显著的抗抑郁和抗焦虑效应。
机制研究发现,TEE 并非通过 mPFC 到 BLA 的通路发挥作用 (该通路在疾病中通常受损) 。相反,TEE 绕过了受损的投射,通过激活一条此前未被充分关注的丘脑-杏仁核回路 (ReExc-BLAInh) 实现这一效果。
具体而言,TEE 可激活 Re 核的兴奋性神经元 (ReExc) ,这些神经元进一步驱动基底外侧杏仁核 (BLA) 的抑制性神经元 (BLAInh) ,通过前馈抑制机制降低 BLA 兴奋性神经元的过度激活,从而恢复 BLA 内的兴奋/抑制 (E/I) 平衡。该回路是皮质损伤后情绪调节的一种补偿性且可靶向的通路。即使在皮层完整性受损的情况下,通过化学遗传学方法激活 ReExc-BLAInh 通路也能重现 TEE 的行为效应。
这些发现揭示了一种此前未被认识的的机制,即外周触觉输入如何激活皮层下情感网络,这可能为情绪障碍的干预提供新的回路靶点和非侵入性治疗策略。
Section.01
文献详解
卒中后抑郁 (Post-stroke Depression, PSD) 是脑卒中 (脑中风) 的并发症之一,主要表现为脑卒中后一段时间内出现情绪低落、兴趣减退等抑郁相关症状[2]。
一、实验前造模
首先是模型的建立。将 1 μL 内皮素-1 (ET-1) 注射至小鼠内侧前额叶皮层 (mPFC) (图 1A) 。——通过破坏这一关键情绪调控脑区,诱导小鼠出现持续的抑郁与焦虑样行为。
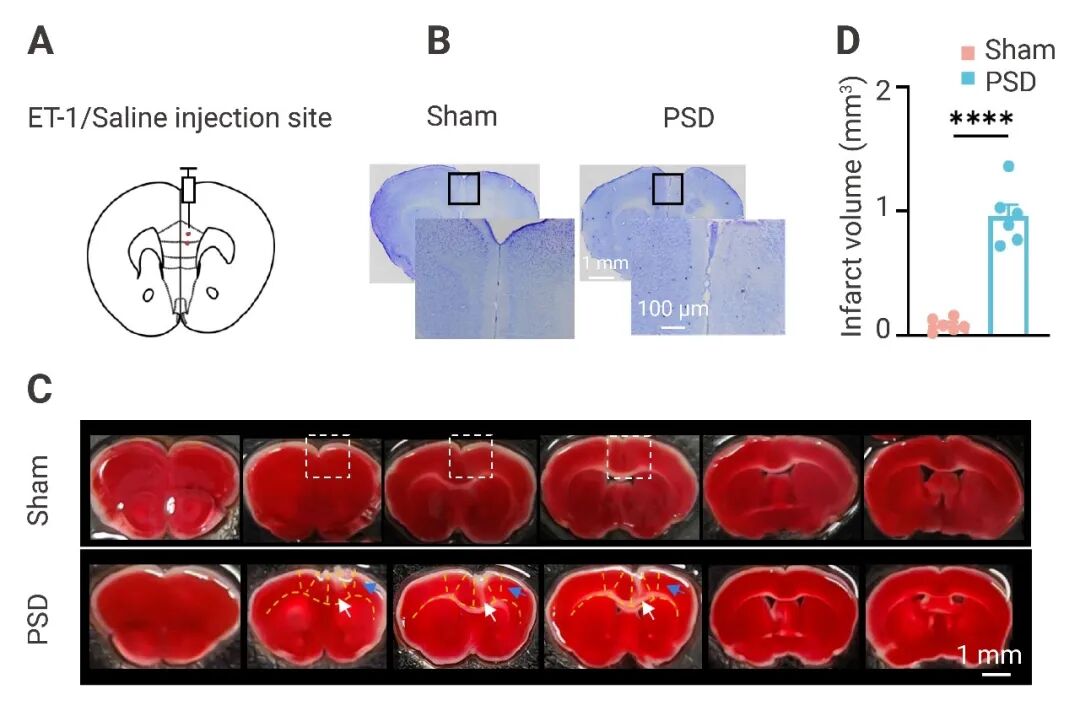 图 1. PSD 小鼠、光化学血栓性丘脑梗死小鼠和光化学血栓性卒中模型小鼠情感障碍的行为表型分析[1]。
图 1. PSD 小鼠、光化学血栓性丘脑梗死小鼠和光化学血栓性卒中模型小鼠情感障碍的行为表型分析[1]。
小鼠 ET-1/生理盐水注射部位示意图。 (B) 代表性图像显示了注射生理盐水 (假手术组) 和 ET-1 (PSD 组) 小鼠 mPFC 区域的甲酚紫 (CV) 染色脑切片。待放大区域以黑色方框标出。 (C) 假手术组和 PSD 组小鼠脑切片经 2,3,5-氯化三苯基四氮唑 (TTC) 染色后的代表性图像。白色虚线框标出了疑似卒中病灶区域。白色和蓝色箭头分别指示前扣带回 (ACC) 和次级运动皮层 (M2) 区域。 (D) 假手术组和 PSD 组小鼠 mPFC 区域梗死体积的定量分析。 (每组 n=6 只小鼠) 。
接着就得确认下咱们的模型是否构建成功。首先,术后 48 小时,注射部位存在局灶性缺血性损伤 (图 1B–D) 。术后 1 周,与对照组相比,PSD 小鼠表现出显著的情感异常。
——这里稍作展开,像研究抑郁症、自闭症、阿尔兹海默症、帕金森等神经相关课题大都会涉及到小鼠的行为学实验。大家如果想了解更多相关内容,举爪投个票,咱们就扯点别的!
表 1. 动物行为学分析类型及实验。
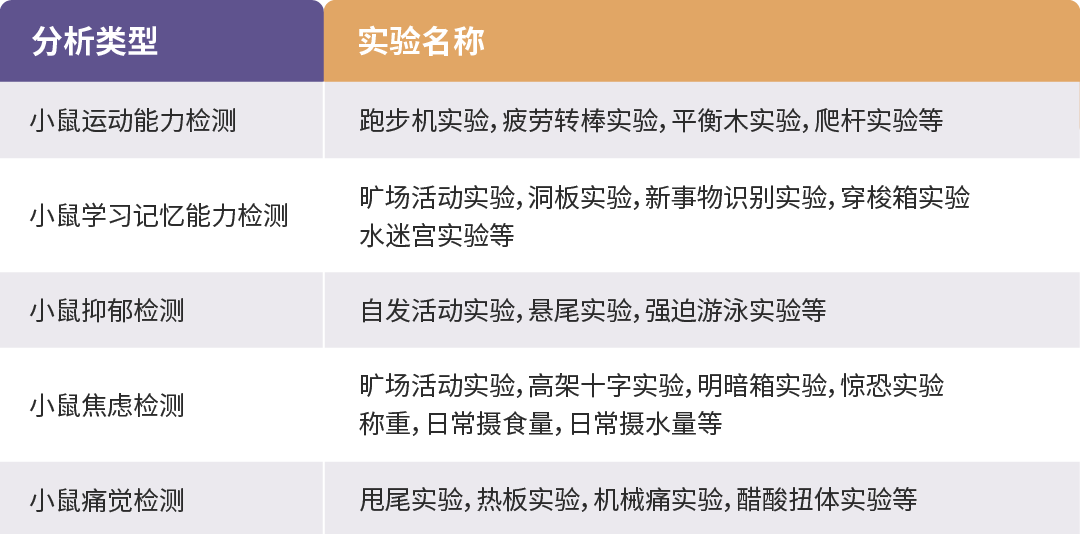
言归正传!PSD 小鼠显著的情感异常具体表现为:旷场实验 (OFTs) 中中心区探索行为减少;高架十字迷宫 (EPMs) 开放臂停留时间与移动距离缩短;强迫游泳试验 (FST) 和悬尾试验 (TST) 中不动时间增加;新奇抑制摄食试验 (NSF) 潜伏期延长;蔗糖偏好试验 (SPT) 中蔗糖偏好度显著降低。重要的是,旷场实验、旋转杆测试及圆柱体评估等测试均未显示整体运动能力或运动协调性存在显著损伤 (图 2) 。
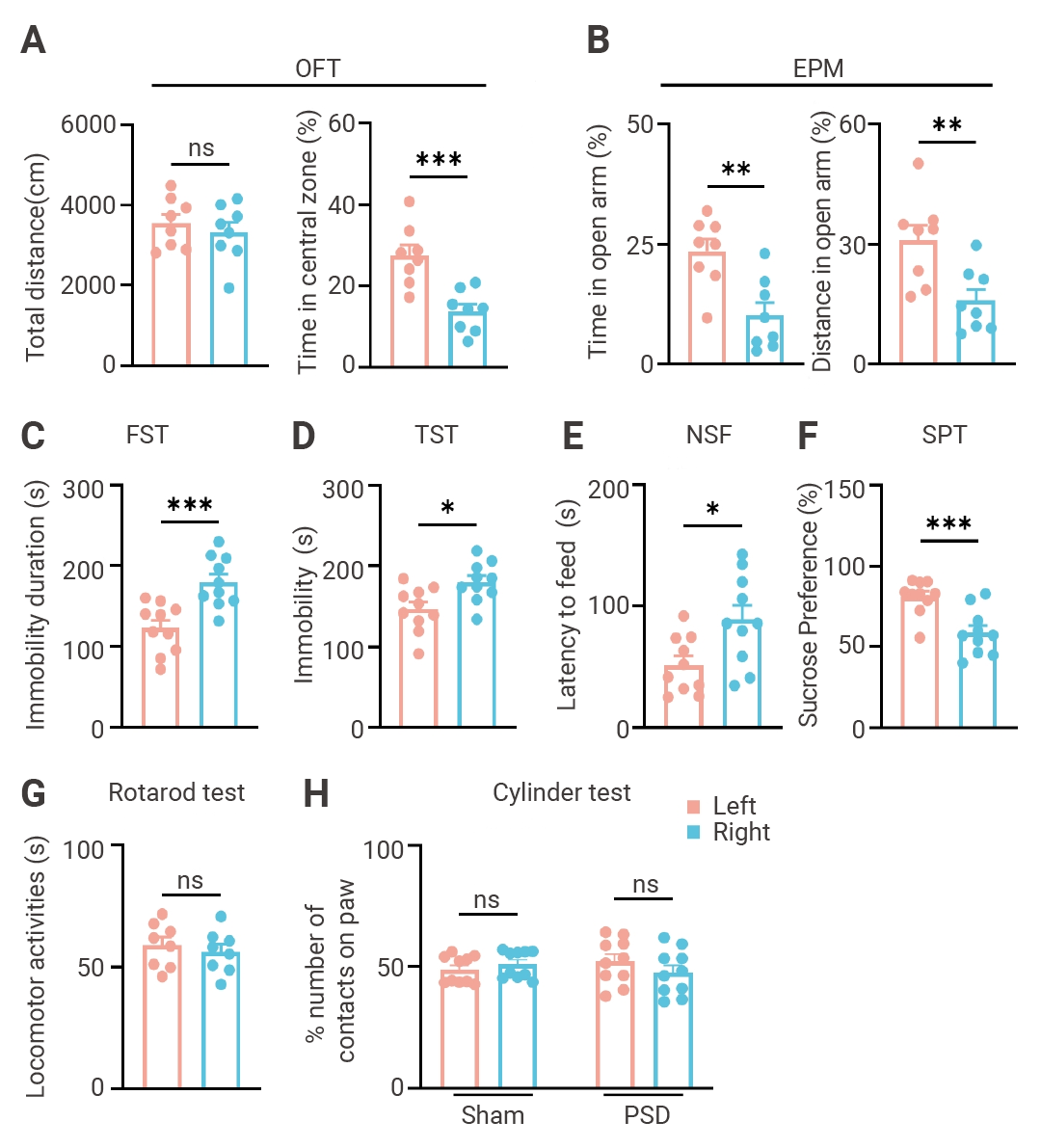 图 2. 术后一周,对假手术组和 PSD 组小鼠进行行为学评估[1]。
图 2. 术后一周,对假手术组和 PSD 组小鼠进行行为学评估[1]。旷场试验 (A) 、高架十字迷宫试验 (B) 、强迫游泳试验 (C) 、悬尾试验 (D) 、神经纤维瘤病试验 (E) 、1% SPT 试验 (F) 、旋转杆试验 (G) 和圆柱试验 (H) 。 (每组 n=8-10 只小鼠) 。
二、实验方案
接下来,实验正式开始!作者探究了一种非侵入性干预手段——触觉刺激。据报道,通过暴露于丰富的环境 (Enriched environment, EE;一种广泛用于行为神经科学和神经生物学研究的实验范式) 对啮齿动物进行多感官刺激,可以增强大脑的可塑性和中风后功能恢复。
为探究其明确的神经机制,研究者设计了一种改进的触觉体验丰富化 (Tactile-enriched experience, TEE) 装置 —— 在实验小鼠的笼子里引入了定制的珠帘,该珠帘由四排塑料珠子组成。小鼠在笼内自由活动或进食时,可以穿过珠帘,使其身体表面接受触觉刺激 (图 1A) 。
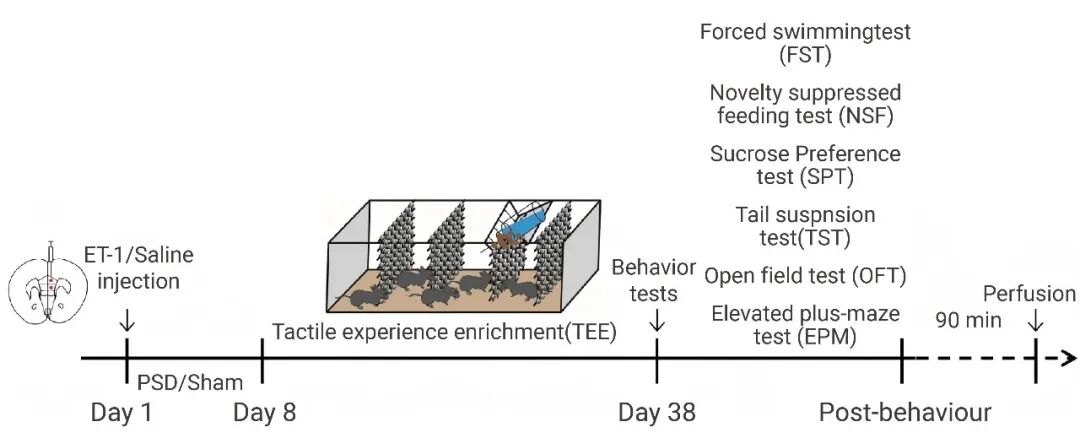 图 3. 实验造模、分组及时间线方案[1]。
图 3. 实验造模、分组及时间线方案[1]。在 PSD 组和对照组 (Sham) 内侧前额叶皮层 (mPFC) 注射 ET-1 或生理盐水 1 周后,小鼠被分为 TEE 亚组 (触觉体验丰富环境) 和 SE 亚组 (标准环境) 。这些亚组随后被安置在独立的笼中。1 个月后,所有小鼠均接受行为学测试及后续实验。
这种 TEE 饲养环境维持一个多月,直至实验结束。期间每周清洁珠帘并更换垫料,以确保清洁卫生。相比之下,对照组小鼠则饲养在标准环境条件下。当然,为了大家迷糊,对本文的实验分组做简要梳理,大家可随时查看。
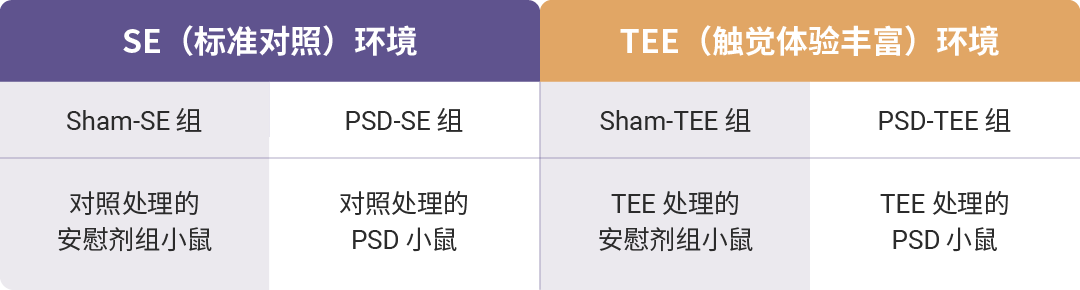
三、TEE 处理:缓解 PSD 小鼠抑郁、焦虑行为
行为学结果显示,经过 TEE 干预后,PSD 小鼠在强迫游泳、悬尾测试中的绝望行为显著减少,在蔗糖偏好测试中的快感缺失逆转为对蔗糖偏好度增加。此外,旷场实验和高架十字迷宫实验显示,PSD 小鼠焦虑水平降低或探索行为增加。证明丰富的触觉刺激具有抗抑郁效应。
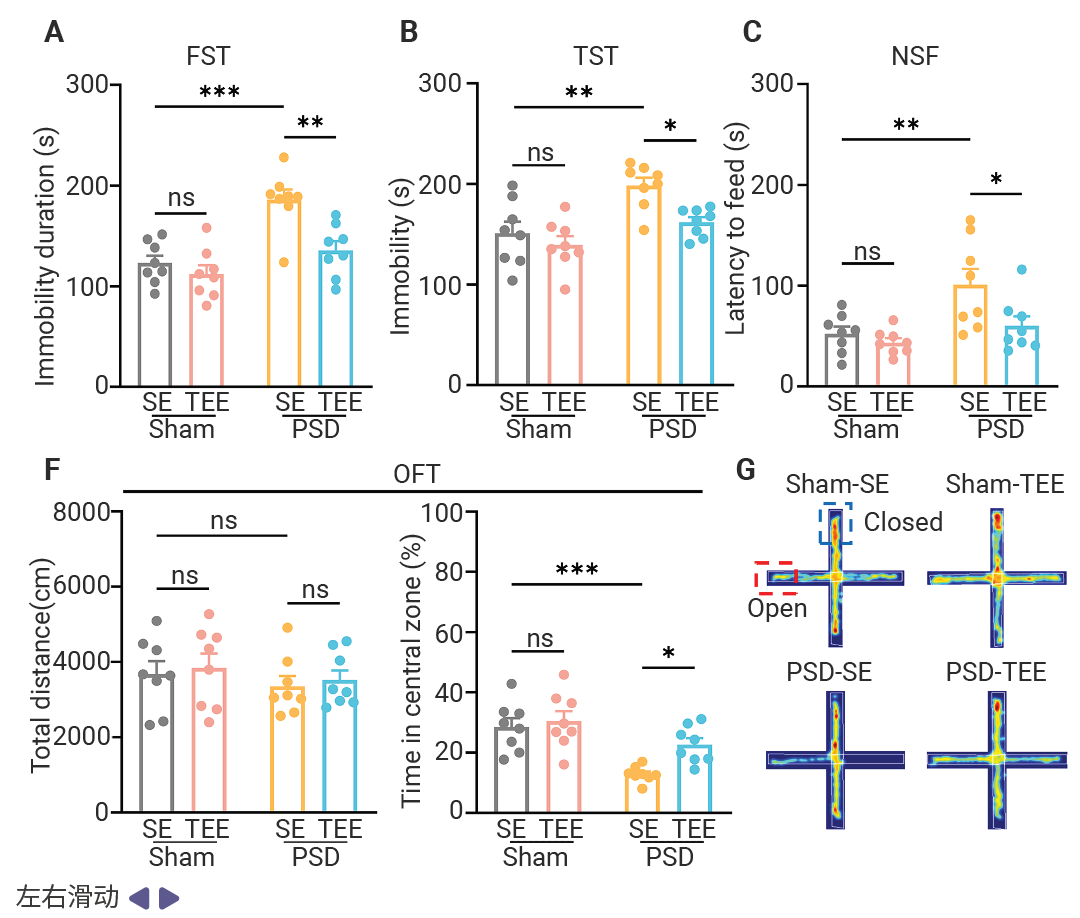
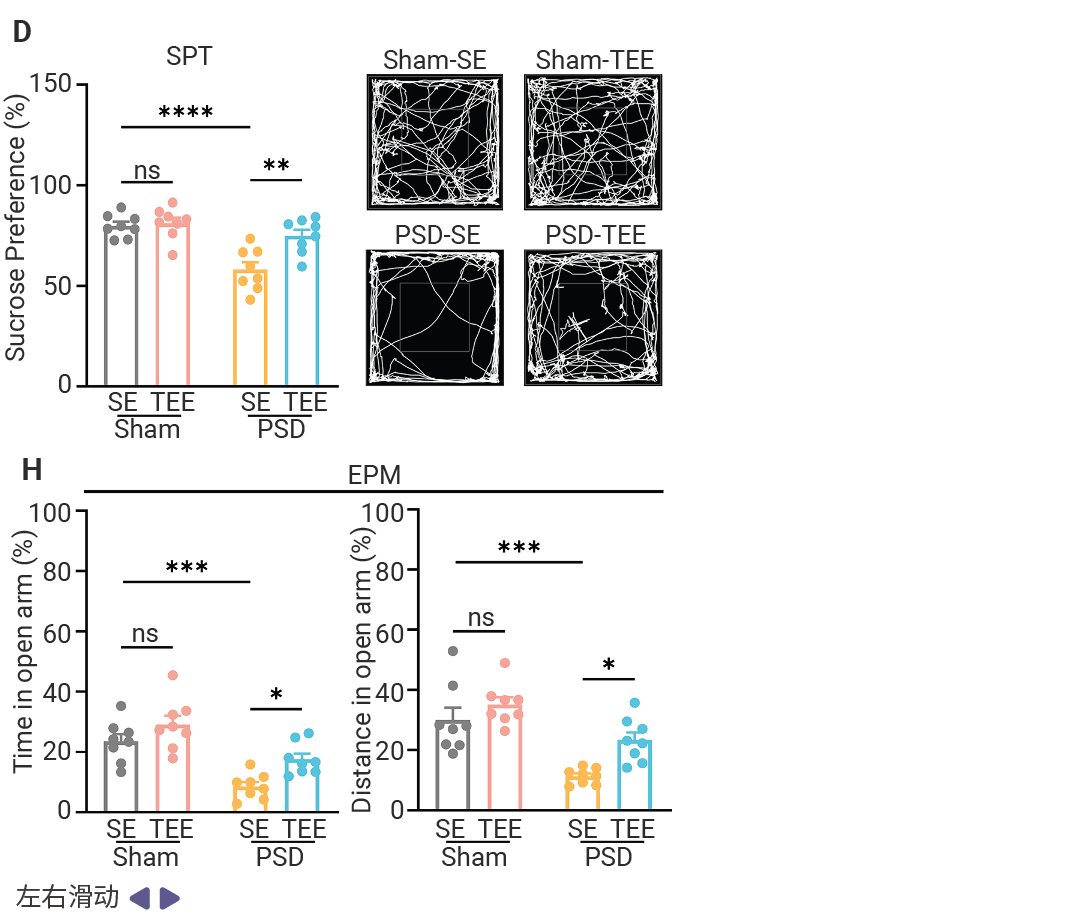
图 4. TEE 处理缓解 PSD 小鼠抑郁样及焦虑样行为[1]。
(A-D) 对 Sham-SE、Sham-TEE、PSD-SE 和 PSD-TEE 小鼠进行了行为学评估,包括强迫游泳试验 (FST) (A) 、悬尾试验 (TST) (B) 、新奇抑制进食试验 (NSF) (C) 和 1% 蔗糖偏好试验 (SPT) (D) 每组 n=8 只小鼠。 (E 和 F) 进行了旷场试验 (OFT) 行为学评估。 (E) 不同组小鼠在 OFT 中的代表性运动轨迹。 (F) 左图显示总运动距离,右图显示不同组小鼠在 OFT 中于中心区域停留的时间 (每组 n=8 只小鼠) 。 (G 和 H) 进行了高架十字迷宫试验 (EPM) 行为学评估。 (G) 不同组小鼠在 EPM 中的代表性运动轨迹热图。红色和蓝色矩形分别表示高架十字迷宫装置的开放臂和封闭臂。(H) 左图显示不同组小鼠在开放臂中停留时间的百分比,右图显示不同组小鼠在开放臂中行进距离的百分比。每组小鼠数量为 n = 8 只。
四、旁路机制:ReExc-BLAInh 回路
在机制探究上,研究人员利用体内电生理的全细胞膜片钳技术证实了 PSD 小鼠 BLA 中存在兴奋性/抑制 (E/I) 失衡(兴奋性神经元群体:Exc;抑制性神经元群体:Inh) 。TEE 处理可恢复 PSD 小鼠 BLA 中受损的突触及内在电生理平衡,从而纠正与抑郁和焦虑表型相关的潜在 E/I 失衡。
具体而言,在体内电生理记录中,与 Sham-SE 组相比,PSD-SE 组小鼠兴奋性神经元 (BLAExc ) 的放电频率显著增加,同时抑制性神经元 (BLAInh) 的放电频率明显降低 (图 5) 。TEE 处理可恢复 PSD 小鼠 BLA 中内在电生理平衡。
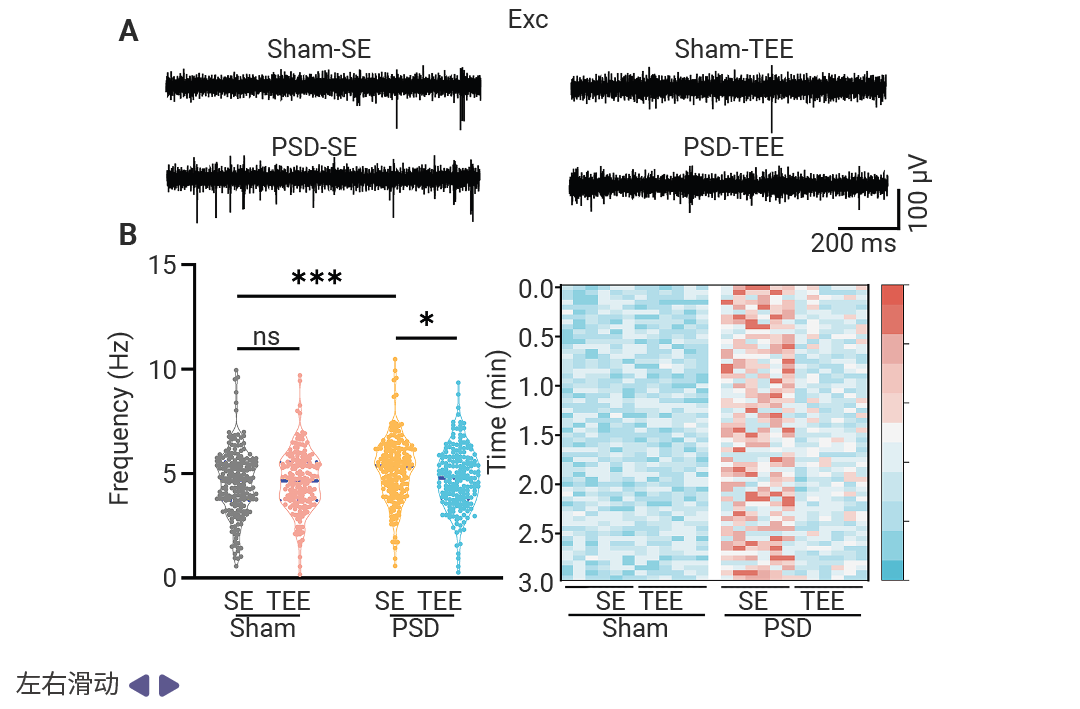
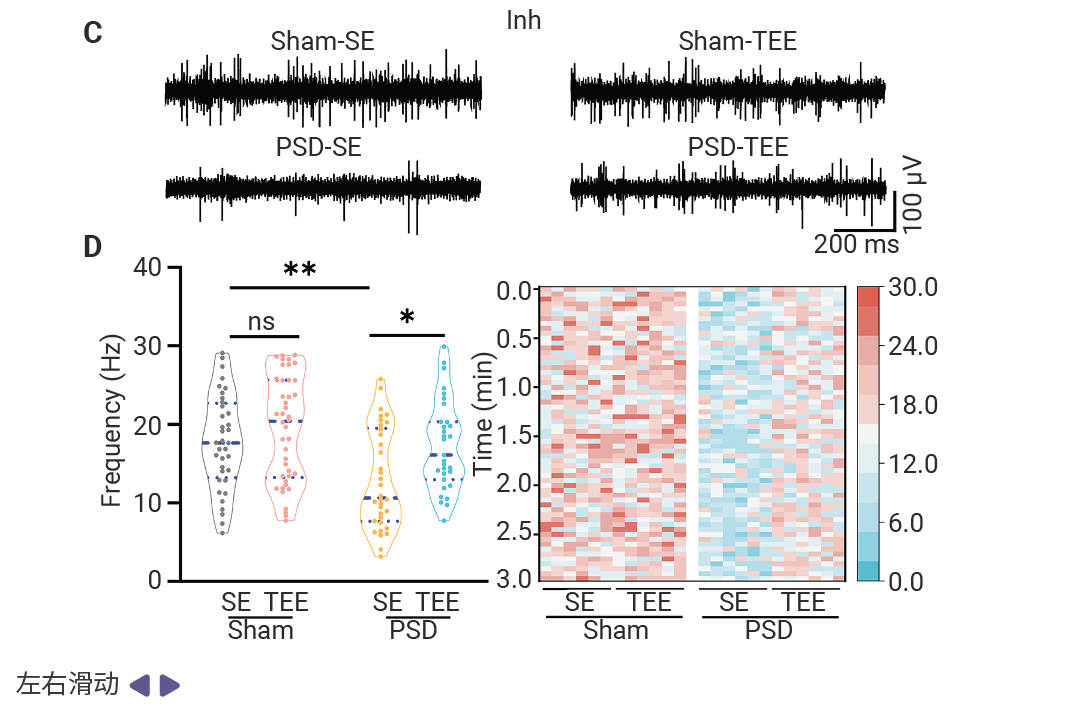
图 5. 对不同组小鼠的 BLAExc 神经元和 BLAInh 神经元进行体内电生理记录。
(A) BLAExc 神经元的代表性记录曲线。 (B) 左图:BLAExc 神经元的脉冲放电定量分析 (每组 8 至 10 只小鼠,共 193 至 210 个细胞) 。右图:描绘 BLAExc 神经元 3 分钟脉冲放电动态的热图 (每组 6 只小鼠,共 4 组) 。 (C) BLAInh 神经元的代表性记录曲线。 (D) 左图:BLAInh 神经元的脉冲放电定量分析 (每组 8 至 10 只小鼠,共 31 至 42 个细胞) 。右图:描绘 BLAInh 神经元 3 分钟脉冲放电动态的热图 (每组 6 只小鼠,共 4 组) 。
全细胞膜片钳记录结果显示,在 PSD-SE 小鼠中,BLA 神经元表现出自发性兴奋性突触后电流 (sEPSC) 频率和幅度升高 (图 6A–C) ,而 BLA 神经元的 sEPSC 参数降低 (图 6D–F) 。TEE 治疗显著逆转了这些改变,使两个神经元群体的突触活动恢复正常 (图 6) 。
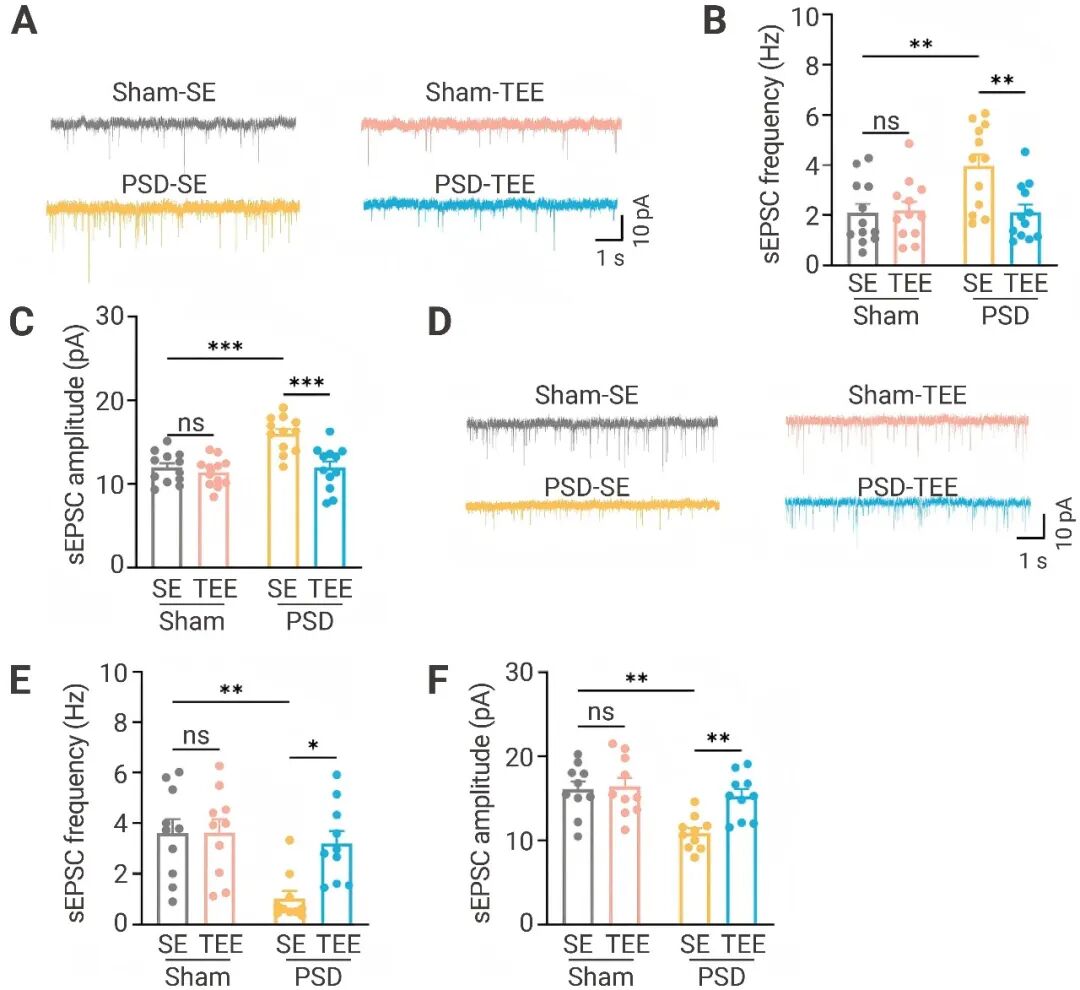 图 6. 对不同组小鼠的 BLAExc 神经元和 BLAInh 神经元进行全细胞膜片钳记录[1]。
图 6. 对不同组小鼠的 BLAExc 神经元和 BLAInh 神经元进行全细胞膜片钳记录[1]。(A-C) 代表曲线 (A) 以及来自不同组小鼠的 BLAExc 神经元的 sEPSC 频率 (B) 和振幅 (C) 的统计分析。每组有 5 - 6 只小鼠,共 12 个细胞。 (D-F) 代表曲线 (D) 以及来自不同组小鼠的 BLAInh 神经元的 sEPSC 频率 (E) 和振幅 (F) 的统计分析。每组有 5 - 6 只小鼠,共 10 个细胞。
进一步地,通过光遗传学与跨脑区病毒示踪技术,研究人员发现 TEE 介导的 PSD 小鼠 BLA 中 E/I 平衡恢复并不依赖于 mPFC-BLA 环路。
而是:ReExc 神经元主要与 BLAInh 神经元建立直接谷氨酸能突触,进而对 BLAExc 神经元产生前馈抑制作用。
具体而言,研究发现 TEE 显著增加了多个脑区的 c-FOS 神经元数量,其中,仅 Re 与 BLA 存在解剖学连接。并且 Re 神经元与 BLA 神经元间建立的是强单突触谷氨酸能连接。TEE 处理增强了 Re 中 CaMKII 阳性兴奋性神经元的活性,这些 ReExc 神经元投射至 BLAInh 神经元并激活它们,从而间接抑制过度活跃的 BLAExc 神经元,恢复兴奋/抑制稳态。
注:CaMKIIα 是脑谷氨酸能神经元特异性的兴奋性标志物,常被用作标记和操纵大脑谷氨酸能投射 (兴奋性回路)的工具。
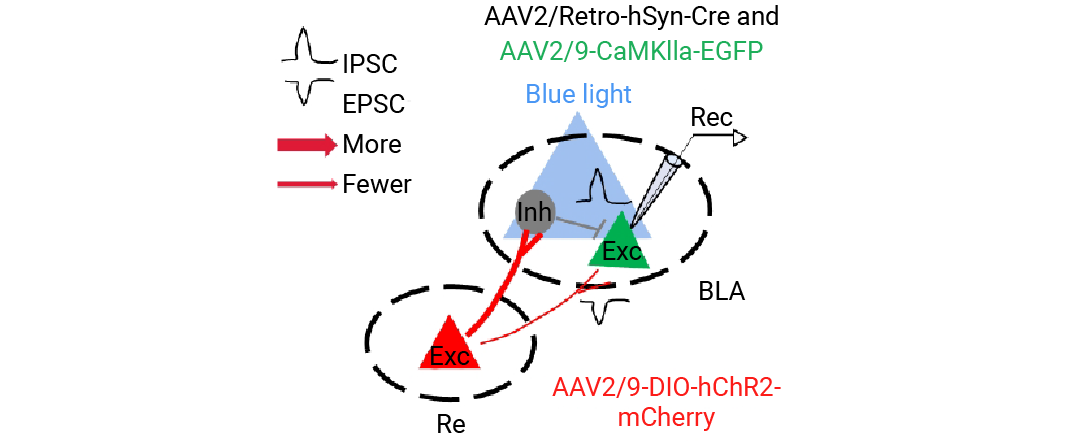 图 7. 在光遗传学激活 ReExc-BLAInh 神经元 (ReExc 神经元为红色,BLAInh 神经元为灰色) 的过程中,BLAExc 神经元 (绿色) 的病毒注射及电生理记录情况[1]。
图 7. 在光遗传学激活 ReExc-BLAInh 神经元 (ReExc 神经元为红色,BLAInh 神经元为灰色) 的过程中,BLAExc 神经元 (绿色) 的病毒注射及电生理记录情况[1]。
“前馈抑制”
对于“前馈抑制”,有些迷糊的小伙伴可以简单理解为在激活 A 的同时,抑制 B。例如,膝跳反射中的前馈抑制就是如此。伸肌在受到刺激而收缩时,屈肌会收到抑制信号。由于伸肌和屈肌在功能上相互拮抗,所以当一组肌肉收缩时,另一组肌肉通常处于抑制状态,这也就是“激活 A 的同时,抑制 B”。这种结构能使目标细胞的兴奋过程被严格限制在极短的时间内,避免过度激活,进而调节传入兴奋信号的幅度和持续时间。
Section.02
小结
总之,该研究首次明确 ReExc-BLAInh 回路通过前馈抑制调节基底外侧杏仁核 (BLA) 的兴奋/抑制 (E/I) 平衡,而非依赖受损的皮质通路 (如 mPFC-BLA) ,为情绪障碍提供了“旁路代偿”的新机制。同时,在卒中后抑郁 (PSD) 、慢性社交挫败应激 (CSDS) 、慢性束缚应激 (CRS) 等多种模型中均能通过激活该通路改善抑郁和焦虑样行为,表明其对不同病因的情绪障碍具有广谱调节作用。此外,非侵入性触觉刺激 (TEE) 可通过激活该通路发挥疗效,提示其可能成为情绪障碍的非药物干预靶点,为临床转化提供了新思路。
产品推荐
CaMKIIα-PHOTAC 是一种光化学靶向嵌合体 (PHOTAC),靶向 Ca2+/钙调蛋白依赖性蛋白激酶 II α (CaMKIIα)。PHOTAC 这类分子能够在特定波长的光照下,通过内源蛋白酶体催化靶蛋白的泛素化和降解。CaMKIIα-PHOTAC 可降低降低突触功能,对维持亚细胞树突结构域的长时程增强和记忆能力具有关键作用。
Clozapine N-oxide 是 Clozapine 的主要代谢产物,也是一种人毒蕈碱设计受体 (DREADDs) 激动剂,不能穿过血脑屏障。Clozapine 还是一种有效的多巴胺拮抗剂和选择性毒蕈碱 M4 受体 (EC50 为 11 nM) 激动剂。
Endothelin 1 (swine, human) (HY-P0202)
Endothelin 1 (swine, human) 是具有人和猪内皮素 1 序列的合成肽,是有效的内源性血管收缩剂。Endothelin 1 通过两种类型受体 ETA 和 ETB 发挥作用。
参考文献
[1]Fan HW, et al. Noninvasive tactile stimulation engaging a thalamic-amygdala circuit ameliorates mood dysfunction in mouse models of depression-like behavior. Neuron. 2026 Apr 1:S0896-6273(26)00176-5.
[2]刘畅, 仝利俊. 卒中后抑郁的发病机制和治疗研究进展[J]. 临床医学进展, 2024, 14(12): 1281-1286.


