TRPV4拮抗剂抑制小鼠心肌缺血再灌注后的抗心律失常作用及潜在机制
2025-04-29 来源:本站 点击次数:556急性心肌梗死(MI)是致死的主要原因之一。再灌注治疗可以挽救缺血组织,但同时它可能会造成额外损伤,引发室性心律失常(VA)进而导致心源性猝死。目前需要新的治疗策略治疗IR损伤,并预防心肌梗死后的室性心律失常。
TRPV4是一种非特异性阳离子通道,主要通透钙离子(Ca2+)。研究证实TRPV4在心肌缺血再灌注期间表达水平会上调。在动物缺血再灌注/心肌梗死模型中,阻断TRPV4可改善心脏功能并提高存活率,在人体中该操作安全且耐受性良好。然而,尽管已知TRPV4对心脏有益,但抑制TRPV4针对心肌缺血再灌注损伤的抗心律失常作用仍未得到充分研究。
在缺血再灌注后,TRPV4的激活可能会促进老年小鼠心脏发生室性心律失常,而抑制TRPV4可减轻无菌性心包炎大鼠的心房重构并逆转钙稳态失衡。钙稳态在室性心律失常的早期后除极和延迟后除极的产生过程中起着重要作用。钙稳态失衡也可能引发心脏交替现象,进而引发室性心律失常。
基于此,华中科技大学同济医学院附属协和医院杜以梅教授团队在Heart Rhythm杂志发表重要研究成果:TRPV4 inhibition suppresses myocardial ischemic-reperfusion arrhythmia of mice by alleviating calcium handling abnormalities,使用TRPV4拮抗剂GSK2193874(GSK219)和TRPV4基因敲除(TRPV4-/-)小鼠,评估抑制TRPV4在缺血再灌注后的抗心律失常作用及其潜在机制。

1. TRPV4抑制降低了IR诱导的VA的易感性
研究通过药理学和遗传学方法探究TRPV4在心律失常中的作用,缺血再灌注早期心电图显示多种室性心律失常,包括室性期前收缩和室性心动过速(VT),未观察到室颤,着重分析室性心动过速的发生率和持续时间。
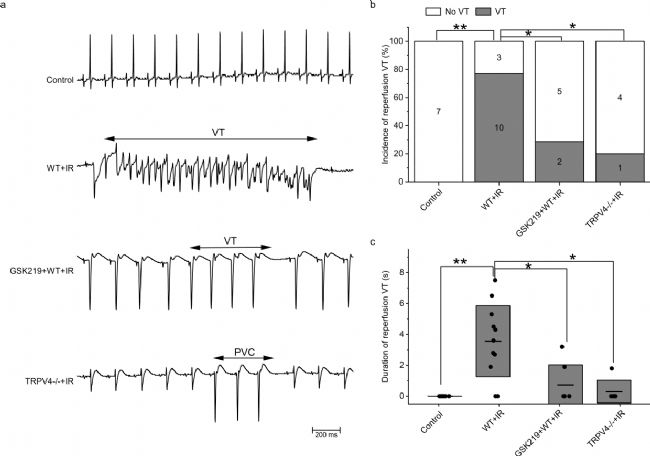
图1. TRPV4的抑制作用在体外可降低IR诱导的VA
2. 抑制TRPV4对IR离体心脏动作电位(AP)和钙瞬变(CaT)的影响
研究发现缺血再灌注10分钟后各组动作电位达到峰值时间和APD均延长、传导速度下降,但组间无显著差异,有效不应期无变化;7Hz起搏下各组钙瞬变的上升时间和CaD80在对照水平和再灌注后组间均无显著差异;总体说明缺血再灌注导致电生理紊乱,抑制TRPV4不能减轻这些紊乱。
3. 抑制TRPV4对IR离体心脏的心脏交替现象的影响
通过增加起搏频率诱发心脏交替现象,发现再灌注后10分钟APD交替增加,GSK219预处理和TRPV4基因敲除预处理不影响IR诱导的APD交替易感性;CaT交替方面,不同起搏频率下有不同表现,IR增加CaT交替、降低交替阈值,而GSK219预处理和TRPV4基因敲除预处理可抑制IR诱导的CaT交替并降低不一致交替现象发生率,说明抑制TRPV4能抑制CaT交替但不能抑制APD交替。
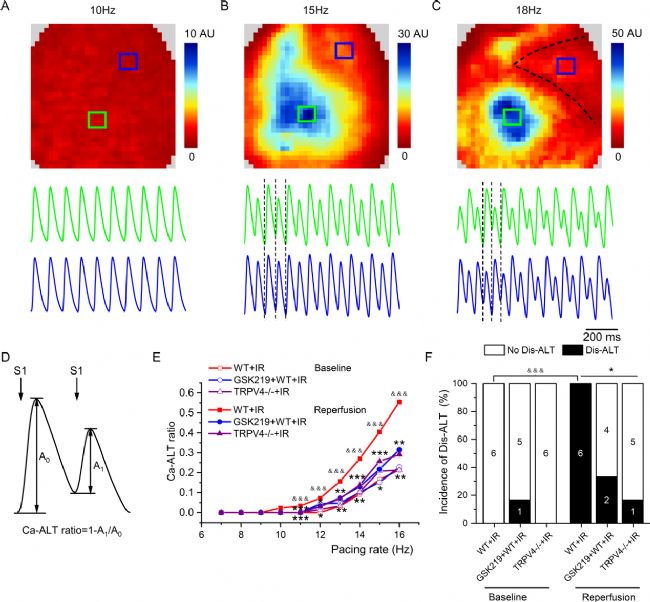
图2. TRPV4的抑制可减少心脏中由IR所诱导产生的钙瞬变交替及不一致性交替现象
4. 抑制TRPV4可改善去极化诱导的CaT恢复,并抑制IR离体心脏中由缺血再灌注所诱导的钙泄漏
本文研究了TRPV4抑制对钙瞬变(CaT)的影响。通过S1S2方案发现,野生型心脏再灌注后CaT恢复比率降低且变异系数增加,而GSK219预处理或TRPV4基因敲除可阻止这些变化。此外,分离心室肌细胞并利用高分辨率激光共聚焦显微镜测量发现,TRPV4抑制能显著抑制缺血再灌注诱导的钙火花(钙火花代表了通常被称为钙泄漏的自发钙释放事件),揭示了TRPV4抑制对心脏保护作用的相关机制。
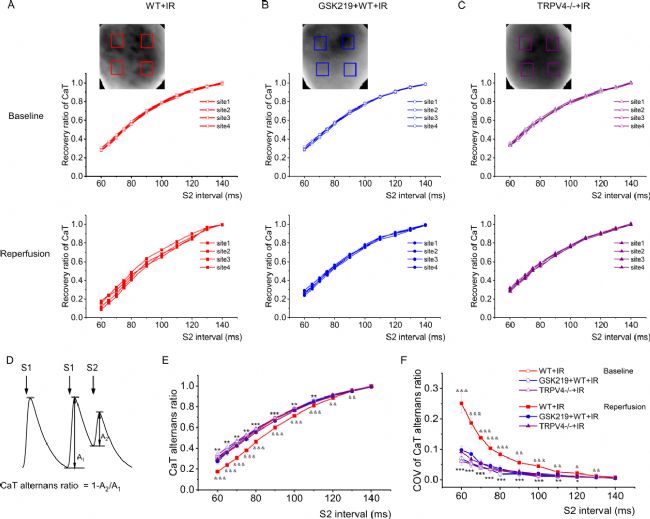
图3.TRPV4抑制对IR离体心脏CaT恢复的影响
5. TRPV4抑制对钙离子(Ca²⁺)稳态相关蛋白表达的影响
该研究旨在探究钙离子稳态失衡的分子基础,通过western blot检测相关蛋白。结果显示,TRPV4抑制(药物或基因方法)能在缺血再灌注后降低苏氨酸286(Thr286)磷酸化的钙调蛋白激酶II(CaMKII)(丝氨酸2814)及其磷酸化比率,但不改变总CaMKII水平;同时降低兰尼碱受体2(RyR2)(Ser2814)和肌浆网磷蛋白PLB(苏氨酸-17(Thr-17))的磷酸化水平,而总RyR2、Ser2804磷酸化的RyR2、总PLB、NCX1和肌质网/内质网钙ATP酶2a(SERCA2a)的水平在TRPV4抑制及缺血再灌注后均无变化。
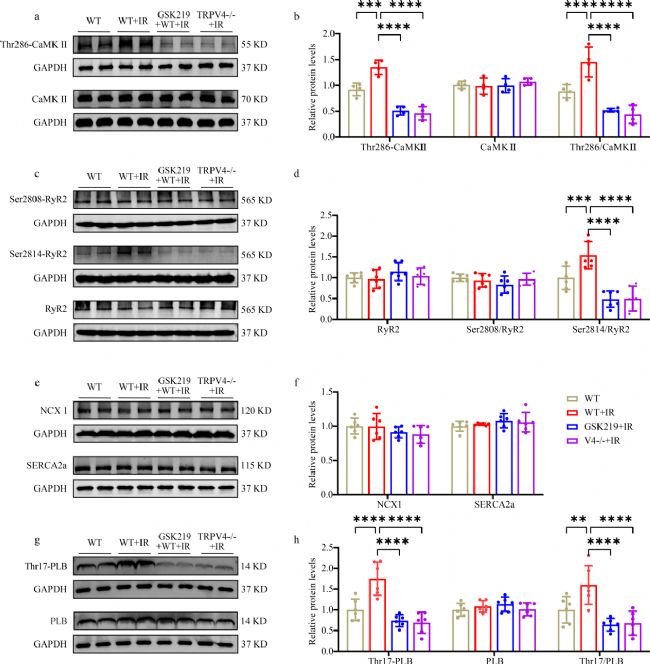
图4.TRPV4抑制对IR离体心脏中Ca2+稳态相关蛋白的影响
6. TRPV4的激活增加了离体心脏对VA的敏感性
探究TRPV4激活对室性心律失常易感性的影响。通过将TRPV4激动剂GSK101灌注到小鼠离体心脏并记录心电图和动作电位,S1S2刺激可诱发室性心律失常。处理前无室性心律失常,GSK101使野生型心脏中室性心律失常发生率显著高于灌注DMSO的对照组。此外,GSK101会延长动作电位除极时间、动作电位时程、降低传导速度、增加特定起搏频率下的动作电位时程交替现象,但不影响有效不应期。
该部分研究了TRPV4激动剂GSK101对钙瞬变相关指标的影响。结果表明,GSK101能延长钙瞬变达峰时间和CaD80,在特定起搏频率下增加钙瞬变交替比率和不一致性钙瞬变交替发生率;延长RyR2不应期,降低钙瞬变恢复比率并增加恢复比率变异系数;增加舒张期钙火花的幅度和频率;还能增加CaMKII(Thr286)、Ser2814磷酸化的RyR2和Thr17磷酸化的PLB的水平,但不改变相关蛋白的总量。而这些由GSK101诱导的效应在TRPV4基因敲除的心脏中不存在,证明了TRPV4介导了GSK101对室性心律失常、钙瞬变交替和钙离子稳态失衡的促进作用。
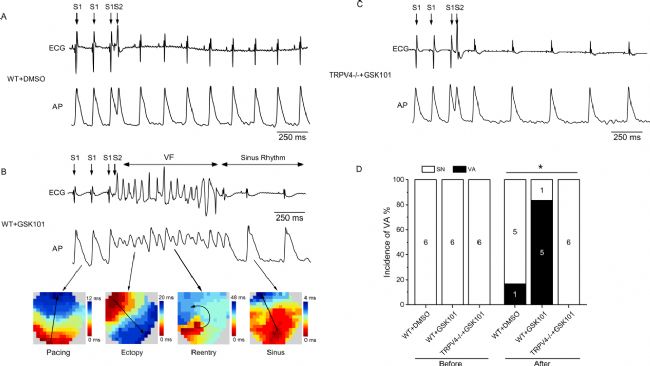
图5. 灌注GSK101会增加离体心脏VA的发生率
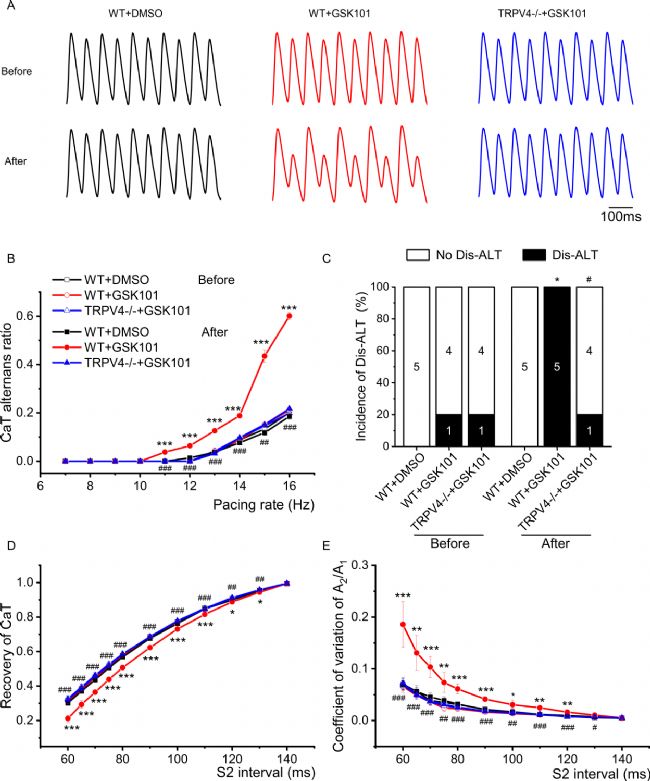
图6. GSK101对心脏中钙瞬变(CaT)交替、不一致性交替以及钙瞬变(CaT)恢复的影响
7. CaMKII抑制可防止GSK101引起的钙稳态失衡
探究CaMKII的增强激活是否与GSK101诱导的钙离子处理异常有关。通过使用CaMKII特异性抑制剂KN93及其无活性类似物KN92进行实验,发现KN93可阻止由GSK101引起的钙瞬变达峰时间和CaD80的增加,还能阻断GSK101对钙瞬变交替比率、不一致性钙瞬变交替发生率、RyR2不应期及其离散度的增加作用。同时,KN93处理显著降低了Thr286磷酸化的CaMKII、Ser2814磷酸化的RyR2和Thr17磷酸化的PLB的水平。
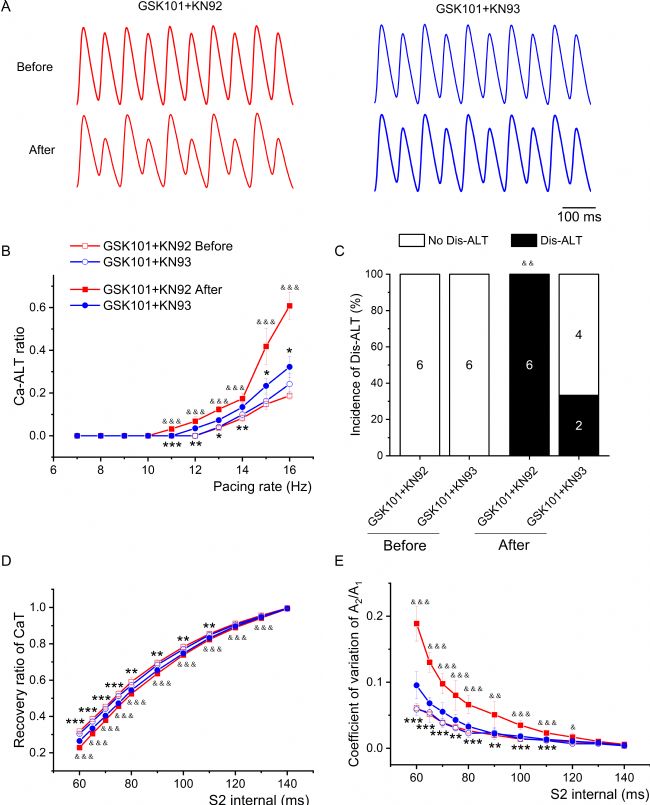
图7. CaMKII抑制剂可抑制在暴露于GSK101的离体心脏中出现的钙瞬变(CaT)交替变化,并改善RyR2的不应性
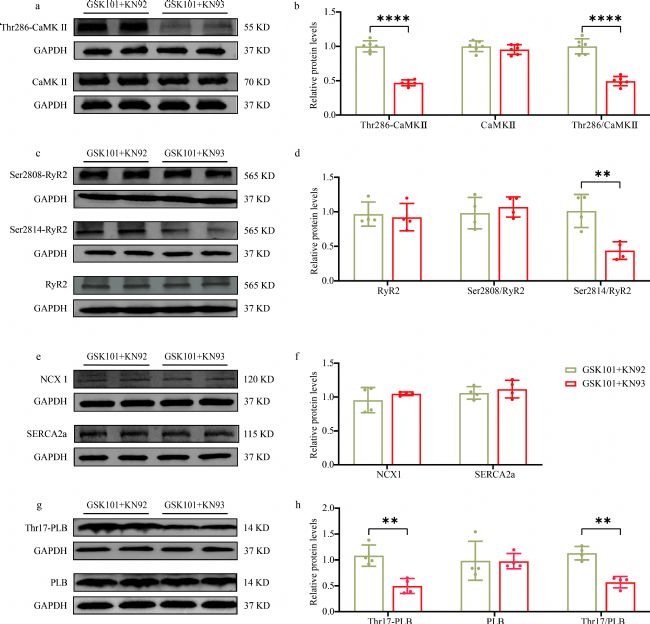
图8. CaMKII抑制剂可抑制由GSK101诱导的钙调控相关蛋白的变化

