血栓四项(TAT/PIC/TM/tPAI·C)的生物学功能、临床价值及应用场景
2025-05-20 来源:本站 点击次数:184一、血栓四项的生物学角色与临床价值
1. TAT(凝血酶-抗凝血酶复合物)
核心功能:直接反映凝血酶活性,标志凝血系统激活的起始阶段。
临床意义:
DIC诊断:在弥散性血管内凝血(DIC)中,TAT水平显著升高。日本指南明确将“TAT≥20 μg/L且PIC≥10 μg/mL”作为纤溶优势型DIC的诊断标准。
感染与肿瘤:感染性疾病患者若TAT<7 ng/mL,DIC风险较低;恶性肿瘤患者TAT与D二聚体同步升高,提示VTE高风险。
溶栓监测:动脉血栓溶栓后24-72小时,TAT先升后降,若治疗后36小时反弹,预示再梗死风险。
2. PIC(纤溶酶-α2纤溶酶抑制物复合物)
核心功能:量化纤溶酶活性,标志纤溶系统激活程度。
临床意义:
脑卒中管理:阿替普酶溶栓后,PIC在3小时达峰并快速衰减,较D二聚体提前3小时反映纤溶状态,对急性缺血性卒中预后评估更具时效性。
出血鉴别:联合tPAI·C可区分DIC继发性纤溶(PIC↑)与原发性纤溶(tPAI·C↑)。
3. TM(血栓调节蛋白)
核心功能:血管内皮损伤的“哨兵蛋白”,结合凝血酶并激活蛋白C抗凝系统。
临床意义:
血管内皮损伤:脓毒症、ARDS、急性肾衰时TM显著升高,提示内皮屏障破坏。
新冠肺炎预警:重症患者TM水平与细胞因子风暴、多器官衰竭密切相关。
4. tPAI·C(组织纤溶酶原激活物-纤溶酶原激活物抑制剂-1复合物)
核心功能:综合反映纤溶活性与血管内皮状态。
临床意义:
妊娠并发症:子痫前期患者tPAI·C下降提示终止妊娠后纤溶亢进缓解,出血风险降低。
肥胖与肿瘤:PAI-1基因突变(如4G4G型)导致tPAI·C代偿性升高,加剧血栓风险;癌症患者tPAI·C增高与肿瘤转移相关。
二、血栓四项的联合应用场景
血栓高危人群筛查:
肿瘤患者:TAT+D二聚体联合监测,预警VTE发生。
妊娠期女性:tPAI·C+TM动态评估孕期高凝状态及产后血栓风险。
抗凝/溶栓疗效监测:
溶栓治疗后:PIC快速下降提示纤溶有效;TAT反弹需警惕再梗死。
抗凝治疗中:TM与PIC比值异常提示内皮损伤未改善。
疑难病例鉴别诊断:
DIC分型:TAT+PIC+TM联合判断凝血-纤溶失衡类型(高凝期/纤溶亢进期)。
出血原因分析:tPAI·C与PIC动态变化辅助区分纤溶机制。
三、检测优势与未来展望
血栓四项通过量化凝血-纤溶系统的关键分子,实现了从“静态检测”到“动态监测”的跨越:
早期预警:在D二聚体升高前捕捉凝血激活信号(如TAT)。
精准分型:辅助区分DIC亚型、溶栓疗效及出血机制。
个体化治疗:为抗凝、抗纤溶药物剂量调整提供依据。
随着研究的深入,血栓四项有望成为心血管疾病、肿瘤、妊娠并发症等领域的常规检测项目,推动血栓管理的精准化与个体化。
总结
血栓四项(TAT/PIC/TM/tPAI·C)通过多维度解析凝血-纤溶平衡,为临床提供了更高效的血栓风险管理工具。从感染性疾病的DIC预警到肿瘤患者的VTE预防,从溶栓治疗的实时监测到妊娠并发症的动态评估,其应用场景仍在不断拓展,成为精准医学时代不可或缺的诊断利器。
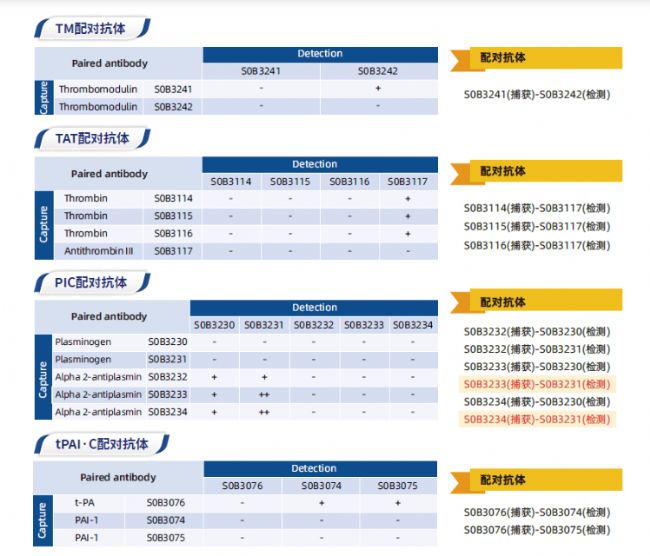
斯达特建立单B细胞抗体开发平台,研发血栓四项配对抗体,助力血栓性疾病早期诊断,欢迎来询!

杭州斯达特 (www.starter-bio.com)志在为全球生命科学行业提供优质的抗体、蛋白、试剂盒等产品及研发服务。依托多个开发平台:重组兔单抗、重组鼠单抗、快速鼠单抗、重组蛋白开发平台(E.coli,CHO,HEK293,InsectCells),已正式通过欧盟98/79/EC认证、ISO9001认证、ISO13485。

