下丘脑分泌的蛋白质激素Raptin在调节食欲和体重中的作用
2025-06-26 来源:MedChemExpress 点击次数:87在现代社会,熬夜已经成为许多人的常态。
然而,你可能不知道,熬夜中的你也许正在慢慢变胖~~
熬夜后,食欲大增,尤其是对高热量食物的渴望难以抑制?
Section.01
睡眠不足,
为何会让人变胖?
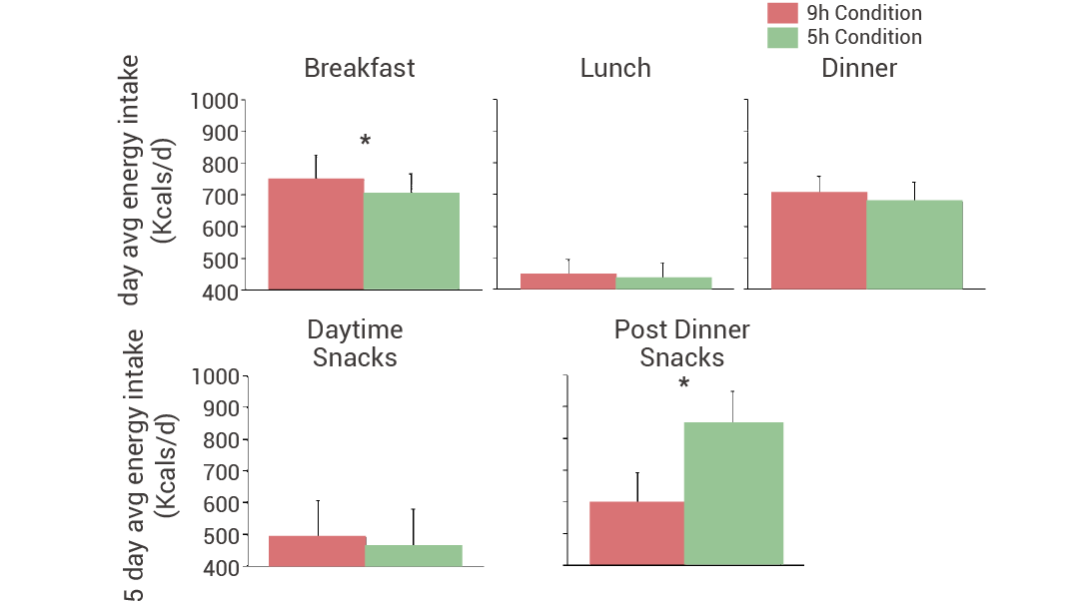
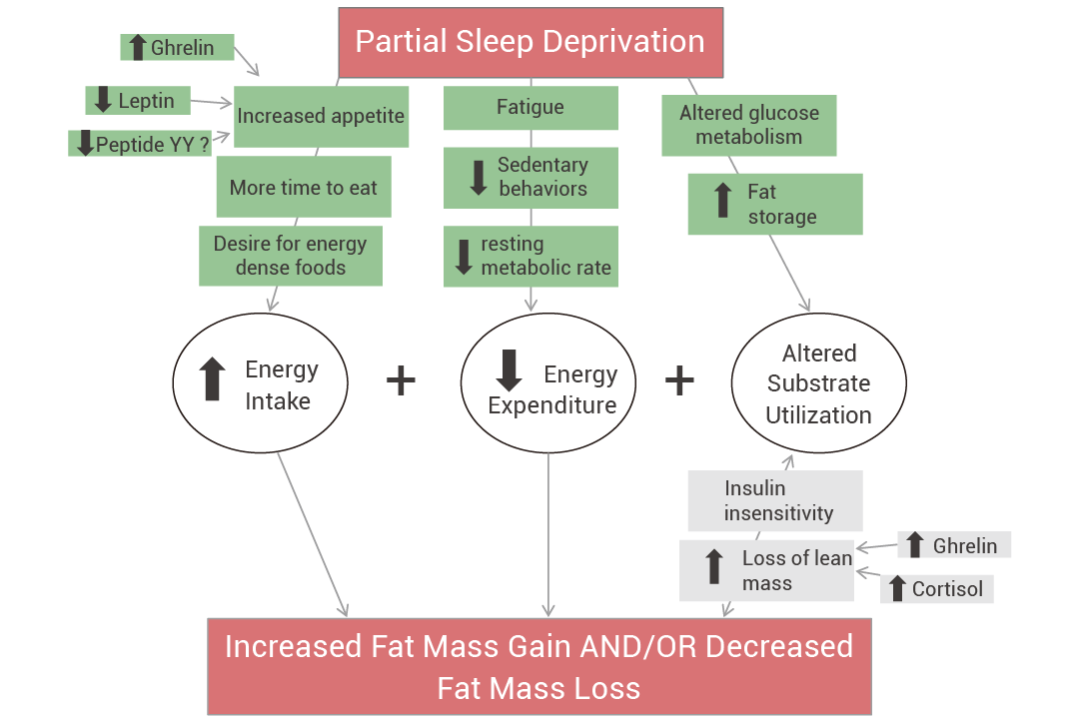
各项研究表明,睡眠不足会导致激素水平的变化,升高饥饿素 (ghrelin) 增强食欲,降低饱腹感激素 (如瘦素、PYY 和 GLP-1) 分泌使人吃得更多,这种能量摄入的增加超过了能量消耗的增加,热量差将导致最终体重增加。
Raptin:
睡眠诱导的"瘦素"新成员
近期, Cell Research 杂志上发表了一项重磅研究,研究者们发现了一种新的下丘脑激素——Raptin。
Raptin:
一种由下丘脑分泌的蛋白质激素,由 reticulocalbin-2 (RCN2) 蛋白经过切割产生。
研究人员通过构建睡眠片段化 (sleep fragmentation, SF) 小鼠模型,对其下丘脑进行蛋白质组学分析,发现与对照组相比,SF 小鼠的下丘脑中有多种蛋白质表达发生改变。其中,RCN2 在下丘脑中表达丰富,尤其是在视交叉上核 (SCN) 和室旁核 (PVN)。进一步研究发现,RCN2 在下丘脑 GT1-7 神经元中可以被切割成一个较短的片段,该片段能够分泌到细胞外。通过质谱分析,研究人员确定了这个片段的氨基酸序列,并将其命名为 Raptin。Raptin 是由 RCN2 的第 28 至 249 位氨基酸组成的片段。
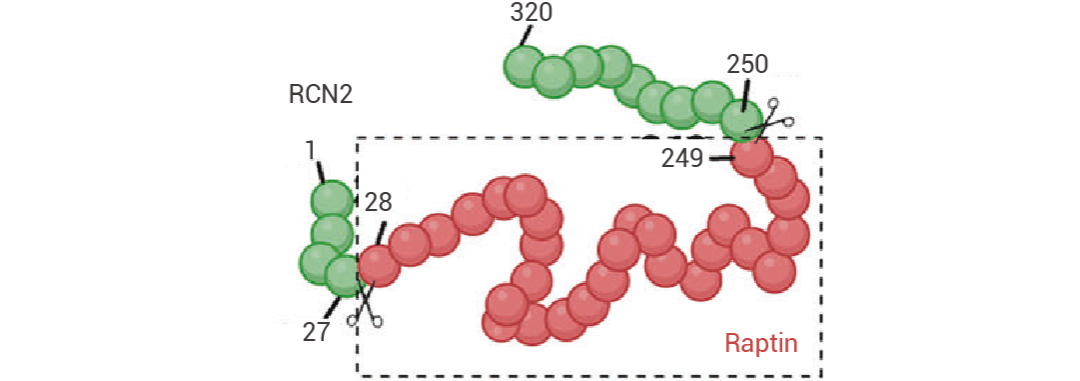
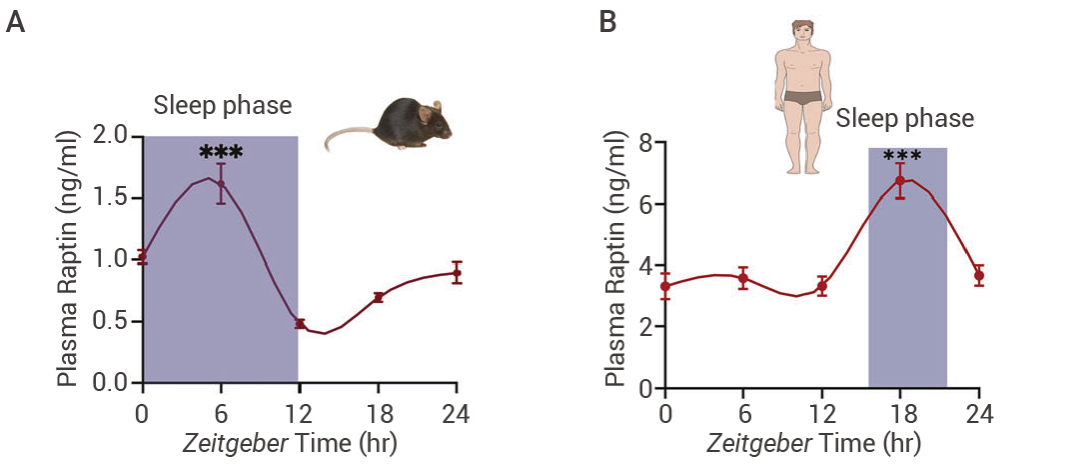 图 4. 3 个月大的雄性小鼠和人类在 ZT0、ZT6、ZT12 和 ZT18 时的血浆 Raptin 水平 (紫色区域表示睡眠阶段)[3]。
图 4. 3 个月大的雄性小鼠和人类在 ZT0、ZT6、ZT12 和 ZT18 时的血浆 Raptin 水平 (紫色区域表示睡眠阶段)[3]。此外,研究者通过标记视旁核 (PVN) 中的 GRM3 阳性神经元 (PVN GRM3 神经元),并利用膜片钳电生理分析发现 Raptin 能够激活这些神经元。通过化学遗传学方法操控 PVN GRM3 神经元,发现其激活能够抑制食欲,但不影响胃排空,表明 PVN 通路与胃无直接联系,而胃中 GRM3+ 神经元的激活则同时抑制食欲并减缓胃排空。
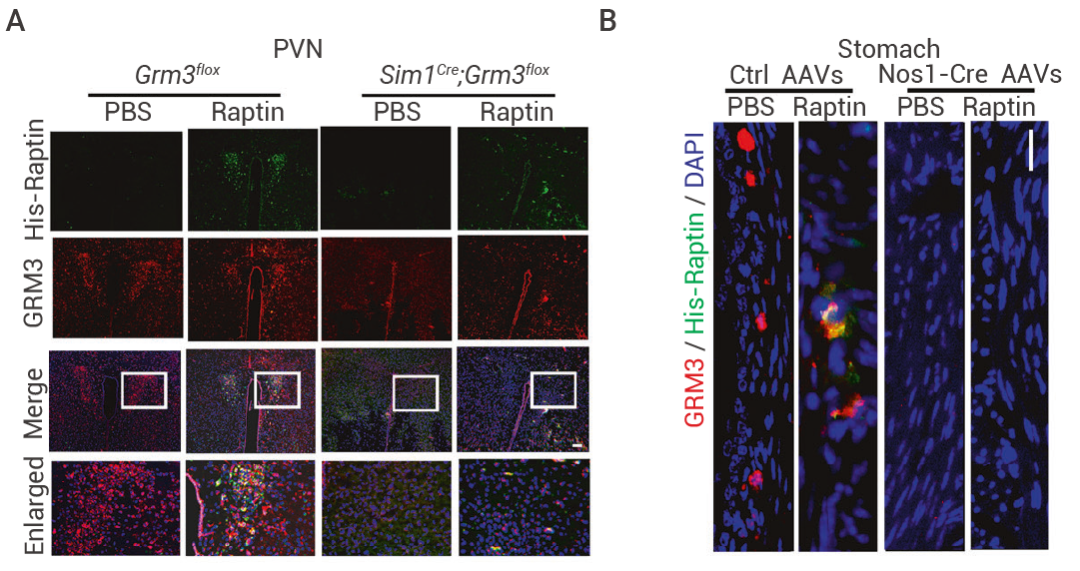
研究还比较了谷氨酸和 Raptin 对下游信号通路的影响,发现谷氨酸通过抑制 cAMP 信号通路影响神经元活性,而 Raptin 则通过激活 AKT 信号通路发挥作用,且两者对 AKT 信号通路无相互影响。此外,通过在 PVN 中特异性敲低 KHC,发现 Raptin 对神经元的激活作用减弱,且其对食欲抑制的效果也降低。结果表明,KHC 在 Raptin-GRM3 信号通路介导的神经元激活和食欲控制中不可或缺。
总之,研究证明 Raptin-GRM3 信号通路通过激活 PI3K-AKT 信号通路,促进 KHC 介导的线粒体运动,调节食欲控制的能量供应,发挥厌食作用。
Section.03
Raptin 的神经回路:
从睡眠到食欲的桥梁
此外,经过进一步探索 Raptin 分泌的神经机制。研究者发现,Raptin 的分泌受到 SCN 中精氨酸加压素 (AVP) 神经元的调控。这些 AVP 神经元通过神经回路与 PVN 中的 Raptin 分泌神经元相连,从而调节 Raptin 的分泌。
通过光遗传学和化学遗传学技术,成功地激活或抑制了 SCN 中的 AVP 神经元,可以观察到 Raptin 分泌和食欲的相应变化。这些实验结果表明,SCN-AVP 神经元与 PVN-Raptin 神经元之间的神经回路是调节食欲和体重的关键。
Section.04
Raptin与肥胖:
临床证据与基因突变
为了更好地揭示 Raptin 在调节食欲和肥胖中的作用,研究者在 SF 小鼠的 PVN 中过表达 Raptin,结果发现与 SF 对照小鼠相比,PVN 中 Raptin 过表达的 SF 小鼠的食物摄入量和体重增加显著减少,PVN 中 Raptin 的过表达还显著改善了 SF 小鼠的葡萄糖耐受性和胰岛素敏感性。这说明 Raptin 不仅能够调节食欲和体重,还对代谢功能有积极影响。这为 Raptin 作为一种潜在的治疗肥胖和代谢紊乱的靶点提供了有力的证据。
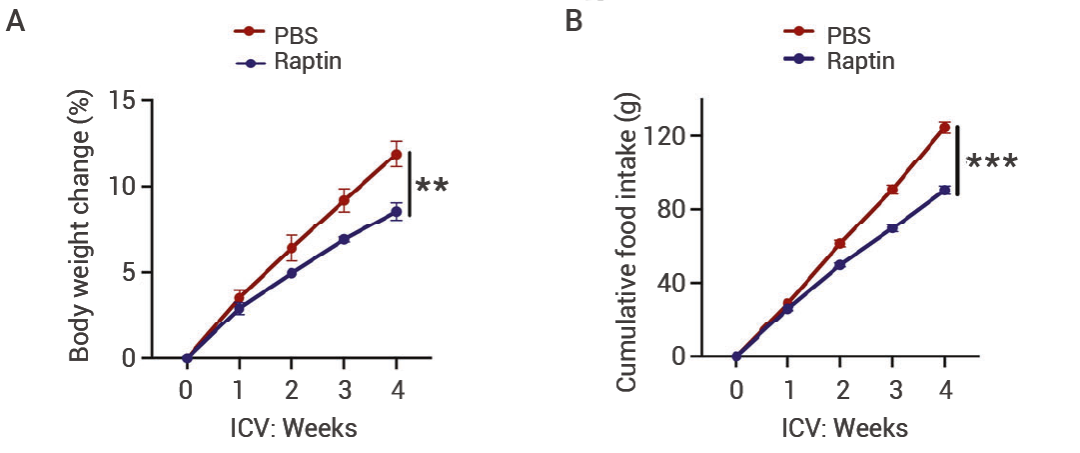 图 6. 4 个月大的 SF 雄性小鼠中,通过脑室内(ICV)输注 Raptin 或 PBS 4 周后的体重变化和累积食物摄入量[3]。
图 6. 4 个月大的 SF 雄性小鼠中,通过脑室内(ICV)输注 Raptin 或 PBS 4 周后的体重变化和累积食物摄入量[3]。除了动物实验,研究者们也对人类进行了研究。他们发现,肥胖患者往往伴随着睡眠质量下降和 Raptin 水平降低。而且,经过睡眠限制疗法 (SRT) 治疗的肥胖患者,其 Raptin 水平显著增加,体重和能量摄入也随之减少。
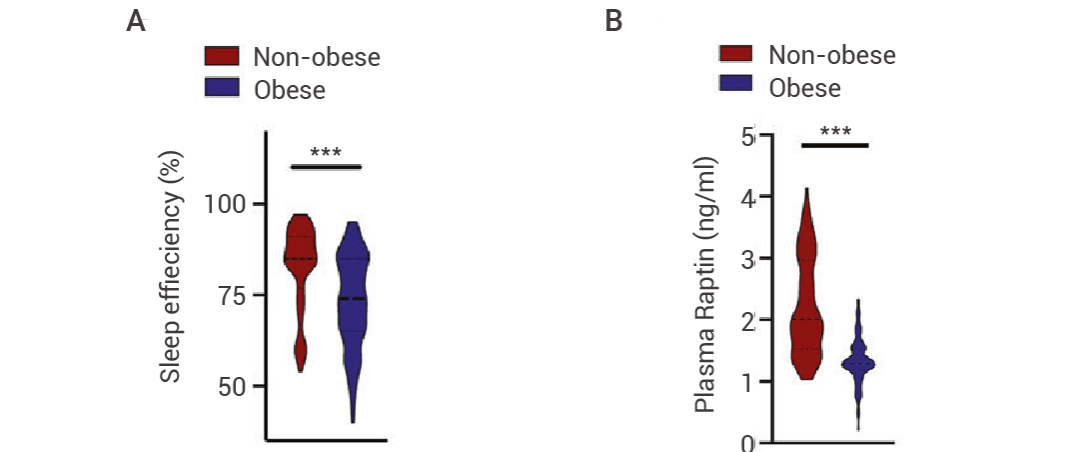 图 7. 肥胖和不肥胖者的睡眠效率和血浆中 Raptin 水平的统计图[3]。
图 7. 肥胖和不肥胖者的睡眠效率和血浆中 Raptin 水平的统计图[3]。此外,研究者们还发现了一种与肥胖相关的 RCN2 基因突变。这种突变会导致 Raptin 无法正常分泌,从而无法有效抑制食欲。携带这种突变的个体不仅更容易肥胖,还会出现夜食综合征,即夜间醒来进食的行为。原来晚上控制不住想吃有可能是基因突变导致的~
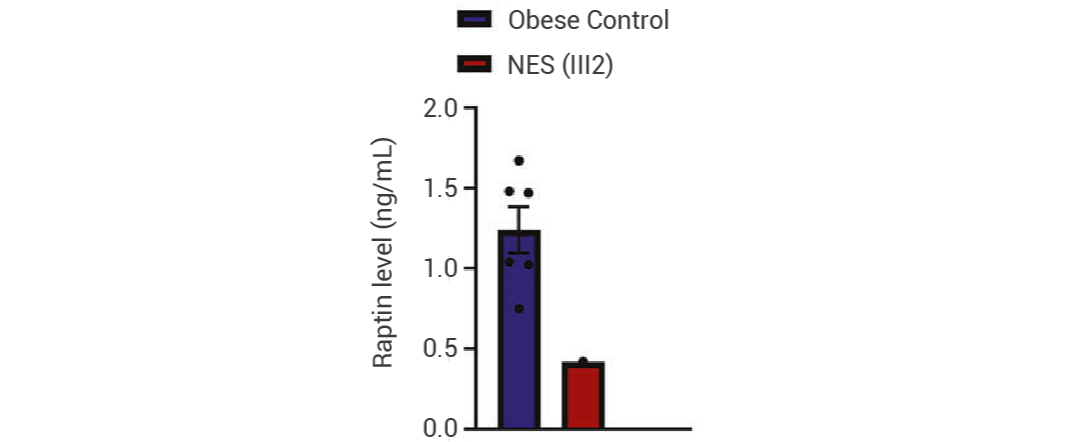 图 8. 患有夜食综合征(NES)的患者与对照组在夜间阶段的血浆 Raptin 水平[3]。
图 8. 患有夜食综合征(NES)的患者与对照组在夜间阶段的血浆 Raptin 水平[3]。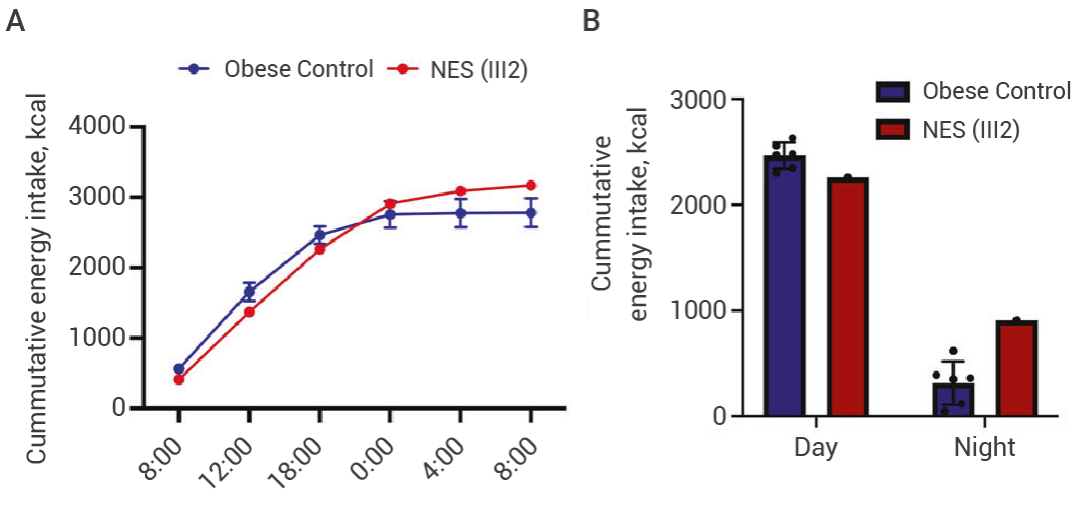 图 9. NES 患者及其肥胖对照组(年龄、性别和 BMI 匹配,n = 6)在白天和夜间阶段的累积能量摄入曲线和定量分析[3]。
图 9. NES 患者及其肥胖对照组(年龄、性别和 BMI 匹配,n = 6)在白天和夜间阶段的累积能量摄入曲线和定量分析[3]。Section.05
Raptin:
未来减肥治疗的新希望
这项研究不仅揭示了 Raptin 在调节食欲和体重中的重要作用,还为未来的减肥治疗提供了新的思路。科学家们认为,通过调节 Raptin-GRM3 信号通路,或许可以开发出新的减肥药物。此外,改善睡眠质量也可能成为一种有效的减肥策略。
总之,Raptin 的发现让我们对睡眠与肥胖之间的关系有了更深入的理解。也许有一天,我们真的可以通过改善睡眠来实现“睡”出好身材的梦想。不过,在那之前,保持良好的睡眠习惯仍然是我们控制体重的重要手段之一。
|
产品推荐 |
|
Peptide YY (PYY), human (HY-P1514) 一种肠道激素,可调节食欲和抑制胰腺分泌,也可以通过神经肽 Y 受体 (Neuropeptide Y receptors) 介导其作用。 |
|
一种有效的,不可逆的,选择性 PI3K 抑制剂,IC50 值为 3 nM。阻断自噬形成,并有效抑制 Polo-like kinase 1 (PlK1) 和 PlK3,IC50 值分别为 5.8 和 48 nM。 |
|
一种广谱 PI3K 抑制剂,也可抑制 CK2 的活性。也是一种竞争性 DNA-PK 抑制剂,可逆结合 DNA-PK 的激酶结构域。还是一种凋亡激活剂。 |
|
一种有效、选择性和可透过血脑屏障的 mGlu2/3R 激动剂,具有抗氧化和神经保护作用。 |
|
一种有效,能透过中枢神经系统的,选择性谷氨酸受体亚型 3 的负变构调节剂, 在啮齿动物中具有抗抑郁和抗焦虑活性。 |
|
一种高效选择性 mGlu3 受体激动剂。 |
|
一种有效,选择性的 group II (mGlu2/3) receptor 激动剂。 |
|
选择性环氧合酶 -2 (COX-2) 的抑制剂,IC50 值为 25.8 μM;有效的肝 N-乙酰转移酶 2 (NAT2) 抑制剂;广泛使用的解热和止痛剂。也可以在小鼠体内诱导铁死亡 (ferroptosis),并造成急性肝损伤。 |
|
代谢型谷氨酸受体 (mGluR) 拮抗剂。 |
|
Protein A/G Magnetic Beads (HY-K0202) Protein A/G 磁珠。 |
|
分离自牛肺的丝氨酸蛋白酶 (BPTI) 抑制剂,对胰蛋白酶和胰凝乳蛋白酶的 Ki 值分别为 0.06 pM 和 9 nM。 |

[1] Markwald RR, et al. Impact of insufficient sleep on total daily energy expenditure, food intake, and weight gain. Proc Natl Acad Sci U S A. 2013 Apr 2;110(14):5695-700.
[2] Shlisky JD, et al. Partial sleep deprivation and energy balance in adults: an emerging issue for consideration by dietetics practitioners. J Acad Nutr Diet. 2012 Nov;112(11):1785-97.
[3] Xie LQ, et al. Raptin, a sleep-induced hypothalamic hormone, suppresses appetite and obesity. Cell Res. 2025 Mar;35(3):165-185.



