人外周血CD3+T细胞分选培养攻略
2026-03-30 来源:本站 点击次数:60分选原理
选用生物素(biotin)标记的单克隆抗体对非目标细胞(非 CD3+ T 细胞)进行标记,然后通过链霉亲和素(streptavidin)标记的磁珠对非目标细胞进行清除,从而达到人外周血 CD3+ T 细胞分选的目的。分选过程需要用到磁力架。
分选试剂及仪器
人CD3+T细胞分选试剂盒(阴选法)(abs50126)
产品组成:
|
组分名称 |
5×108 cells |
1×109 cells |
|
Biotin-Antibody Mix |
100uL |
200uL |
|
Streptavidin |
1mL |
2mL |

分选方法
1、制备人 PBMC:利用 Ficoll 密度梯度离心法从人外周血中分离 PBMC,收集 PBMC,以 PBS
洗涤细胞,离心后将 PBMC重悬于分选 buffer中,调整细胞密度为 1×108 cells/mL。
2、将 100 μL 细胞悬液(1×107个细胞)加入无菌流式管底部,再加入 2 μL Biotin-Antibody Mix,混匀后4°C 孵育 10 min。
注意:将细胞悬液直接加入流式管底部,避免沿流式管管壁加入。根据所使用磁力架不同也可使用离心管进行细胞分选。如果分选更多细胞,则按比例增加 Biotin-Antibody Mix 的用量。
3、孵育完成后,在流式管中加入 20 μL 清洗过的 Streptavidin,混匀后 4°C 孵育 10 min(磁珠使用前需要用分选 buffer 进行清洗:涡旋振荡彻底重悬磁珠,取实验需要的磁珠至 1.5 mL 离心管,加入分选 buffer 至总体积为 1 mL,10000 g,离心 1 min,弃上清。加入 1 mL 分选 buffer 重悬磁珠,10000 g,离心 1 min,弃上清。用与起初相同体积的分选 buffer 重悬磁珠。如取 20 μL 磁珠进行清洗,则清洗后用 20 μL 分选 buffer 进行重悬)。
注意:如果分选更多细胞,则按比例增加 Streptavidin 用量。例如分选 5×107 个细胞,在 500 μL 细胞悬液中加入 10 μL Biotin-Antibody Mix 和 100 μL treptavidin。如果分选少于 1×107个细胞,则将细胞悬液体积补至 100 μL,加入 2 μL Biotin-Antibody Mix 和 20 μL Streptavidin。
4、孵育完成后,在流式管中加入 2.5 mL 分选 buffer,用移液器吹打 5 次混匀(避免剧烈振荡或者上下颠倒混匀)。
5、将含有细胞的流式管置于磁力架上,静置 5 min。
6、将细胞悬液轻柔倒入一个无菌离心管中(倾倒过程中流式管不要脱离磁力架),此细胞悬液中即包含纯化的人 CD3+ T 细胞。300 g,离心 5 min。弃上清,收集细胞。
7、根据实验需要洗涤细胞后,将细胞重悬于所需缓冲液或培养基中,进行培养。

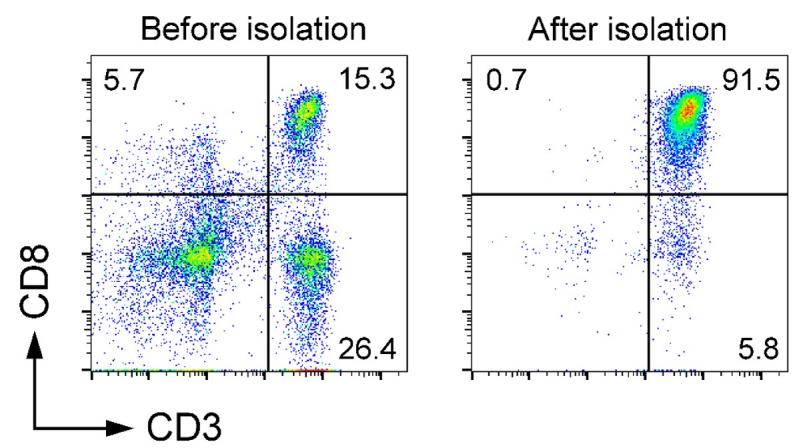
从人PBMC中分选CD3+ T细胞,用PE标记的 anti-human CD3抗体(克隆号OKT3)染色后进行流式细胞分析. 结论:分选前后的CD3+ T细胞纯度分别为69.1%和97.9%。
培养原理
人 CD3/CD28 T 细胞激活磁珠可以简单快捷的活化及扩增T 细胞,无需饲养层细胞(抗原递呈细胞)或抗原。磁珠为直径 5 µm 的惰性超顺磁珠,大小与抗原呈递细胞相似,同时共价偶联抗CD3 和抗CD28 抗体。细胞培养过程中可使用重组人 IL-2 刺激 T 细胞群扩增。活化或扩增后,磁珠可以通过磁力架轻松去除。
培养步骤
一、试剂配置
1、清洗 buffer:含有 2 mM EDTA 和 2% 胎牛血清(FBS)的 PBS 或者含有 2 mM EDTA 和 5% BSA的 PBS,需预先通过 0.22 μm 滤膜过滤除菌。
2、免疫细胞无血清培养基(abs9772);
3、IL-2(abs04045);
4、CD3/CD28磁珠(abs160032);
5、青霉素-链霉素溶液(100×,双抗)(abs9244)
二、操作步骤
1、清洗磁珠
(1)彻底重悬试管中的磁珠(如涡旋>30秒,或置于旋转仪5分钟)。
(2) 吸取目标体积的磁珠至流式管中,加入同等体积的清洗Buffer。若不足1mL,添加1mL的清洗Buffer,涡旋5秒,或使用移液器吹打混匀,注意避免产生气泡(此处也可直接使用细胞培养基清洗)。
(3)将流式管置于磁力架上3分钟,弃上清。
(4)重复步骤2-3,本次使用细胞培养基对磁珠再次清洗。共清洗磁珠两次。
(5) 使用细胞培养基重悬磁珠(比如:吸取 25 μL 磁珠进行清洗,清洗后用 1 mL 细胞培养基进行重悬)。
注意事项
取用激活磁珠前彻底重悬磁珠(如涡旋>30秒,或置于旋转仪5分钟),吹打时避免产生气泡。进行流式检测前,使用磁力架去除磁珠(包括结合在细胞上的磁珠,可以通过轻柔吹打释放磁珠),此时细胞位于上清液中。收集上清液,进行下一步的流式检测。
2、人 T 细胞的扩增
(1)调整CD3+ T细胞种板浓度为1-1.5 x 106 cells/mL,按照磁珠与细胞比例1:1加入激活磁珠。
(2)激活 2天后,向培养基中添加 300 U/mL 的重组人 IL-2。
(3)细胞与磁珠放于 37℃,5% CO2培养箱中孵育,根据实验需要决定细胞的培养时长。
(4) 每日查看细胞激活与扩增情况,注意细胞的大小和形状。当细胞皱缩或增殖速度明显放慢时,提示细胞可能耗竭。
(5)推荐在细胞激活的前 2天时不要处理细胞,2 天后随时观察细胞状态,当培养基变黄或孔内细胞数目过多时换液或传代。每次换液或传代后,应及时补充重组人 IL-2 至 300 U/mL。
(6)定期进行细胞计数,当细胞密度超过 5x 106 cells/mL 时,轻柔吹打混匀,将细胞密度调整为 0.5-1 x 106 cells/mL。
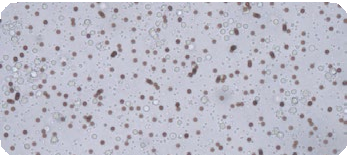 |
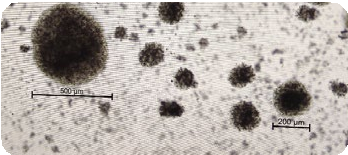 |
| 刚接种的 T 细胞(棕色为抗体欧联磁珠) | T 细胞-day5-细胞增殖明显(T细胞团) |
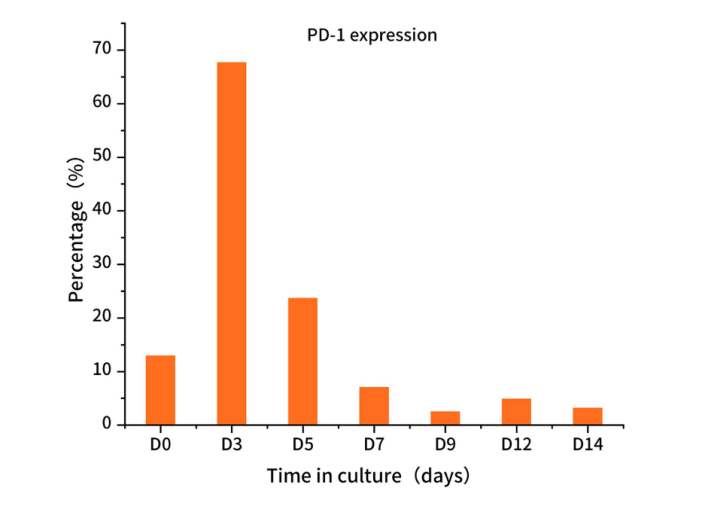
活化人T细胞的PD-1表达。人T细胞用抗人CD3/CD28磁珠刺激,并扩增14天
使用人CD3/CD28 T细胞激活磁珠,刺激CD3+ T细胞24到48小时,细胞用FITC anti-human CD69抗体(克隆号FN50 )和PE anti-human CD25抗体(克隆号BC96)标记,进行流式细胞仪分析。 结论:刺激前后CD25+ CD69+ T细胞占总细胞的比例分别为0.70% 和75.81%
产品推荐
|
货号 |
品名 |
规格 |
|
人CD3+T细胞分选试剂盒(阴选法) |
1mL/2mL |
|
|
细胞磁性分离器(多功能) |
1个 |
|
|
免疫细胞无血清培养基 |
1L |
|
|
Recombinant Human IL-2 Protein |
10ug/50ug/100ug |
|
|
CD3/CD28磁珠 |
1mL |
|
|
青霉素-链霉素溶液(100×,双抗) |
100mL |

