肠脑轴新机制的研究揭示神经肽 SP 护肠抗焦虑关键通路
2026-04-02 来源:本站 点击次数:16
中国农业大学马云飞团队于《Nature communication》发表了一篇名为“Neuropeptide SP protects against colitis and linkedanxiety-like behavior through the putative roles ofgut microbiota and metabolite inositol”的文章。其研究旨在系统评估神经肽 P 物质(SP)对 DSS 诱导的小鼠结肠炎及其相关焦虑样行为是否具有保护作用,并进一步在 TNBS 结肠炎模型中验证其有效性;同时阐明 SP 的保护作用是否依赖肠道菌群,以明确菌群在该过程中的关键地位。在此基础上,筛选并验证 SP 调控肠道菌群后产生的关键代谢物,确定介导肠–脑信号传递的核心分子,并解析 SP 通过菌群–代谢物途径影响海马小胶质细胞与星形胶质细胞的具体信号通路,从而揭示肠–脑轴的分子机制,最终为炎症性肠病(IBD)合并焦虑等精神共病提供新的治疗靶点与干预策略。
01、研究方法
1 动物模型与分组处理
构建 DSS 诱导的急性结肠炎小鼠模型,设置正常对照组、模型组、模型联合物质 P 干预组以及单纯物质 P 处理组。同时建立 TNBS 诱导的克罗恩病样结肠炎模型,设置空白对照、模型对照以及不同剂量物质 P 干预组。通过混合抗生素清除小鼠肠道菌群,再进行 DSS 造模与物质 P 干预,开展菌群耗竭实验;分别将正常小鼠、模型小鼠及模型联合物质 P 干预小鼠的粪便移植至经抗生素预处理的受体小鼠体内,完成粪菌移植实验;此外,通过外源性肌醇干预及肌醇合成抑制剂阻断试验,进一步验证关键代谢物的功能作用。
2 肠道损伤评价方法
试验期间每日记录小鼠疾病活动指数与体重变化,试验结束后检测结肠长度以评估肠道大体损伤。通过组织病理学染色观察肠道组织形态,借助透射电镜分析肠道超微结构改变;采用免疫荧光技术检测肠道黏液屏障及上皮连接相关蛋白表达,同时测定血清荧光标记葡聚糖含量评估肠道通透性,并检测髓过氧化物酶活性与炎症因子水平,综合评价肠道炎症及屏障损伤程度。
3 行为学评价方法
运用旷场实验、高架十字迷宫、高架零迷宫及明暗箱实验等多种行为学范式,系统评估小鼠的焦虑样行为表现;待肠道炎症消退后重复开展行为学检测,以排除炎症本身引发的躯体不适对行为学结果的干扰。
4 海马损伤与神经炎症检测
通过组织染色观察海马神经元形态及损伤情况,采用免疫荧光及免疫组化技术检测海马区小胶质细胞与星形胶质细胞的活化水平;结合多重细胞因子检测、实时荧光定量 PCR 及蛋白免疫印迹技术,分析海马组织炎症因子表达及相关信号通路蛋白水平,探究海马区域神经炎症与损伤特征。
5 组学与分子机制检测
利用 16S rRNA 高通量测序分析肠道菌群的多样性及群落组成,通过非靶向代谢组学筛选并鉴定菌群相关差异代谢物;分别对海马组织及流式分选后的小胶质细胞、星形胶质细胞进行转录组测序,分析关键信号通路的表达变化;采用双标免疫荧光技术定位相关通路蛋白及受体在胶质细胞中的表达分布;并通过小胶质细胞与星形胶质细胞体外培养模型,验证关键代谢物的生物学功能。
6 数据统计分析
数据统计采用单因素及双因素方差分析、Tukey 多重比较检验,结合主坐标分析、置换多元方差分析、基因集富集分析及 Spearman 相关性分析等方法进行处理与解析。
02、研究内容
1 SP 可显著改善 DSS 诱导的结肠炎与焦虑样行为
SP 干预可明显降低结肠炎小鼠 DAI 评分、减轻体重下降、恢复结肠长度。组织学显示 SP 能改善结肠黏膜损伤、隐窝丢失与炎症细胞浸润,透射电镜结果表明 SP 修复结肠上皮微绒毛与细胞间隙结构。AB‑PAS 与免疫荧光证实 SP 恢复杯状细胞数量与 MUC2 分泌,降低肠道通透性,减少结肠促炎因子水平。
行为学结果显示,DSS 模型小鼠出现显著焦虑样表现,而 SP 可显著逆转旷场、高架十字迷宫、高架零迷宫、明暗箱中的焦虑行为。在肠道炎症消退后,焦虑行为仍持续存在,SP 依然可发挥抗焦虑作用,证明其效果不依赖急性炎症缓解。

图1 SP能缓解DSS诱导小鼠的结肠炎症和焦虑样行为
2 SP 减轻海马损伤与神经炎症,调控小胶质 / 星形胶质细胞
DSS 导致海马神经元出现核固缩、细胞丢失等病理损伤,尼氏小体大量减少,SP 可显著改善上述损伤。同时 DSS 引起海马促炎因子升高、抗炎因子降低,诱发强烈神经炎症。
免疫荧光显示,DSS 使海马小胶质细胞大量激活,星形胶质细胞数量明显下降;SP 可抑制小胶质细胞活化,减少 M1 型标记物 iNOS 表达,并阻止星形胶质细胞丢失,提高 GFAP 水平。说明 SP 通过维持海马胶质细胞稳态发挥神经保护作用。

图2 SP能减轻DSS诱导小鼠的海马损伤和神经炎症
3 SP 无法透过血脑屏障,而是重塑肠道菌群结构
ELISA 与 qPCR 证实,外源性 SP不能有效穿过血脑屏障进入海马,提示其脑保护作用来自外周途径。
16S 测序显示,SP 不改变菌群 α 多样性,但显著重塑 β 多样性结构。在门水平,SP 提高厚壁菌门丰度,降低拟杆菌门与变形杆菌门异常升高;在科与属水平,SP 提高毛螺菌科、Muribaculaceae 等有益菌丰度,降低拟杆菌属、大肠志贺菌属等有害菌丰度。PICRUSt2 预测显示 SP 恢复菌群代谢功能,显著上调肌醇磷酸代谢通路。

图3 SP能改善肠道微生物菌群失调
4 SP 的保护作用完全依赖肠道菌群
抗生素清除菌群后,SP 对结肠炎的改善作用几乎完全消失,体重、DAI、结肠长度、组织病理、杯状细胞丢失等均无法被 SP 逆转。同时行为学结果显示,菌群耗竭后 SP 不再具有抗焦虑效果。
粪菌移植实验证实,移植 DSS+SP 供体粪便可显著改善受体鼠的结肠炎、肠道屏障损伤与结肠炎症;同时改善焦虑样行为,减轻海马病理损伤,抑制小胶质细胞 M1 极化、恢复星形胶质细胞数量。受体鼠菌群结构也向正常状态恢复,证明肠道菌群介导 SP 的肠与脑保护作用。
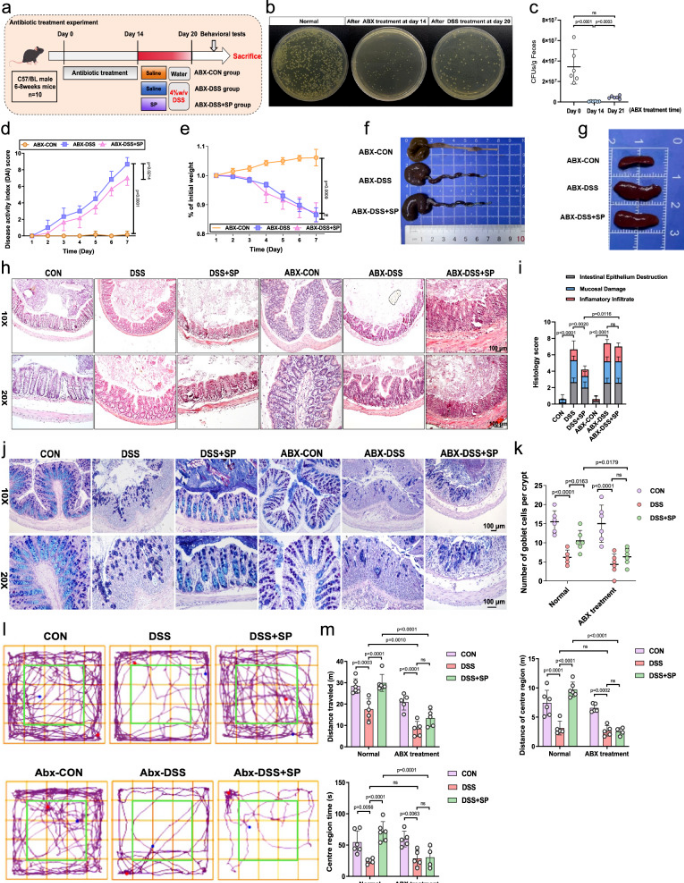
图4 SP以肠道微生物群依赖的方式保护DSS引起的肠道损伤和类焦虑障碍

图5 FMT实验显示,SP通过调节肠道微生物群,减轻了DSS引起的结肠炎和焦虑样行为
5 SP 通过菌群调控海马NF‑κB 与 GABAergic/Ca²⁺信号通路
粪菌移植后的海马转录组显示,DSS‑FMT 显著激活NF‑κB 通路,而 SP‑FMT 可抑制该通路。分子验证显示,SP 通过菌群降低小胶质细胞 p‑p65、p‑IKBα 水平,抑制神经炎症核心通路。
同时 SP‑FMT 显著激活神经活性配体–受体互作与Ca²⁺信号通路,提高 GABA 合成关键酶、GABAA/GABAB 受体与 CaMKII 的表达。双标免疫荧光证实,SP 通过菌群抑制小胶质细胞内 p‑IKBα,增强星形胶质细胞 GABA 受体与 CaMKII 信号。流式分选细胞转录组进一步确认:SP 通过菌群抑制小胶质细胞 NF‑κB、增强星形胶质细胞 GABAergic/Ca²⁺。

图6 SP通过调节肠道微生物群影响海马体的基因表达2+信号通路
6 SP 提高菌群代谢物肌醇,肌醇可模拟 SP 全部保护效应
非靶向代谢组学显示,SP 显著提高结肠内容物中肌醇水平,为最显著上调的代谢物,且富集于肌醇磷酸代谢通路。
直接补充肌醇可重现 SP 的全部效果:改善 DSS 结肠炎、修复肠道上皮、降低炎症;逆转焦虑样行为;减轻海马病理与神经炎症;抑制小胶质细胞活化、恢复星形胶质细胞数量;提高海马 GABA 含量与 GABA 受体、GAT1 表达。证明肌醇是 SP 发挥作用的关键下游代谢物。

图7 SP增强肠道微生物群来源代谢物肌醇的富集
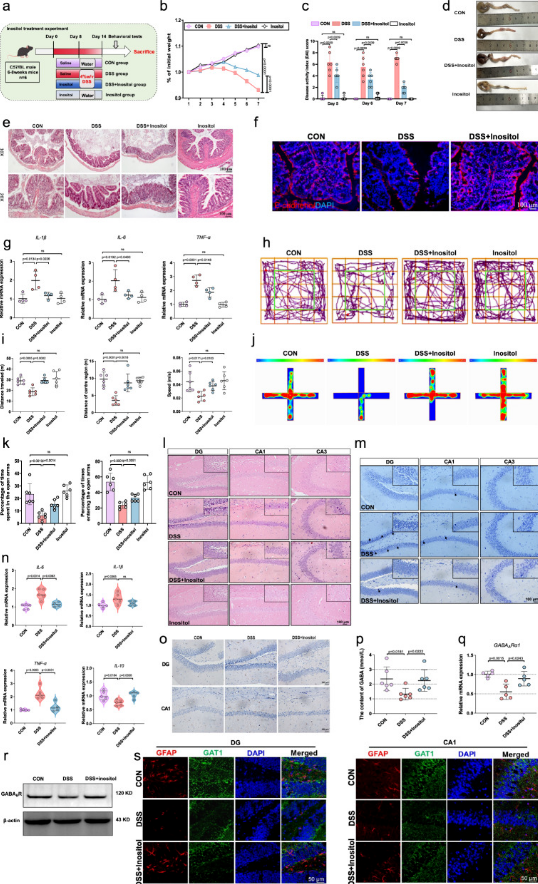
图8 肠道代谢物肌醇介导SP对DSS诱导小鼠结肠炎和焦虑样行为的保护作用
7 阻断肌醇合成可完全逆转SP 的神经保护与抗焦虑作用
使用肌醇合成抑制剂 L‑690330 后,SP 对焦虑样行为的改善作用消失,海马神经元损伤与尼氏小体丢失重新出现。FMT‑SP 可提高血清与海马肌醇含量,体外实验证实肌醇可抑制 LPS 诱导的小胶质细胞炎症,并在星形胶质细胞中激活 GABAergic/Ca²⁺信号。证明肌醇是 SP 发挥神经保护与抗焦虑作用的必需分子。

图9 肌醇在SP对抗DSS诱导小鼠焦虑类行为的作用中起关键作用
03、创新点
首次揭示 SP 通过微生物–肠–脑轴发挥双重保护作用:打破传统认为 SP 主要促炎的认知,证实外源性 SP 可同时改善 IBD 肠道损伤与焦虑样行为,且作用不依赖直接入脑。
明确肠道菌群是 SP 发挥作用的必需环节:通过抗生素耗竭与粪菌移植严格证明,SP 的肠保护与神经保护作用完全依赖肠道菌群,为神经肽调控菌群提供直接证据。
发现肌醇是介导 SP 肠–脑信号的关键代谢物:首次鉴定菌群来源的肌醇作为核心效应分子,可模拟 SP 全部功能,抑制肌醇则阻断 SP 作用,填补菌群代谢物介导 IBD 相关焦虑的机制空白。
04、启发
重新认识神经肽的双重功能:同一分子在不同剂量、来源、疾病阶段可发挥相反作用,研究中应区分内源性与外源性效应,避免单一功能定性。
肠–脑轴研究应重视 “菌群–代谢物” 核心环节:很多神经、精神、代谢药物可能通过肠道菌群起效,机制研究必须纳入菌群与代谢物验证。
胶质细胞是情绪调控的关键靶点:焦虑研究不应只关注神经元,小胶质细胞炎症与星形胶质细胞功能异常是重要突破口。
参考文献:Lan J, Wang J, Huang S, Li C, Deng Z, Hao Z, Ma Y. Neuropeptide SP protects against colitis and linked anxiety-like behavior through the putative roles of gut microbiota and metabolite inositol. Nat Commun. 2026 Jan 8;17(1):295. doi: 10.1038/s41467-025-67904-0IF: 15.7 Q1 . PMID: 41507168; PMCID: PMC12789692.
征稿启示
深耕科研之路,每一次实验突破、每一篇论文产出、每一份思路沉淀,都值得被看见、被传播、被借鉴。
为搭建优质学术交流平台,汇聚各领域科研智慧,助力更多科研工作者互通思路、共享成果、碰撞灵感,本公众号正式开启长期科研推文征稿,诚邀广大科研同仁踊跃投稿,让你的学术见解发光发热!
-END-


想了解更多内容,获取相关咨询请联系
电 话:+86-0731-84428665
伍经理:+86-180 7516 6076
工程师:+86-180 7311 8029
邮 箱:consentcs@163.com


