小鼠模型助力发现CD4⁺ T细胞新亚群的研究,揭示肠道炎症新机制
2026-04-22 来源:本站 点击次数:1182026年4月2日,西湖大学医学院董晨院士团队在 Nature Immunology 在线发表了题为“A unique CD4+ T cell subset expressing granzyme K is regulated by transcription factor EOMES and important for T cell-mediated intestinal inflammation”的研究成果。该研究鉴定出一种以高表达颗粒酶K(GZMK)为特征的新型CD4+ 辅助T细胞亚群——THK细胞,并系统揭示了其由转录因子EOMES调控的特异机制及其在肠道炎症中的关键作用。这一发现不仅丰富了CD4+ T细胞的功能分类体系,还为炎症性肠病等慢性炎症疾病的免疫治疗提供了新思路。
南模生物为该研究提供了Gzmk-2A-CreERT2-2A-tdTomato(目录号:NM-KI-241127)小鼠模型。

肠道炎症性疾病严重威胁人类健康,传统观点认为CD4+ T细胞可分为TH1、TH2、TH17、Treg等经典谱系,每个亚群都有专属的核心转录因子,介导不同类型的免疫应答。颗粒酶家族蛋白此前主要发现于具有杀伤功能的免疫细胞中,其中颗粒酶K(granzyme K,GZMK)在CD4+ T细胞中的表达缺乏系统鉴定。对此,研究团队进行了以下研究:
1 人类中具有非典型特征的 GZMK+ CD4+ T细胞
为探究肠道炎症中是否存在非经典的CD4+ T细胞亚群,研究团队重新分析了来自炎症性肠病(IBD)患者(包括溃疡性结肠炎和克罗恩病)及健康对照者的整合单细胞RNA测序(scRNA-seq)数据集。结果表明,除已知的TH1、TH2、TH17、TFH及Treg等亚群外,存在一个以GZMK高表达为特征的CD4+ T细胞群体,该群体几乎不表达典型的CD4+ T细胞谱系标志物,同时GZMB表达极低(图1a)。进一步分析显示,在活动性溃疡性结肠炎患者的黏膜活检组织中,GZMK的表达水平显著高于缓解期患者和健康对照(图1b)。此外,在人类泛癌scRNA-seq数据中同样可观察到这一GZMK+ high CD4+ T细胞群体,且同样缺乏典型谱系标志物。以上数据提示,GZMK+ CD4+ T细胞是一个在人类炎症及肿瘤背景下广泛存在、具有非典型分子特征的潜在新亚群。
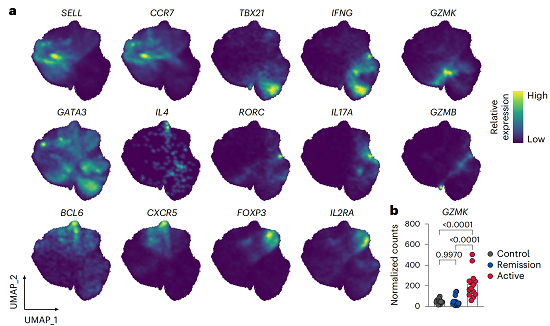
图1. 人类肠道炎症中GZMK表达CD4+ T细胞亚群的鉴定
2 小鼠结肠炎中表达GzMK的CD4+ T细胞的特性
为明确小鼠结肠炎模型中是否存在类似的GzMK+ CD4+ T细胞群体,研究团队整合了初始CD4+ T细胞过继转移结肠炎模型的公共scRNA-seq数据集。结果表明,结肠CD4+ T细胞可被分为六个转录亚群,其中聚类1以高表达Gzmk、几乎不表达其他谱系定义转录因子为特征,区别于TH1、TH17、Treg等经典亚群(图2a-c)。进一步利用Gzmk-P2A-CreERT2-T2A-tdTomato(GzmK-tdTomato)报告小鼠进行验证,发现在结肠炎小鼠的结肠固有层及肠系膜淋巴结中均可检测到GzmK-tdTomato+ CD4+ T细胞,且这些细胞主要为效应/记忆表型(CD44+ CD62L-)(图2d-e)。与GzmK- tdTomato- 细胞相比,该群体表达更高水平的穿孔素和颗粒酶B,但IFNγ表达水平相对较低(图2f-g)。体外细胞毒性实验显示,GzmK-tdTomato+与 GzmK-tdTomato- CD4+ T细胞对靶细胞均具有相似的杀伤能力。以上数据表明,小鼠结肠炎中存在一个独特的GzmK+ CD4+ T细胞亚群(THK),其具有效应/记忆表型,但细胞毒活性并非该群体所特有。
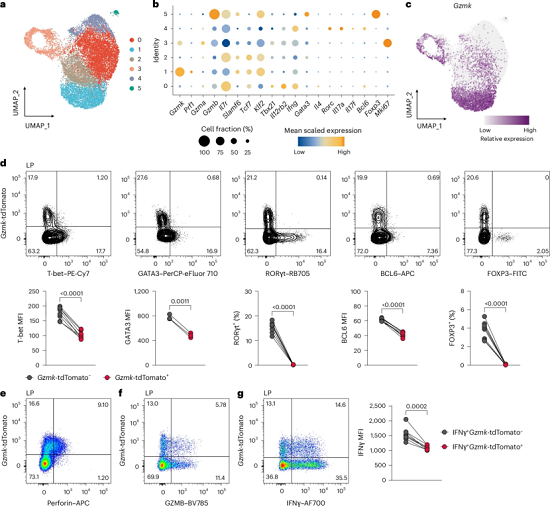
图2. 小鼠结肠炎中一个独特的Gzmk表达CD4+ T细胞群体
3 THK细胞分化不依赖于经典辅助T细胞谱系
为明确THK细胞的分化是否需要已知的辅助T细胞发育通路,研究团队采用共转移体系,将野生型与Tbx21缺陷(TH1 谱系关键转录因子缺失)的初始CD4+ T细胞同时转入Rag1-/-受体小鼠。结果显示,尽管Tbx21缺陷导致GZMB表达显著降低,但穿孔素阳性的CD4+ T细胞频率反而增加,且Gzmk的表达水平未受明显影响(图3a-c)。进一步分析显示,在Stat6缺陷(TH2谱系必需)的CD4+ T细胞中,Gzmk与穿孔素的表达基本不变(图3d-e);而在Rorc缺陷(TH17谱系相关)的CD4+ T细胞中,两者的表达反而显著升高(图3f-g)。此外,Bcl6缺陷可降低结肠CD4+ T细胞中Gzmk与Prf1的表达。同时,THK细胞不表达CD8α,且Runx3缺陷对Gzmk表达无显著影响。以上数据表明,THK细胞的分化独立于TH1、TH2和TH17的经典谱系定向程序,可能来源于Bcl6+ 祖细胞群体,且不同于CD4+ CD8α+ 细胞毒性T细胞。
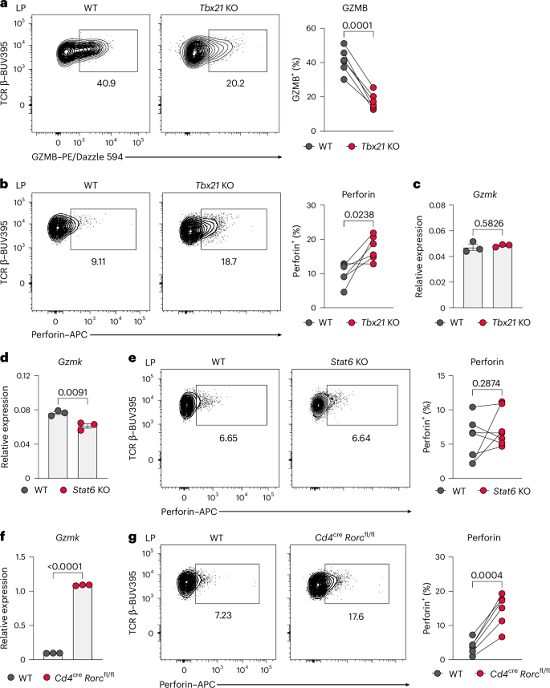
图3. THK细胞分化不依赖于TH1、TH2和TH17程序
4 Eomes与THK细胞在转录和表观遗传上相关联
为探究调控THK细胞独特身份的关键转录因子,研究团队对结肠炎小鼠固有层中分选的GzmK-tdTomato+与GzmK-tdTomato- CD4+ T细胞进行了bulk RNA-seq分析。结果表明,GzmK+ 细胞具有独特的转录特征,其中Eomes 是上调最显著的基因之一(图4a)。将该THK特征基因集映射至scRNA-seq数据,发现聚类1(THK)富集评分最高(图4b)。进一步分析显示,在小鼠结肠炎及人类CD4+ T细胞数据中,Gzmk与Eomes 呈现近乎一致的共表达模式(图4c-d);在溃疡性结肠炎患者的bulk RNA-seq数据中,EOMES与GZMK的表达呈最强正相关(图4e)。流式细胞术也证实,结肠炎小鼠的固有层及肠系膜淋巴结中,GzmK-tdTomato+ 细胞与EOMES蛋白显著共表达(图4f)。时间进程分析显示,THK细胞在转移后第14天出现,约3-4周达稳定水平,晚于TH1和TH17细胞。此外,EOMES的表达不依赖于T-bet、STAT6或RORγt,但受Bcl6调控(图4g-j)。ATAC-seq分析显示,GzmK+ 细胞在Eomes、Gzmk、Prf1等THK相关基因座具有更高的染色质可及性,而典型CD4+ 谱系基因(如 Rorc、Il17a)则相反(图4k-l)。基序富集分析表明,T-box家族基序(包括Eomes结合位点)在GzmK+ 细胞的可及性区域中显著富集(图4m)。以上数据表明,Eomes与THK细胞在转录和表观遗传水平上紧密相关,是调控该亚群身份的关键候选因子。
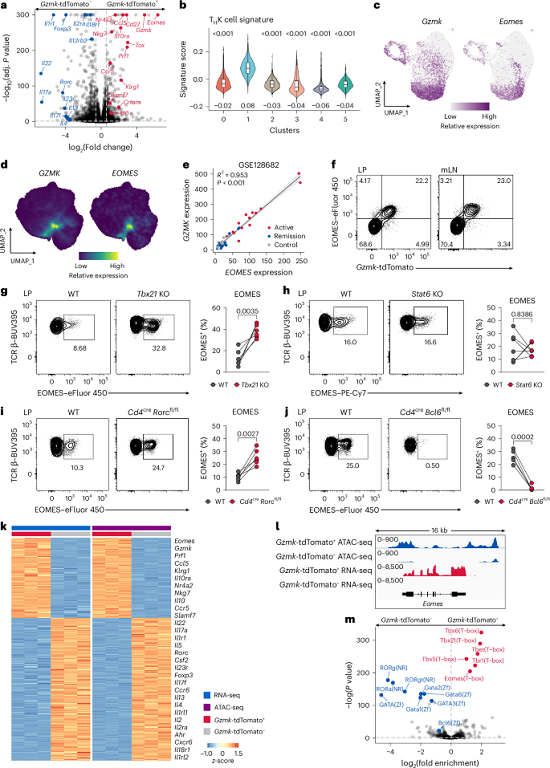
图4. Eomes在转录水平和表观遗传学层面均与THK细胞身份相关
5 EOMES驱动THK命运并限制替代性辅助T细胞谱系
为明确EOMES是否足以诱导THK细胞转录程序,研究团队在非极化条件下活化CD4+ T细胞并逆转录病毒过表达Eomes,随后进行bulk RNA-seq分析。结果显示,与对照相比,Eomes过表达导致1,239个基因上调和1,336个基因下调(图5a)。基因富集分析证实,THK细胞特征在Eomes过表达细胞中显著富集(图5b);将该上调特征映射至结肠炎CD4+ T细胞scRNA-seq数据,发现其在聚类1(THK)中富集程度最高(图5c)。流式细胞术进一步表明,Eomes过表达在非极化条件下显著增加了GzmK-tdTomato及穿孔素的表达(图5d-e)。CUT&Tag实验显示,EOMES直接结合Gzmk和Prf1基因座,且这些区域在THK细胞中染色质可及性增加(图5f-g)。此外,在体外TH1、TH2、TH17及Treg极化条件下,Eomes过表达分别抑制了T-bet、GATA3、RORγt/IL-17A及FOXP3的表达;在OVA免疫模型中,Eomes过表达也抑制了TFH细胞标志物PD-1、CXCR5和BCL6。结肠炎小鼠中,THK细胞几乎不表达BLIMP1。以上数据表明,EOMES不仅直接驱动THK核心程序,同时抑制其他辅助T细胞谱系的分化。
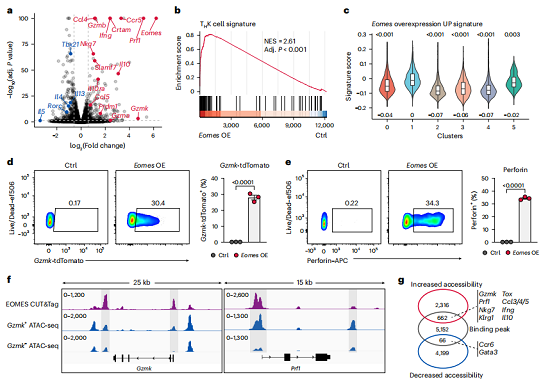
图5. Eomes在转录水平和表观遗传学层面均与THK细胞身份相关
6 Eomes是结肠炎中THK细胞分化所必需的
为确定Eomes是否为THK细胞体内发育所必需,研究团队将Cd4-Cre;Eomesfl/fl(Eomes-cKO)初始CD4+ T细胞与野生型对照共转移至Rag1-/- 受体。结果显示,Eomes-cKO细胞中THK相关基因(Gzmk、Prf1、Nkg7、Slamf7)表达显著降低,THK 特征富集评分下降(图6a-c)。整合多组学数据,共鉴定出18个EOMES直接靶基因,包括Gzmk、Prf1、Ccl5等(图6d-e)。功能上,Eomes-cKO组小鼠结肠炎显著减轻,表现为体重下降减少、结肠缩短缓解及组织学评分降低(图 6f-h)。流式细胞术显示,Eomes缺陷几乎完全消除 GzmK-tdTomato 表达,并显著降低穿孔素水平,但GZMB、T-bet及IFNγ变化有限(图6j-l)。同时,RORγt+ 、IL-17A+ 及 FOXP3+ 细胞频率升高,提示缺乏THK时细胞向替代谱系偏移。相比之下,单独缺失Gzmk并不减轻疾病。以上数据表明,Eomes是THK细胞分化所必需的关键转录因子,其调控的效应程序具有冗余性,靶向EOMES核心网络可能更具治疗潜力。
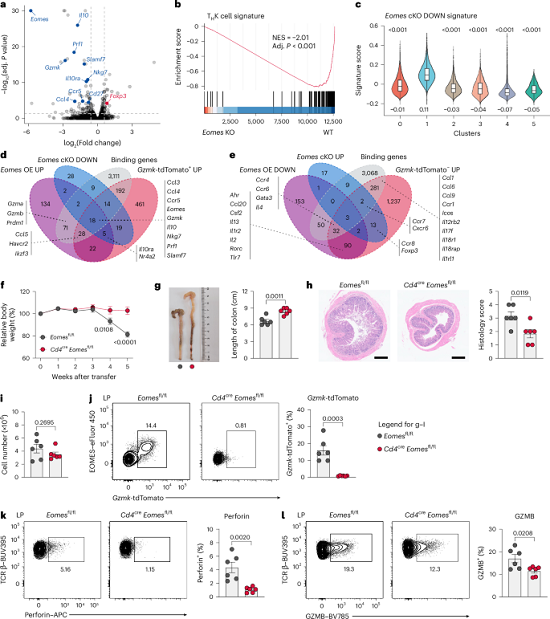
图6. Eomes是THK细胞分化及肠道免疫病理学过程所必需的因子
7 Eomes依赖的THK程序驱动肠道炎症
为评估THK细胞在肠道炎症中的致病作用,研究团队将Eomes-cKO或对照小鼠的初始CD4+ T细胞分别转移至Rag1-/-受体。结果显示,Eomes-cKO组小鼠结肠炎显著减轻,表现为体重下降减少、结肠缩短缓解及组织学炎症评分降低(图6f-h)。两组供体T细胞总数无显著差异,排除增殖或归巢缺陷(图6i)。流式细胞术表明,Eomes缺陷几乎完全消除GzmK-tdTomato表达,并显著降低穿孔素水平,但GZMB、T-bet 及 IFNγ 仅轻度改变(图6j-l)。值得注意的是,Eomes缺陷导致RORγt+ 、IL-17A+及FOXP3+ CD4+ T细胞频率升高,提示THK缺失促使细胞向替代谱系偏移。相比之下,单独缺失Gzmk并不减轻疾病。以上数据表明,Eomes依赖的THK程序是驱动肠道炎症的关键,其致病效应依赖于EOMES下游多个效应分子的协同作用,而非单个GZMK。
总的来说,本研究通过单细胞转录组、多组学分析、基因敲除与过表达、结肠炎模型等多种实验技术方法,发现并系统鉴定了以高表达Gzmk为特征、受转录因子EOMES驱动的CD4+ T细胞新亚群——THK细胞。该细胞独立于经典TH分化通路,且转录程序在人类和小鼠的多种疾病中高度保守。它指明了EOMES-THK细胞作用轴是一个潜在的、富有前景的治疗靶点。针对这一通路的干预,有望为炎症性肠病等T细胞介导的慢性炎症性疾病带来新的精准治疗策略。
关于我们
上海南方模式生物科技股份有限公司(Shanghai Model Organisms Center, Inc.,简称"南模生物"),成立于2000年9月,是一家上交所科创板上市高科技生物公司(股票代码:688265),始终以编辑基因、解码生命为己任,专注于模式生物领域,打造了以基因修饰动物模型研发为核心,涵盖多物种模型构建、饲养繁育、表型分析、药物临床前评价等多个技术平台,致力于为全球高校、科研院所、制药企业等客户提供全方位、一体化的基因修饰动物模型产品解决方案。

