MSTN小鼠模型的药效验证:揭示其与GLP-1联用实现减脂保肌的机制
2026-04-30 来源:本站 点击次数:30当GLP-1受体激动剂的减重热潮逐渐回归理性,其单靶点治疗的一个关键副作用——“显著肌肉流失”开始凸显。据2025年发表在《The Journal of Clinical Endocrinology & Metabolism》的综述指出,GLP-1类药物带来的减重中,约25%至40%源自去脂体重的流失。这一问题催生了“减脂保肌”的新理念,即既要减重,也要保住肌肉。在此背景下,先前因在脊髓性肌萎缩症等肌肉疾病药物开发过程中屡遭挫折(如罗氏Emugrobart于2026年终止相关研发)的MSTN靶点,却在与GLP-1相关药物联用时迎来转机。今天鼠博士就为大家介绍MSTN这一靶点。
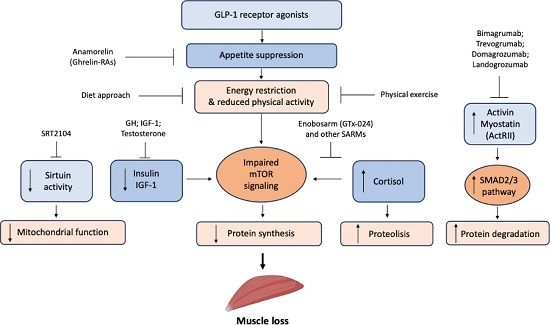
图1. GLP-1受体激动剂治疗相关肌肉流失的主要机制及应对策略[1]。
MSTN介绍
MSTN (肌肉生长抑制素,Myostatin),又称GDF-8 (Growth Differentiation Factor 8),是转化生长因子-β (TGF-β) 超家族的一个关键成员。
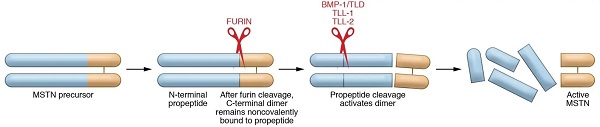
图2. MSTN的产生[2]。
MSTN主要在骨骼肌中高表达,并且在脂肪组织中也有表达。值得注意的是,其在棕色脂肪组织 (BAT) 中的表达对于调节产热和全身能量稳态具有重要作用。MSTN启动子包含多个转录因子结合位点,如MyoD、MEF2、PPARγ和糖皮质激素受体等,这些因子集成各种生理信号来调节其转录。此外,机械负荷、microRNAs (miRNAs) 和长链非编码RNAs (lncRNAs) 也参与其转录后调控。
作为一种重要的分泌型信号分子,MSTN的核心功能是充当骨骼肌生长发育的负向调控因子。MSTN通过抑制成肌细胞增殖和分化,并促进蛋白质降解,进而调控骨骼肌的生长。除此之外,MSTN也是连接肌肉与脂肪代谢的关键节点。它能抑制棕色脂肪组织产热和脂肪酸氧化,并可能通过损害线粒体功能来降低骨骼肌的氧化代谢能力。此外,它还可能通过KLF4/FGF21等因子介导肌肉与脂肪组织间的对话。
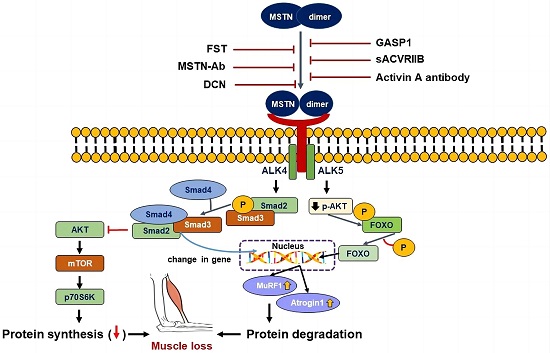
图3. MSTN相关信号传导通路[3]。
MSTN候选药物开发方向
自1997年通过基因敲除小鼠的“双肌 (Double Muscling)”表型被发现以来,MSTN便成为了肌肉生物学、代谢调控及相关疾病治疗研究的核心靶点。
肌肉萎缩症相关疾病药物开发
鉴于MSTN是骨骼肌生长的强效负调控因子,抑制其信号曾被视为治疗脊髓性肌萎缩症(SMA)、杜氏肌营养不良(DMD)等肌肉萎缩症的直接策略。理论上,通过药物阻断MSTN,可为持续萎缩的肌肉创造生长条件,改善运动功能,甚至逆转疾病进程,因而该靶点一度被寄予厚望。
然而,针对肌肉萎缩症相关疾病的MSTN抑制剂开发却屡遭重创。从辉瑞早期终止的Stamulumab,到后续多个在关键临床试验中未达终点的候选分子,实践结果与预期落差巨大。2026年3月,罗氏因疗效不足正式终止了其抗MSTN抗体Emugrobart的研发。研发团队认为MSTN抑制剂失败的主要原因在于,在SMA、DMD等疾病中,肌肉长期缺乏神经支配,单纯增加肌肉体积难以转化为有意义的肌力或功能改善,这使MSTN靶点在原发肌肉萎缩领域至今未能取得成功。
代谢减重领域药物开发
近年来,MSTN靶点的研究重点正在发生关键转移,即从单纯“增肌”转向评估其在代谢稳态中的系统性作用。在目前GLP-1类药物盛行的背景下,为了对抗快速减重带来的肌肉流失,优化身体成分,MSTN抑制剂类药物与GLP-1类药物联用的疗法开发被提上日程。目前药物披露数据显示:Apitegromab 联合替尔泊肽,比单用减重药多保留了约54.9%的瘦体重;而 Trevogrumab 联合司美格鲁肽可使因药物流失的瘦体重减少约一半。这一系列围绕肥胖症保肌的积极数据,不仅证明了抑制MSTN在特定场景下对肌肉显著的保留作用,也证明了其不会干扰减脂效果。这标志着MSTN靶点的研发逻辑彻底完成了从“治疗衰竭”到“预防流失”的转变。同时,siRNA等新一代基因沉默技术正处在早期研发阶段,旨在实现更长效、更精准的MSTN调控。
南模生物相关小鼠模型
南模生物长期致力于代谢类药物靶点人源化小鼠模型的开发,自主研发了一系列MSTN靶点人源化小鼠模型,为相关药物的药效评估和安全性评价提供了强有力的工具。
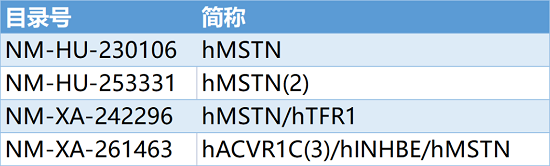
表1. MSTN相关靶点人源化小鼠
hMSTN mouse(NM-HU-230106)
-
正常饮食下hMSTN小鼠的代谢药物药效评价
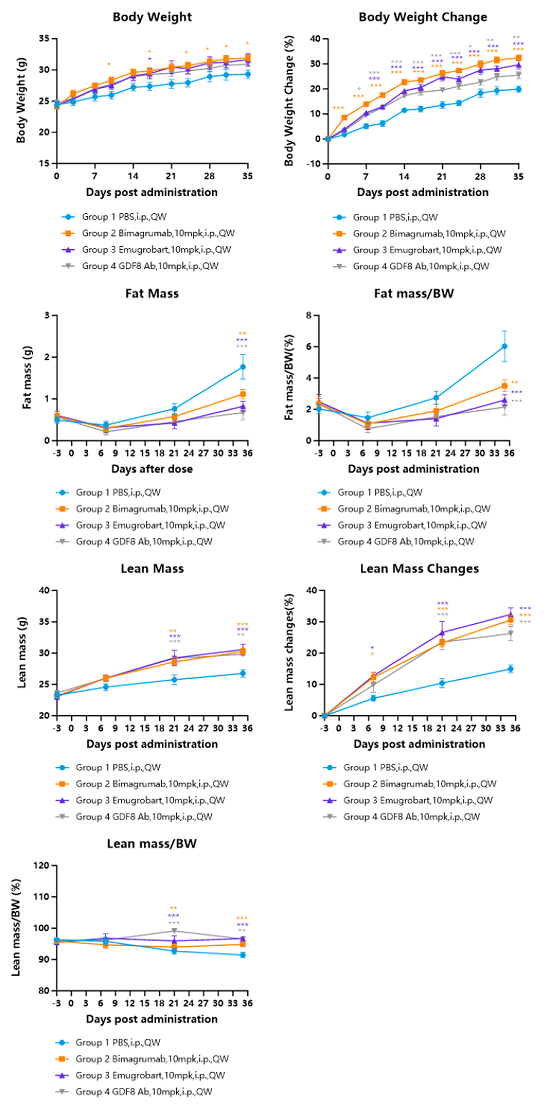
图1. Bimagrumab、Emugrobart与MSTN(GDF8)抗体的在正常饮食的hMSTN小鼠上的药效检测。
结果表明MSTN受体抗体与MSTN抗体均可促进普通饲料喂食hMSTN小鼠(6weeks,n=7)肌肉含量,减少小鼠脂肪含量。
-
高脂饮食下hMSTN小鼠的代谢药物药效评价
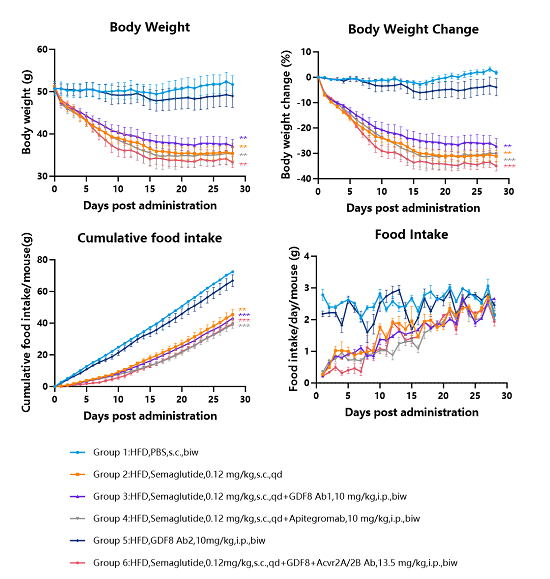
图2. Semaglutide与MSTN(GDF8)抗体、MSTN受体抗体连用在高脂饮食的hMSTN小鼠上的体重变化与进食检测。
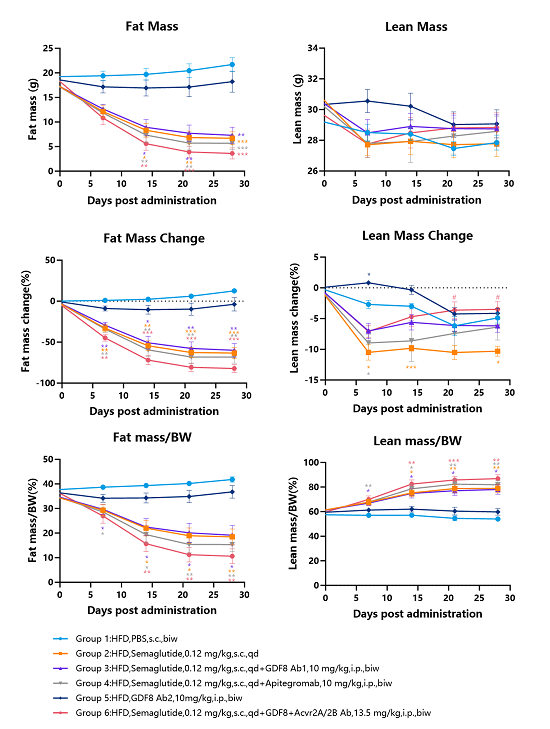
图3. Semaglutide与MSTN(GDF8)抗体、MSTN受体抗体连用在高脂饮食的hMSTN小鼠上的脂肪肌肉变化检测。
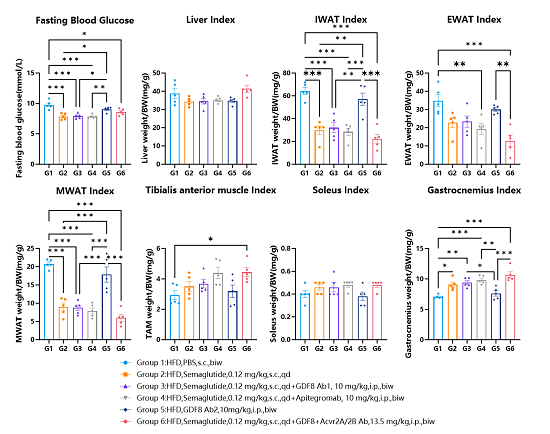
图4. Semaglutide与MSTN(GDF8)抗体、MSTN受体抗体连用在高脂饮食的hMSTN小鼠上的各组织指数检测。
结果表明Semaglutide与MSTN(GDF8)抗体联用,虽然无法增加Semaglutide的减重效果,但能显著减少肌肉流失。
Semaglutide与MSTN(GDF8)抗体、MSTN受体抗体联用能更进一步增强减重效果,且更显著减少肌肉流失。
Reference:
[1] Rossi, G., Bucciarelli, L., Mananguite, CL. et al. Muscle loss and GLP-1R agonists use. Acta Diabetol 63, 333–342 (2026).https://doi.org/10.1007/s00592-025-02611-2
[2] Rossi, G., Bucciarelli, L., Mananguite, CL. et al. Muscle loss and GLP-1R agonists use. Acta Diabetol 63, 333–342 (2026).https://doi.org/10.1007/s00592-025-02611-2
[3] Baig MH, Ahmad K, Moon JS, Park S-Y, Ho Lim J, Chun HJ, Qadri AF, Hwang YC, Jan AT, Ahmad SS, Ali S, Shaikh S, Lee EJ and Choi I (2022) Myostatin and its Regulation: A Comprehensive Review of Myostatin Inhibiting Strategies. Front. Physiol. 13:876078. doi: 10.3389/fphys.2022.876078
关于我们
上海南方模式生物科技股份有限公司(Shanghai Model Organisms Center, Inc.,简称"南模生物"),成立于2000年9月,是一家上交所科创板上市高科技生物公司(股票代码:688265),始终以编辑基因、解码生命为己任,专注于模式生物领域,打造了以基因修饰动物模型研发为核心,涵盖多物种模型构建、饲养繁育、表型分析、药物临床前评价等多个技术平台,致力于为全球高校、科研院所、制药企业等客户提供全方位、一体化的基因修饰动物模型产品解决方案。

