ATAC-seq助力探究RBM22打破心肌细胞增殖壁垒,为心衰治疗开辟新路径
2026-04-27 来源:本站 点击次数:75

期刊:Nature communications
影响因子:15.7
发表时间:2026年3月
通讯作者:上海交通大学医学院附属仁济医院占贞贞
伯豪生物技术服务:ATAC-seq
科学问题
成年哺乳动物心肌细胞在心肌梗死(MI)后会发生不可逆丢失,而内源性心肌细胞的增殖再生能力极度微弱,无法弥补损伤造成的细胞缺失,是心室病理性重构、心力衰竭进展乃至死亡的核心原因。目前临床现有治疗手段仅能缓解心衰症状,无法实现功能性心肌的再生修复。染色质重塑如何精准调控心肌细胞的细胞周期重启与增殖过程?RNA结合基序蛋白22(RBM22)在心脏再生与损伤修复中扮演何种角色、其背后的分子机制是什么?这些问题尚未得到阐明,也是心肌再生领域亟待突破的关键科学瓶颈。
患者队列与样本处理
样本分组:新生小鼠心尖切除(AR)模型、新生及成年小鼠心肌梗死(MI)模型;心肌细胞特异性Rbm22组成型条件敲除小鼠、他莫昔芬诱导型Rbm22条件敲除(iCKO)小鼠。
细胞模型:原代新生/成年小鼠心肌细胞、人诱导多能干细胞来源心肌细胞(hiPSC-CMs)。
技术服务
ATAC-seq
(技术服务由伯豪生物提供)
主要研究
1. RBM22的动态表达模式与心肌再生潜能高度关联
研究团队通过跨物种转录组整合分析,筛选出7个在心脏出生后成熟过程中持续下调、而心肌损伤后显著重新激活的RBM家族基因,其中RBM22的损伤诱导上调幅度最为显著。
研究发现,RBM22的蛋白表达水平在小鼠出生后1天至7天持续下降,与新生小鼠心脏再生窗口的关闭进程完全吻合;而在新生小鼠心尖切除或心肌梗死后,RBM22在心肌细胞中发生显著上调,且主要富集于梗死周边区。同时,RBM22的表达与心肌细胞增殖标志物(Pcna、Mki67)呈显著正相关,与细胞周期抑制因子呈负相关,体外缺氧刺激同样可显著诱导心肌细胞中RBM22的表达,提示其与心肌细胞增殖、心脏再生潜能密切相关。
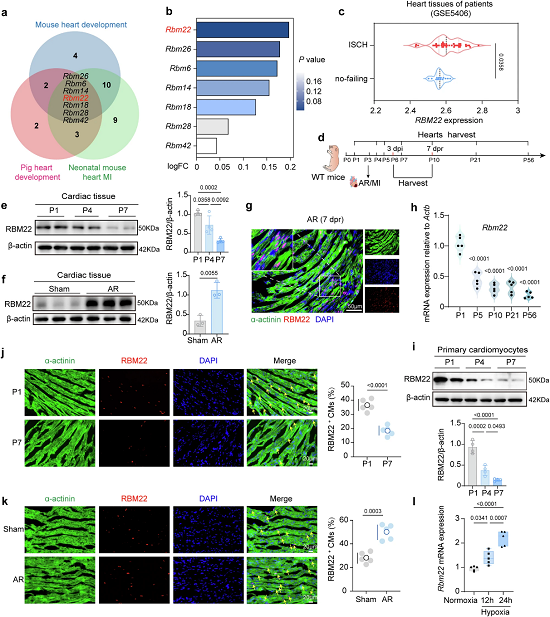
图1. RBM22在心脏发育及损伤后的表达谱
2. RBM22缺失严重损害新生及成年小鼠的心脏再生能力
为明确RBM22在心脏再生中的功能,研究团队构建了心肌细胞特异性Rbm22敲除小鼠模型。结果显示,心肌细胞中Rbm22的缺失会完全阻断新生小鼠心尖切除与心肌梗死后的心脏再生过程,导致小鼠心功能显著恶化、心肌纤维化面积大幅增加,再生能力完全丧失。
进一步的机制验证发现,Rbm22敲除后,心肌细胞的EdU、pH3、Aurora B阳性率显著下降,意味着心肌细胞的细胞周期进入、有丝分裂与胞质分裂过程均被全面抑制,心肌细胞总数减少、体积代偿性增大。而在成年小鼠心肌梗死模型中,心肌细胞特异性Rbm22缺失同样会加剧心室病理性重构与心功能恶化,显著抑制梗死周边区心肌细胞的增殖活性,减少具有增殖潜能的单核二倍体心肌细胞比例,证实RBM22是维持心肌细胞增殖能力、介导心脏损伤修复的关键必需分子。
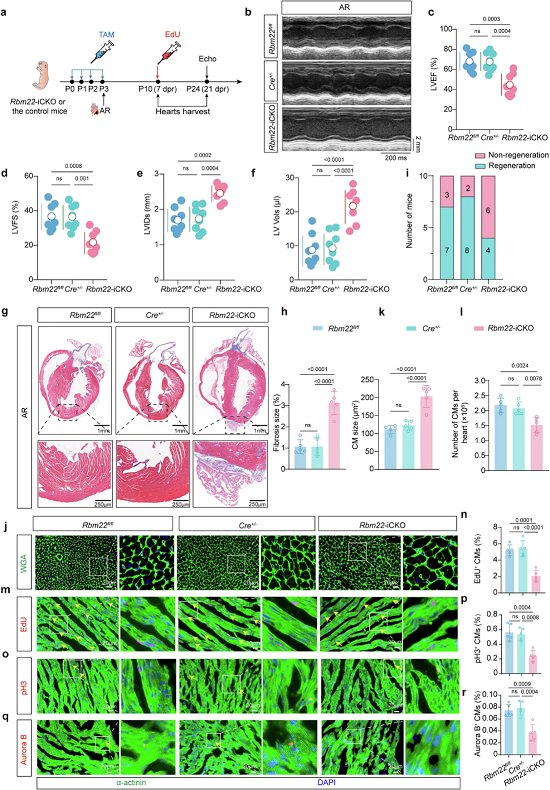
图2. RBM22是心肌细胞增殖和新生心脏再生所必需
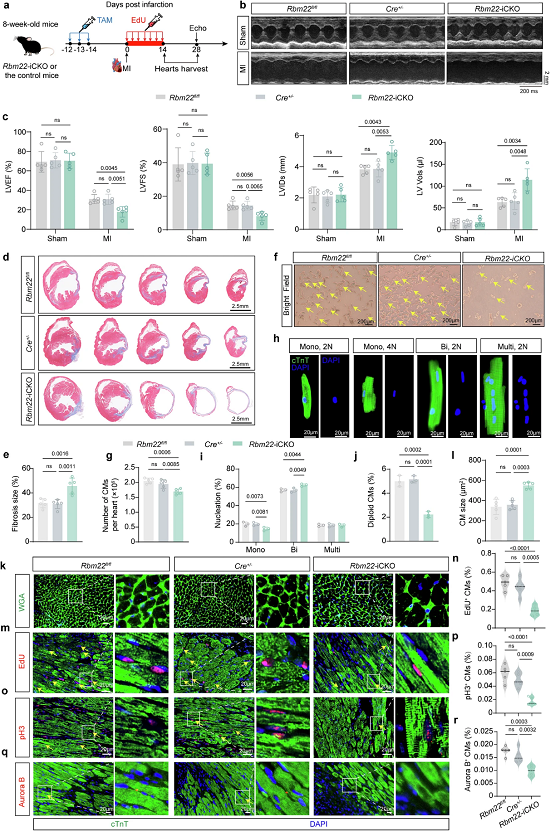
图3. Rbm22基因敲除通过抑制成年小鼠心肌梗死后心肌细胞增殖而损害心肌修复
3. RBM22通过直接转录激活关键细胞周期基因驱动心肌增殖
为解析RBM22调控心肌细胞增殖的分子机制,研究团队对RBM22敲低的原代心肌细胞进行了RNA-seq分析。结果显示,Rbm22缺失会导致DNA复制、细胞周期相关通路的基因发生显著富集性下调,其中核心细胞周期调控基因Cdk4、Ccna2、Ccne1的表达下降最为显著。
令人意外的是,研究发现RBM22并非通过经典的RNA结合蛋白功能——调控mRNA稳定性或可变剪接来发挥作用。亚细胞分级实验证实,RBM22大量富集于心肌细胞的染色质组分中;CUT&Tag测序与ChIP-qPCR进一步验证,RBM22可选择性地直接结合到Cdk4、Ccna2、Ccne1等关键细胞周期基因的近端启动子区域,通过序列特异性结合直接激活这些基因的转录,而不结合管家基因与细胞周期抑制基因的启动子,展现出高度的基因靶向特异性。
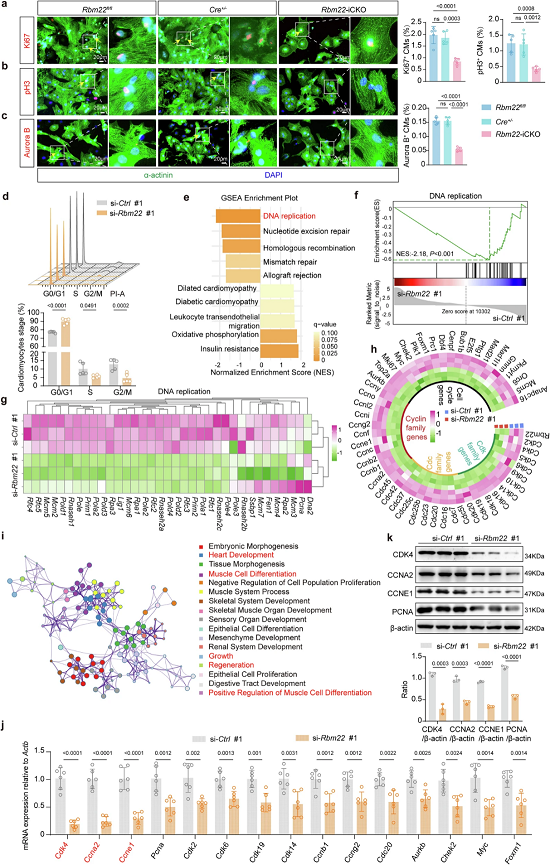
图4. Rbm22缺失导致细胞周期基因转录下调
4. RBM22招募SMARCA4重塑染色质可及性,突破增殖的表观遗传屏障
成年心肌细胞难以重启增殖的核心障碍之一,是细胞周期基因启动子区域的染色质高度浓缩、可及性极低,转录机器无法结合。研究团队通过ATAC-seq发现,RBM22敲低会导致大量细胞周期基因启动子区域的染色质可及性显著降低,而RBM22过表达则能显著开放这些位点的染色质状态。
进一步的分子互作实验揭示了其背后的机制:RBM22可通过其脯氨酸富集结构域,与SWI/SNF染色质重塑复合物的核心ATP酶亚基SMARCA4发生直接蛋白互作,将SMARCA4特异性招募至Cdk4、Ccna2、Ccne1等基因的启动子区域。SMARCA4通过ATP依赖的核小体重塑,开放这些基因启动子的染色质构象,进而促进RNA聚合酶II的招募与转录起始,从表观遗传层面打破了心肌细胞的增殖阻滞。
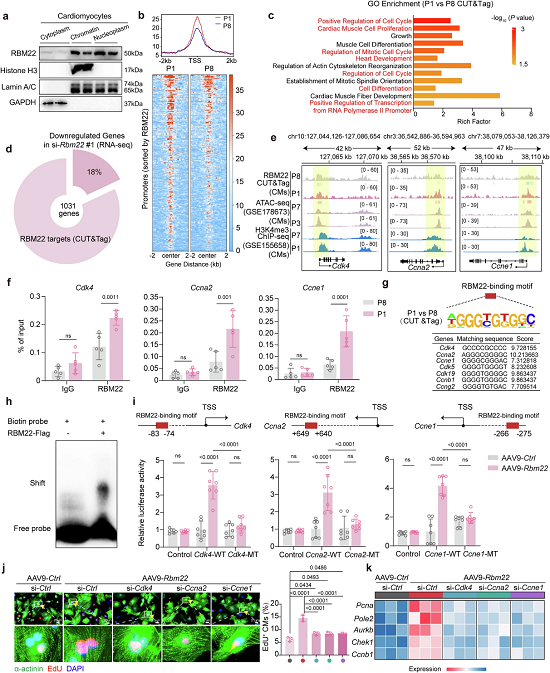
图5. RBM22选择性结合细胞周期基因的近端启动子以激活转录
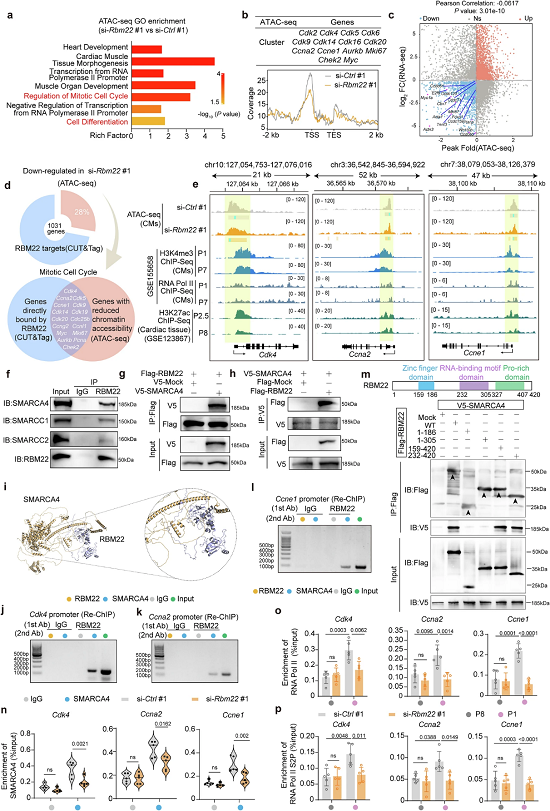
图6. RBM22与SMARCA4相互作用以增加细胞周期基因启动子的染色质可及性
5. AAV9-RBM22基因治疗显著改善成年小鼠心梗后心脏修复
基于上述机制发现,研究团队探索了RBM22作为治疗靶点的临床转化潜力,构建了心肌细胞特异性cTnT启动子驱动的AAV9-Rbm22递送系统,在成年小鼠心肌梗死模型中进行体内干预。
实验结果显示,心梗后心肌内注射AAV9-Rbm22可显著上调梗死周边区心肌细胞的RBM22表达,大幅提升EdU、Ki67阳性的增殖心肌细胞比例;长期随访发现,RBM22基因治疗可显著提升小鼠左心室射血分数(LVEF)、短轴缩短率(LVFS)等核心心功能指标,减少左心室扩张与心肌纤维化面积,增加心肌细胞总数与单核二倍体心肌细胞比例,有效逆转了心梗后的心力衰竭进程。
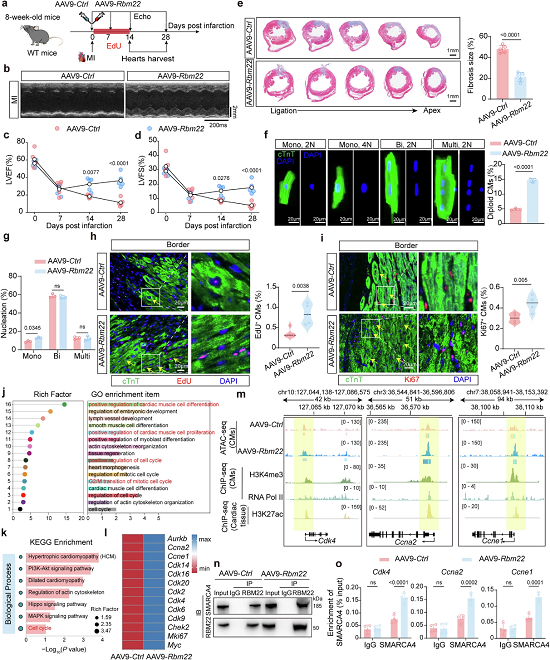
图7. AAV9-Rbm22基因治疗促进成体心脏修复
6. RBM22可高效驱动人源心肌细胞增殖,具备坚实的临床转化价值
啮齿类动物的研究结果能否转化至人类,是心肌再生疗法的核心考验。研究团队证实,人与小鼠的RBM22蛋白序列具有高度保守性,在hiPSC-CMs中过表达RBM22,可显著增加EdU、Aurora B阳性的增殖心肌细胞比例,有效驱动人源心肌细胞重新进入细胞周期并完成胞质分裂。
同时,RBM22过表达可显著上调hiPSC-CMs中CDK4、CCNA2、CCNE1等细胞周期基因的表达,下调心肌成熟相关标志物,证实其在人源心肌细胞中同样具备强大的促增殖活性,为该靶点从基础研究走向临床应用奠定了坚实的实验基础。
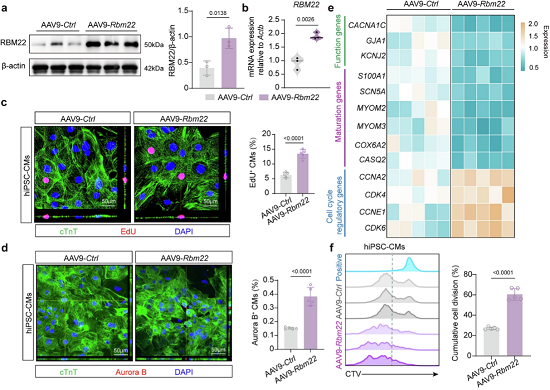
图8. RBM22促进人源心肌细胞增殖
结论
本研究系统解析了RBM22在维持心脏再生能力中的核心作用,首次阐明了RBM22通过招募SMARCA4介导染色质重塑,特异性打开细胞周期基因的“转录开关”,从而帮助心肌细胞重新进入细胞周期的全新机制。
同时,研究验证了AAV9介导的RBM22基因治疗在成年动物心梗模型中的显著疗效,以及在人源心肌细胞中的促增殖活性,为终末期心力衰竭的再生医学治疗提供了全新的靶点与极具转化潜力的干预方案,为攻克心脏损伤后缺乏再生能力这一临床顽疾提供了极具潜力的治疗思路。
参考文献:
1. Duan X, Tan Y, Zhang Y, et al (2026) Restoration of RBM22 overcomes the transcriptional and epigenetic barriers of cardiomyocyte proliferation for heart regeneration. Nat Commun 17:3684. https://doi.org/10.1038/s41467-026-70235-3

