单细胞及空间转录组揭示中性粒细胞在肿瘤微环境中的促转移新机制
2026-04-29 来源:本站 点击次数:66
期刊:Nature
影响因子:48.5
通讯作者:Jose M. Adrover、Mikala Egeblad
通讯单位:美国冷泉港实验室
主要技术:单细胞 RNA 测序,空间转录组测序
科学问题
中性粒细胞在肿瘤微环境中如何调控肿瘤血管功能、组织坏死与远处转移?三者之间是否存在因果关联?能否通过靶向中性粒细胞打破这一促肿瘤循环?
实验材料和方法
1. 动物模型
多种小鼠自发 / 移植肿瘤模型(乳腺癌、肺癌、胰腺癌等)
2. 临床样本
人乳腺癌、肺癌组织样本
3. 多组学技术
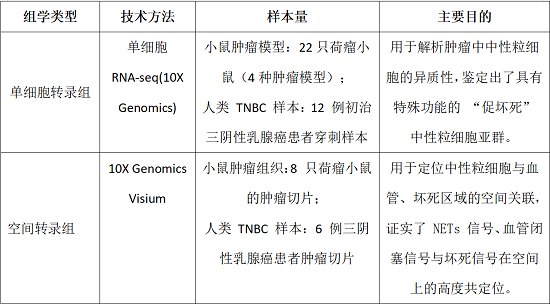
导语
肿瘤的 “坏死” 与 “转移”,一直是临床肿瘤治疗中最棘手的两大难题:为什么有的肿瘤内部会出现大片坏死?坏死又为何常常和肿瘤的远处转移 “绑定出现”?背后的共同元凶是什么?这篇发表在《Nature》的重磅研究,首次完整揭示了中性粒细胞在肿瘤微环境中的 “双面杀手” 角色—— 它不仅会堵塞肿瘤血管、直接造成肿瘤坏死,还会通过坏死组织释放的信号,主动 “护送” 肿瘤细胞完成转移,为靶向中性粒细胞的抗肿瘤治疗开辟了全新方向。
主要技术
单细胞 RNA 测序、空间转录组测序
研究结果
1. 中性粒细胞在肿瘤血管内形成物理闭塞
通过活体双光子显微镜首次直接观察到,中性粒细胞会在肿瘤血管内快速聚集,与NETs、血小板及肿瘤细胞碎片共同形成聚集体,物理堵塞血管腔,导致肿瘤组织血流灌注下降。多色免疫荧光染色进一步确认,MPO与citH3双阳性的中性粒细胞及NETs簇分布于CD31标记的血管内皮周围,呈现血管内聚集体引发闭塞的原位形态。
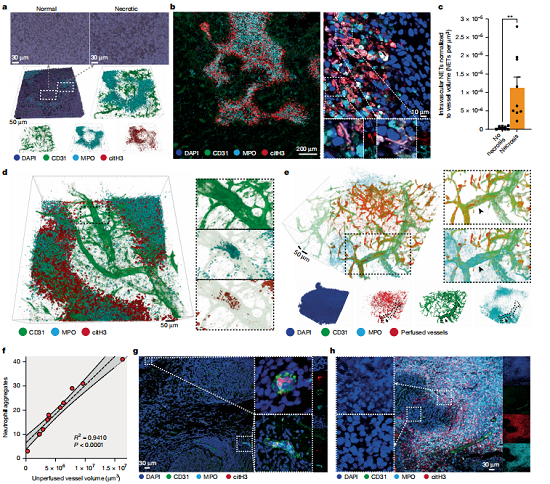
图 1 活体成像揭示中性粒细胞介导的肿瘤血管闭塞
2. 定位中性粒细胞、NETs与坏死区的共谋
研究者利用10x Genomics Visium空间转录组技术,对肿瘤组织进行微米级空间定位。空间转录组图谱清晰将组织划分为坏死区、坏死周边区与非坏死区。中性粒细胞特征基因S100a8、S100a9、Cst3r的表达信号,与NETs相关信号、坏死特征基因及缺氧信号在空间位置高度重合,从而在原位分子层面证明中性粒细胞及其释放的NETs是诱导肿瘤坏死的空间核心。同时,功能富集分析显示,坏死区域显著富集EMT、细胞迁移、伤口愈合等促进转移通路基因,提示该微环境与肿瘤恶性进展直接相关。
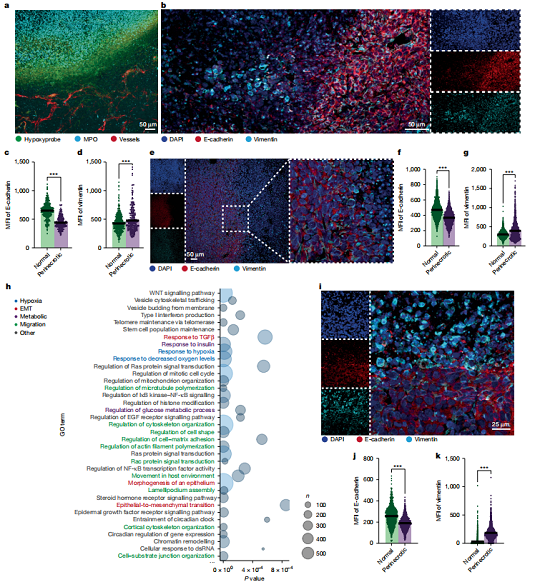
图2 坏死周围癌细胞获得促转移特性
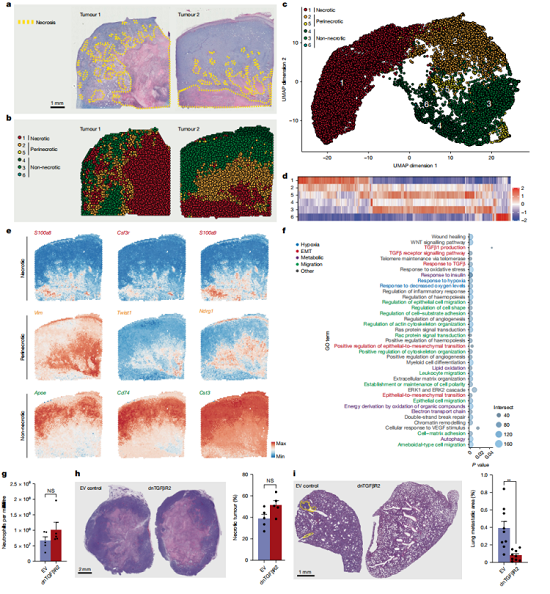
图3 空间转录组图谱证实中性粒细胞与坏死区的偶联
3. 单细胞测序鉴定血管限制性中性粒细胞
对荷瘤小鼠骨髓中性粒细胞进行单细胞RNA测序,发现一个肿瘤诱导的独特亚群:Ly6GᴴiᵍʰLy6Cᴸᵒʷ。其转录特征与经典Ly6Cᴴiᵍʰ亚群相反:迁移相关基因(Cxcr2、Itgb2、S100a8)显著下调,而NETs相关基因(Pad4、Elane、Mpo)及黏附分子(Icam1、Itgax)上调。功能验证证实:Ly6Cᴸᵒʷ细胞对趋化因子fMLP和IL-1β的跨内皮迁移能力严重受损,但在PMA刺激下NETs释放效率更高,且与血小板黏附更强。单细胞测序精准定位了这群“血管限制性”中性粒细胞——因迁移缺陷滞留血管腔,凭借高NETs能力成为闭塞的直接执行者。
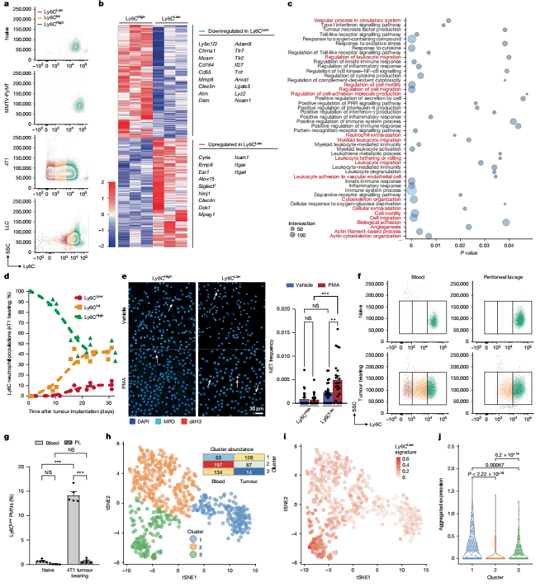
图4 NETs 的释放助力肿瘤细胞逃逸与远处定植
4. 坏死组织信号触发中性粒细胞的持续招募
单细胞测序发现4T1肿瘤高表达CXCL1,驱动骨髓紧急造血,增加Ly6Cᴸᵒʷ中性粒细胞输出。敲除CXCL1后,循环中性粒细胞减少,血管内聚集和坏死显著减轻。空间转录组则显示坏死周边巨噬细胞是TGFβ的主要来源。阻断TGFβ信号抑制EMT和转移但不影响坏死。两类测序技术共同描绘了坏死自我扩大的信号网络。
5. NETs降解基质并协助癌细胞远处定植
为确立NETs的因果作用,研究者采用多种干预:PAD4敲除鼠无法形成NETs,肿瘤坏死减少70%,肺转移显著下降;DNase I降解NETs同样减轻坏死和转移;GSK484抑制NETs但不影响肿瘤生长,说明NETs促转移不依赖增殖;清除中性粒细胞则完全阻断血管闭塞、坏死和转移。机制上,NETs携带的弹性蛋白酶和基质金属蛋白酶可降解血管基底膜,为癌细胞跨血管定植开辟通道。
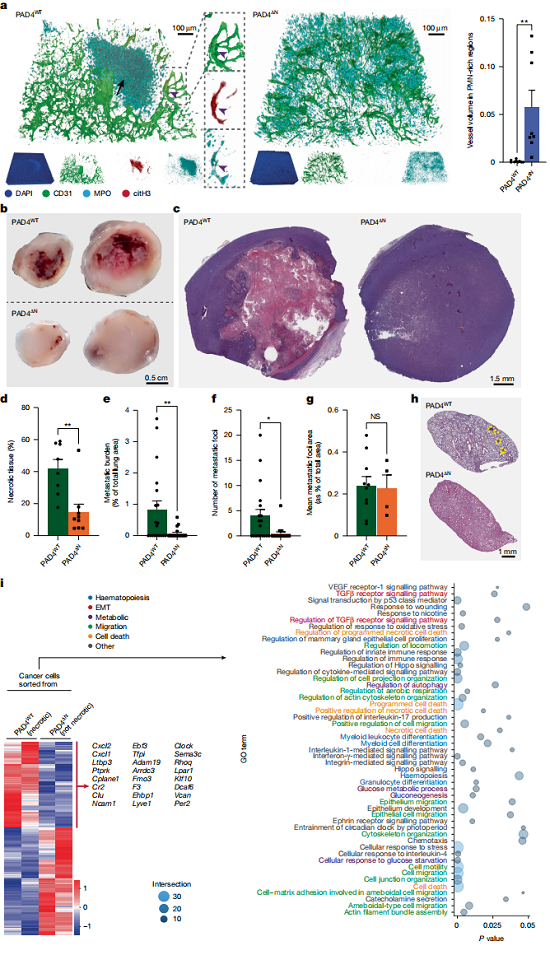
图5 靶向 NETs 通路抑制肿瘤坏死并改善患者预后
6. 靶向NETs通路展现双重治疗获益
靶向NETs通路多个节点均能同时抑制坏死和转移:敲除CXCL1、阻断E/P选择素、PAD4敲除或DNase I、清除中性粒细胞。阻断TGFβ则仅抑制转移。相比完全清除中性粒细胞(增加感染风险),靶向NETs生成或CXCL1—CXCR2轴更具转化前景,可实现特异性抑制“病理型”中性粒细胞。
结论
本研究通过活体成像、多组学分析与临床队列验证,首次系统阐明了中性粒细胞驱动肿瘤血管堵塞、坏死与转移的完整机制链:中性粒细胞通过在肿瘤血管内形成聚集体引发血管堵塞与肿瘤坏死,坏死组织进一步招募更多中性粒细胞,而坏死区域的中性粒细胞又通过释放 NETs 促进肿瘤细胞侵袭与转移,形成持续放大的促肿瘤循环。该研究打破了以往对中性粒细胞在肿瘤中单一作用的认知,将肿瘤坏死与转移这两个看似独立的临床现象通过中性粒细胞串联起来,为开发靶向中性粒细胞或 NETs 的抗肿瘤治疗提供了全新的理论基础与转化方向。
参考文献:
Adrover JM, Han X, Sun L, et,al. Neutrophils drive vascular occlusion, tumour necrosis and metastasis. Nature. 2025 Sep;645(8080):484-495. doi: 10.1038/s41586-025-09278-3.

