利用MOIS HT揭示“减胆固醇”纳米疫苗的淋巴结靶向关键证据
2026-05-07 来源:本站 点击次数:155肿瘤免疫治疗的核心理念之一是激活患者自身的免疫系统去攻击癌细胞。树突状细胞(Dendritic Cells, DCs)作为专业的抗原呈递细胞,在这一过程中扮演着“侦察兵”和“信号官”的双重角色——它们摄取肿瘤抗原,加工处理后呈递给T细胞,启动特异性免疫应答。
然而,肿瘤微环境中的树突状细胞常常处于功能失调状态,导致癌症疫苗效果大打折扣。尽管近年来研究人员尝试了多种策略来增强DC功能——包括促进抗原的溶酶体逃逸与胞质递送、调控DC亚群向免疫刺激表型极化、以及增强DC-T细胞相互作用——但一个能够同时整合抗原递送、膜调控和突触增强的“全能型”纳米平台始终缺失。
2026年4月16日, Nature Nanotechnology在线发表了一项来自华中农业大学金红林教授研究团队的最新成果。研究者发现:树突状细胞膜的胆固醇水平是调控抗原呈递的“隐形开关”。基于这一发现,他们开发了一种名为NPCM-OT的聚乳酸基纳米疫苗,通过甲基-β-环糊精(MeβCD)原位消耗DC膜胆固醇,显著增强了免疫突触的形成和T细胞活化,在黑色素瘤、肺转移瘤、乳腺癌等多种模型中展现出强大的抗肿瘤效果。

01 从临床困惑到机制突破:为何高DC浸润反而预后更差?
研究团队首先分析了TCGA黑色素瘤数据集,发现一个反直觉的现象:肿瘤组织中DC浸润程度高的患者,其总生存期反而更差。差异基因表达和基因集富集分析显示,这些高浸润DC中胆固醇合成和膜胆固醇稳态相关通路显著富集。换句话说,这些DC虽然数量多,但功能被“锁死”了——膜胆固醇代谢紊乱使它们无法有效激活T细胞。为了验证这一点,研究者将B16F10黑色素瘤小鼠的DC分别在体外补充或消耗胆固醇后回输,联合PD-1抗体治疗。结果令人印象深刻:胆固醇补充组肿瘤生长几乎不受抑制,与PBS对照组无异;而胆固醇消耗组则显著抑制肿瘤生长,瘤内CD8⁺ T细胞、IFN-γ⁺/TNF-α⁺双功能性T细胞以及效应记忆T细胞比例均明显升高。这提示,膜胆固醇不是一个简单的代谢产物,而是一个可被靶向的免疫调节节点。
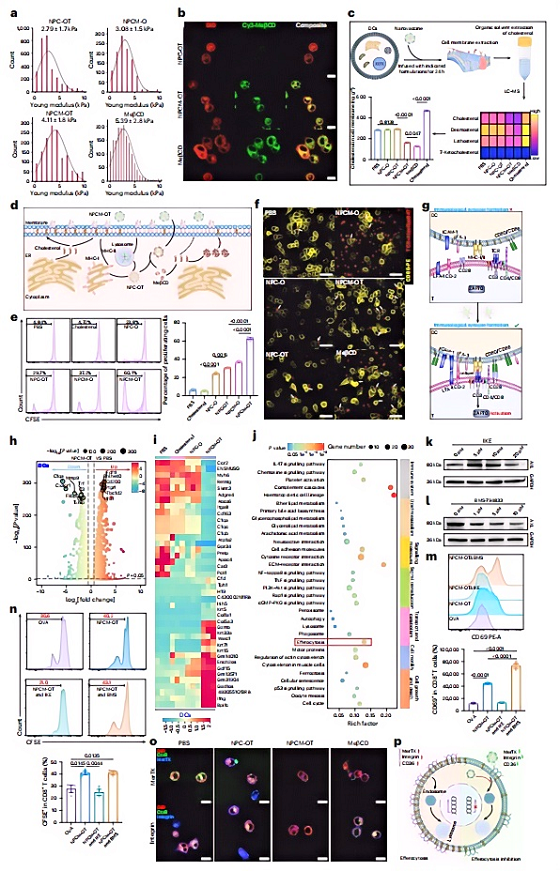
图1.Fig 1 耗竭树突状细胞(DC)膜胆固醇可通过抑制胞吐作用,增强抗原呈递细胞(APCs)与T细胞之间的免疫突触形成
02 纳米疫苗的精密设计:一个平台、四个功能
基于上述发现,研究者构建了一个多功能纳米平台-NPCM-OT。聚乳酸-吡咯啉-钴离子(PDLLA-PPa-Co²⁺)作为骨架,通过疏水相互作用装载胆固醇修饰的CpG佐剂和MeβCD,再通过Co²⁺配位连接组氨酸标签化的OT-I/OT-II抗原肽以及TATk穿膜肽。
稳定性实验表明,在10%小鼠血清中72小时后仍有超过50%的抗原肽保持装载状态。这种设计确保了四个核心功能模块能够同时到达同一靶细胞:抗原提供T细胞表位,CpG激活先天免疫,MeβCD消耗膜胆固醇,TATk增强细胞摄取和淋巴结穿透。
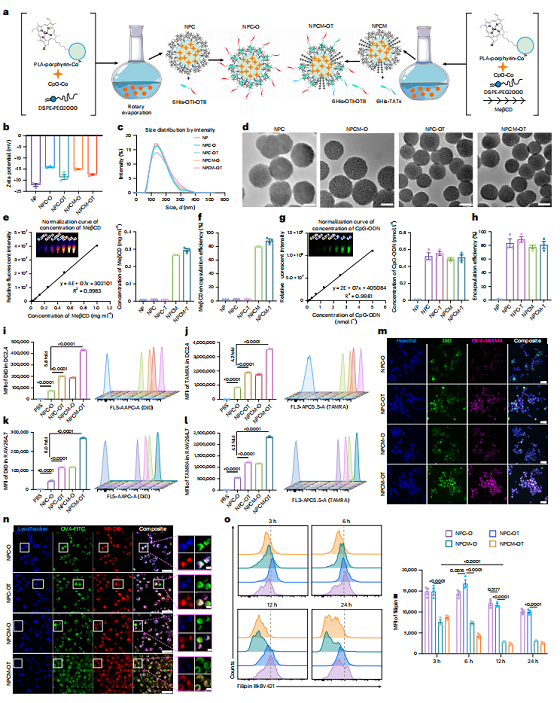
图2.Fig 2 NPCM -OT的制备、表征、靶向作用及胆固醇耗竭效应
03 机制解析:从膜刚性增加到免疫突触稳定
在细胞水平上,NPCM-OT展现了突出的DC摄取能力。双荧光追踪显示,其摄取效率是基础配方NPC-O的5.8倍,并且能够高效逃逸溶酶体——这意味着抗原更有可能进入MHC-I类交叉呈递途径,激活CD8⁺ T细胞。
更重要的是,含MeβCD的配方可选择性消耗DC膜胆固醇(而非总细胞胆固醇),Cy3标记的MeβCD在2小时内即定位于质膜区室。原子力显微镜测量表明,胆固醇消耗后DC膜的杨氏模量从约2.8 kPa升至4.1 kPa,即膜刚性增加。这一变化看似细微,对免疫突触形成却至关重要。当NPCM-OT处理的DC与OT-I CD8⁺ T细胞共培养时,共聚焦显微镜下可见TCR与CD86在DC-T细胞接触界面显著共定位,T细胞活化标记CD69和增殖标记CFSE稀释均呈现数倍的增强。
NPCM-OT要在体发挥效果,必须在引流淋巴结中被DC摄取,而非滞留在注射局部或被非特异性清除。这是整个免疫启动链中最关键、也最难直接验证的一环。研究者对同一批小鼠进行了长达三天的连续活体追踪,分别在6、12、24、48和72小时采集腹股沟引流淋巴结的荧光信号。成像结果显示,不含MeβCD和TATk的NPC-O组信号微弱且很快衰减;而NPCM-OT组在6小时即出现可检测的信号,24至48小时达到峰值,72小时仍有明显残留。通过定量分析后发现,NPCM-OT组的淋巴结荧光强度是NPC-O组的数倍以上。这一动态数据首次直观地证明,TATk和MeβCD具有协同促进淋巴结蓄积的作用,而且游离的MeβCD或单个组分均无法实现这种高效的靶向。
转录组学进一步揭示了一条全新的调控轴:膜胆固醇消耗 → 抑制转录因子Myc和Klf2 → 下调胞葬作用受体(MerTK、整合素、CD36)→ 抑制胞葬作用 → 增强DC成熟、抗原呈递和免疫突触形成。使用胞葬作用抑制剂BMS-794833可模拟NPCM-OT的效果,而激活剂IKE则逆转其作用,基因敲低MerTK或Timd4也获得了类似的结果。这些数据将膜胆固醇、胞葬作用和T细胞活化三个看似不相关的领域联系在了一起。
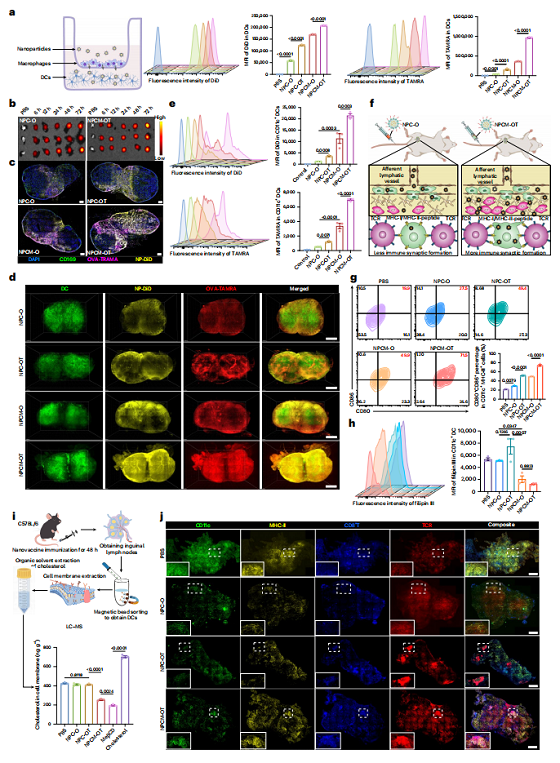
图3.Fig 3 评估 NPCM -OT浸润淋巴结及诱导免疫突触形成的能力
04 体内疗效:预防模型中90%生存率,联合治疗协同增效
在预防性疫苗模型中,提前两周免疫两次NPCM-OT的小鼠在接种B16-OVA黑色素瘤后,肿瘤生长被显著抑制,60天生存率达到90%,而对照组(PBS、NPC-O、NPCM-O、NPC-OT)的生存率均未超过20%。采用TRP-1抗原替代OVA同样有效,证明该平台具有抗原通用性。T细胞耗竭实验表明,CD4⁺和CD8⁺ T细胞共同介导了保护作用,两者同时耗竭则疗效完全消失;使用FTY720阻断淋巴细胞从淋巴结向外周循环的归巢,同样废除了疫苗的保护效果。这证实,淋巴结内T细胞的初始启动是疗效的核心,而非外周局部效应。
在治疗性模型中,研究者采用了更接近临床的场景:静脉注射B16F10细胞建立肺转移模型,然后在第4、10、17天给予NPCM-TT(含TRP-1抗原)联合PD-1抗体治疗。结果显示,联合治疗组的肺转移结节数显著少于PBS、单药或单用纳米疫苗组。免疫荧光和流式细胞术证实,联合治疗增加了转移灶中CD8⁺ T细胞、CD4⁺ T细胞和CD11c⁺ DC的浸润,同时提高了活化cDC1、TNF-α⁺/Granzyme B⁺/IFN-γ⁺效应T细胞的比例,降低了PD-1⁺耗竭T细胞。在4T1乳腺癌模型中同样观察到了肿瘤抑制和Th1极化,同时瘤内调节性T细胞和髓源性抑制细胞减少。这些数据表明,膜胆固醇消耗策略与免疫检查点抑制剂具有天然的协同潜力。
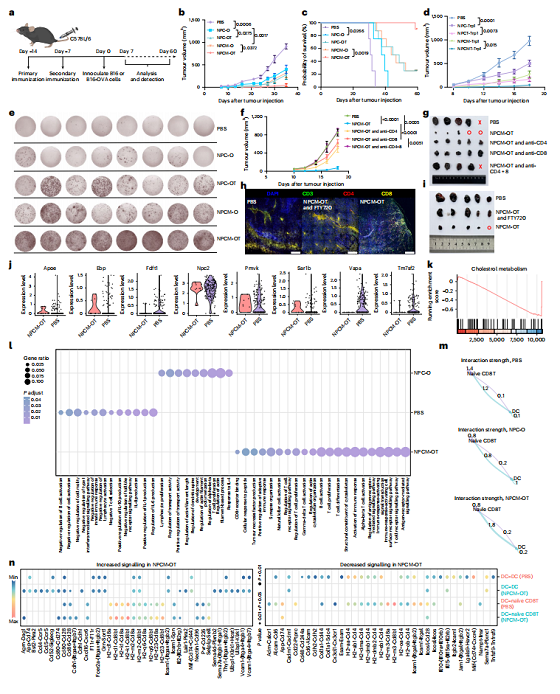
图4.Fig 4 NPCM -OT肿瘤预防能力及其作用机制的体内验证
05 单细胞测序与临床前验证
对引流淋巴结(84,217个细胞)和肿瘤组织(104,063个细胞)的单细胞RNA测序进一步解释了NPCM-OT重塑免疫网络的深度。在淋巴结中,研究者鉴定出一个CD63⁺ mreg DC亚群,该亚群与Treg扩增和抗肿瘤免疫受损相关。随着肿瘤进展,淋巴结内CD63⁺ mreg DC的比例及其膜胆固醇水平同步升高;而NPCM-OT虽然不改变该亚群的比例,但显著降低了其膜胆固醇水平,并在功能上逆转了其免疫抑制表型——经NPCM-OT处理的CD63⁺ mreg DC能够重新获得刺激OT-I T细胞活化和增殖的能力。在CD8⁺ T细胞一侧,伪时间轨迹分析显示NPCM-OT促进了初始T细胞向效应记忆和终末效应状态的分化,而PBS组细胞则富集于T细胞活化负调控等免疫抑制通路。CellChat分析表明,NPCM-OT增强了DC与初始CD8⁺ T细胞之间多条信号轴(VCAM1-整合素、ULBP1-KLRK1、H2-M2-CD8A、CD86-CD28)的通讯强度。
最后,研究团队在更接近临床的人源化模型中验证了转化潜力。他们利用免疫肽组学结合deepNovo和LC-MS,从胰腺肿瘤样本中预测了HLA-A33:03限制性抗原肽,装载入NPCM-T后免疫HLA-A33:03人源化小鼠。分离脾脏CD8⁺ T细胞与HLA-A33:03⁺ PANC-1胰腺癌细胞共培养,结果显示NPCM-T免疫组显著增强了肿瘤细胞杀伤,CD69⁺、Granzyme B⁺和IFN-γ⁺ CD8⁺ T细胞比例均明显升高。这为个体化新抗原疫苗的临床应用提供了概念验证。
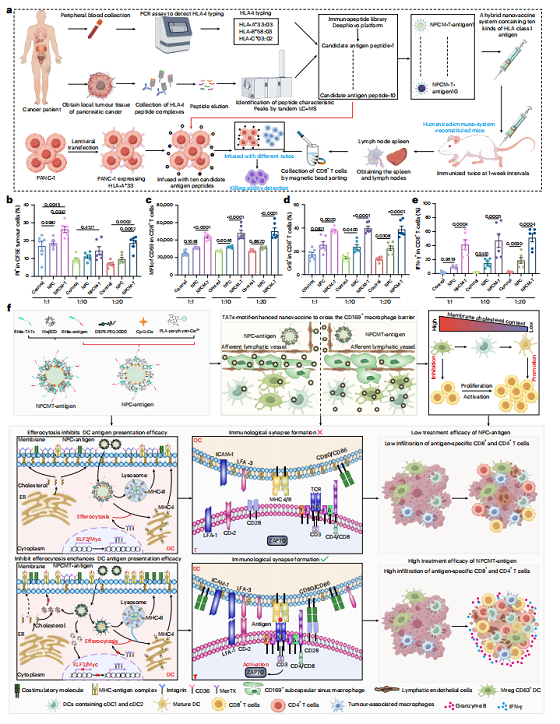
图5.Fig 5 在人源化HLA-A*33:03胰腺癌模型中对预测抗原肽纳米疫苗的验证。
总结
这项研究从临床困惑出发,经过机制探索、平台构建、多模型验证到人源化转化,形成了一个完整的证据链。其核心创新在于:不是“补充”而是“消耗”膜胆固醇来增强免疫应答;区分了胞内胆固醇(支持DC代谢活化)与膜胆固醇(调节免疫突触)的不同功能;并将抗原递送、胆固醇调控和淋巴结靶向集成于一个生物可降解的纳米平台。
当然,正如作者在结论中坦承的,该策略仍面临细胞特异性尚不完美、胆固醇消耗的安全窗口需要优化、以及规模化生产与临床转化等挑战。但无论如何,“膜胆固醇调制”已从一个代谢概念变成了一个可操作的疫苗设计原则。我们有理由期待,未来的癌症疫苗将不再是简单地“递送抗原”,而是可以同时调控多个免疫节点的物理状态与功能。
最后研究团队借助瑞沃德MOIS HT小动物活体光学成像系统,首次实现了对纳米疫苗淋巴结靶向行为的动态、定量、纵向活体追踪。实时成像数据清晰揭示:NPCM-OT在引流淋巴结中高效蓄积,峰值信号持续24-48小时——这一不可替代的影像学证据,直接锁定了“淋巴结靶向是疗效核心”的结论,也为纳米疫苗的精准设计点亮了方向。
文章链接|Article Link
Deng, Z., Lu, L., Xu, T. et al. Enhancing antitumour nanovaccine efficacy via integrated cholesterol modulation in situ. Nat. Nanotechnol. (2026). https://doi.org/10.1038/s41565-026-02153-w


