微波辅助快速原位制备超高亮度近红外探针,实现低剂量体内炎症成像
2026-05-12 来源:恒光智影 点击次数:125本文要点:位于近红外第二窗口(NIR‑II,1000–1700 nm)的荧光探针具有高组织透过率、最小的组织光子散射与吸收特性,已被广泛应用于疾病早期诊断。本文提出一种全新的原位策略,通过对化学合成的Ag₂S纳米颗粒(NPs)进行后处理,制备超高亮度Ag₂S纳米颗粒(Ag₂S超级纳米颗粒):仅需2分钟快速微波辐照即可生长一层保护性外壳。该外壳可有效降低表面缺陷与结构缺陷,使量子产率提升25倍,荧光寿命提升38倍。经聚乙二醇(PEG)修饰的Ag₂S超级纳米颗粒无毒性,可在低激发激光(1 mW/cm²)与低给药剂量(0.5 mg/kg)下实现体内深层组织成像。进一步偶联靶向肽后,在胃炎与心肌炎模型的靶向炎症成像中,Ag₂S超级纳米颗粒的成像性能显著优于商用Ag₂S纳米颗粒,荧光强度提升90%以上。本研究提供一种高效、低成本、快速的增强方法,可制备超高亮度NIR‑II成像造影剂,推动其在临床前诊断成像中的应用。
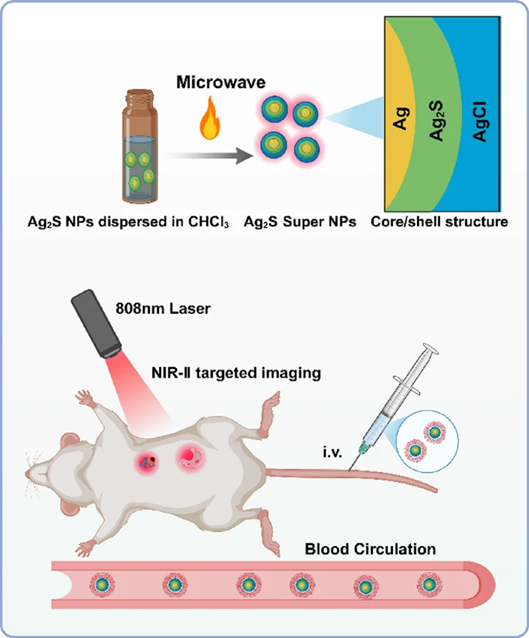
荧光成像无创灵敏,是疾病早期诊断的重要手段,但体内应用受组织信号衰减限制。近红外生物窗口(700–1800 nm)可提升光穿透深度,其中NIR‑II(1000–1700 nm)最具应用价值,相关荧光纳米颗粒能实现高信噪比深层成像。Ag₂S纳米颗粒为典型NIR‑II材料,发射谱宽、无毒性重金属、Ag⁺释放极少,且800 nm激发可降低背景自发荧光,适合体内使用。然而其亮度不足,量子产率与荧光寿命偏低,主要受等离子耦合、表面结构缺陷及溶剂相互作用影响。现有改性方法中,飞秒激光处理效果显著但设备昂贵、耗时久,超声处理可小幅提升量子产率,却无法解决溶剂猝灭问题,仍需更简便高效的亮度增强技术。
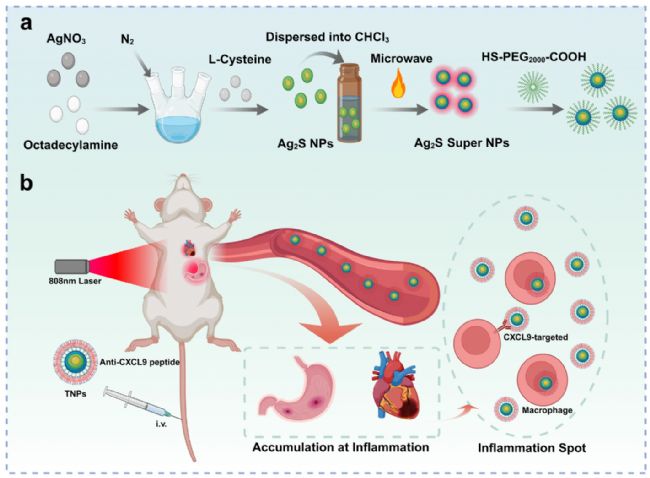
图1. Ag2S super NPs的合成工艺示意图(a)及其靶向修饰后对胃炎和心肌炎的体内高亮度、低剂量炎症成像的应用能力(b)。
本研究提出一种简单高效的Ag₂S纳米颗粒化学合成后处理方法,可使量子产率提升25倍(图1)。该方法仅需将分散在三氯甲烷(CHCl₃)中的Ag₂S纳米颗粒用微波炉进行2分钟超快非电离辐照,诱导形成AgCl保护性外壳,显著降低溶剂猝灭效应与表面/结构缺陷带来的非辐射跃迁。经靶向肽修饰后的超高亮度Ag₂S纳米颗粒,可在超低激发光强(30 mW/cm²)与超低注射剂量(~0.5 mg/kg)下实现胃炎、心肌炎的高质量体内成像,荧光强度较商用探针提升2倍。本工作为制备超高亮度NIR‑II发射造影剂提供快速、低成本、操作简便的策略,推动其在临床前诊断成像中的应用。
微波是一种非电离电磁能,频率范围300–300000 MHz,可凭借高能量加速化学反应。本研究采用功率可调微波炉提供微波能量,将化学合成的Ag/Ag₂S异质二聚体(以下简称Ag₂S纳米颗粒)分散于CHCl₃中,经微波辐照制备Ag₂S超级纳米颗粒。本化学合成方法会产生副产物Ag纳米颗粒,这是由于合成温度下Ag⁺氧化还原电位较高所致。
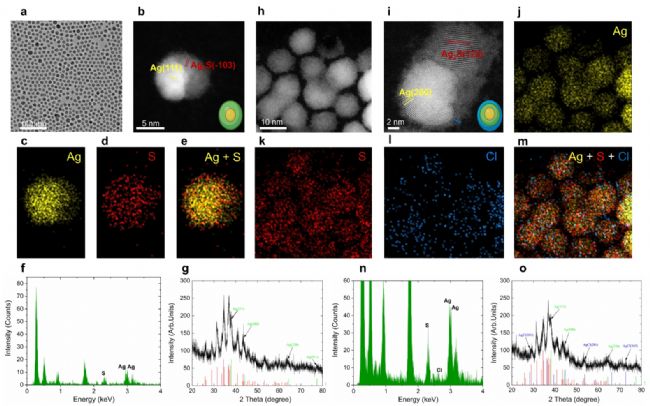
图2. 微波辐照前后Ag2S纳米粒子的形貌和元素分析。
在CHCl₃中的Ag纳米颗粒经微波辐照会转化为AgCl。图2展示微波辐照前后Ag₂S纳米颗粒的形貌与元素分析。图2a为微波辐照前Ag₂S纳米颗粒的透射电镜(TEM)图像,纳米颗粒呈椭圆形,平均尺寸约10 nm,单个颗粒内存在两种明显衬度,表明单一颗粒内形成两种不同物相。图2b高分辨扫描透射电镜(HRSTEM)与元素分析(图2c–e)显示,单个Ag₂S纳米颗粒呈类蛋黄‑壳晶体结构,核心电子致密,外壳电子透明。核心晶面间距d(111)=2.34 Å,对应立方相Ag;外壳晶面间距d(̅103)=2.38 Å,对应单斜相Ag₂S。衬度差异源于Ag₂S密度(7.2 g/cm³)低于Ag(10.50 g/cm³)。元素mapping(图2c–e)显示核心富Ag,S主要分布于外壳;EDX能谱(图2f)显示Ag:S原子比为64:36;XRD图谱(图2g)证实存在立方相Ag与单斜相Ag₂S。综上,合成的Ag₂S纳米颗粒内部含Ag核心。
经210 W微波辐照2分钟后,纳米颗粒平均直径由10 nm增至12 nm(图2h)。图2i高分辨STEM显示两种晶面:核心晶面间距d(200)=2.04 Å(立方相Ag),外壳晶面间距d(122)=2.09 Å(单斜相Ag₂S)。颗粒周围出现约1 nm厚无定形层(蓝色标注)。元素mapping(图2j–l)显示辐照后颗粒仍含Ag、S,且全部分布Cl元素(图2m),源于AgCl层形成。EDX分析(图2n)与XRD图谱(图2o)进一步证实AgCl存在,微波处理后Ag:S:Cl原子比为63:31:6。结果表明,Ag₂S纳米颗粒由立方相Ag与单斜相Ag₂S组成,经微波辐照后结构与组成改变,表面形成全新的无定形AgCl薄外壳。
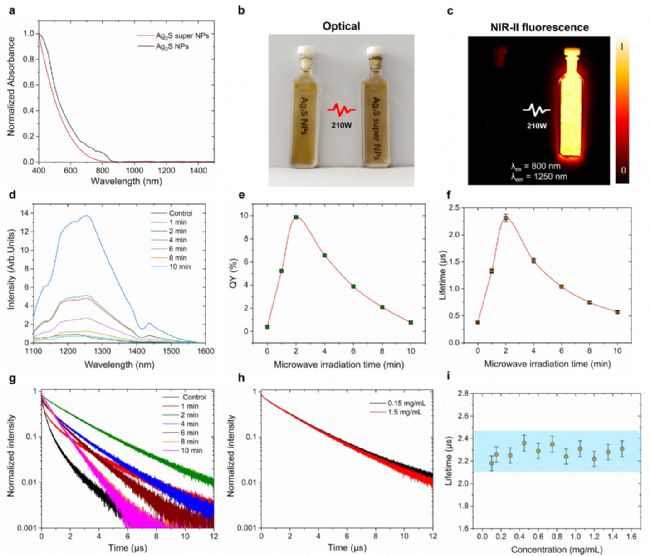
图3. 微波辐照前后Ag₂S纳米粒子的荧光性质表征。
微波辐照引发的结构变化显著提升光学性能。如图3a,微波处理后样品在400–800 nm处吸光度降至30%,且与210 W下辐照时间密切相关。处理前Ag₂S纳米颗粒在400 nm附近有特征肩峰,源于小尺寸Ag₂S纳米颗粒的等离子体带,微波处理后该峰消失。
图3b为1.5 mg/mL CHCl₃分散液中微波辐照(210 W,2分钟)前后Ag₂S纳米颗粒的光学照片,颜色无明显变化;但NIR‑II荧光图像(图3c)显示,微波辐照后亮度显著提升。未处理的化学合成Ag₂S纳米颗粒几乎检测不到NIR‑II荧光信号。
图3d为210 W下不同辐照时间(1、2、4、6、8、10分钟)的Ag₂S纳米颗粒荧光光谱。辐照后发射强度较未处理组提升,2分钟时达到最大增强,随时间延长逐渐下降;光谱形状保持一致,表明微波处理未改变化学组成,但发射峰位发生微小红移(由1220 nm至1255 nm),可能源于CHCl₃解离产生活性氯,在Ag₂S纳米颗粒表面形成高氯覆盖层。
荧光量子产率(QY,图3e)与荧光寿命(图3f)随微波时间的变化趋势与发射强度一致:1分钟辐照后QY开始上升,2分钟达峰值,继续延长时间则下降。经210 W、2分钟微波处理,Ag₂S纳米颗粒QY由0.38%提升至9.8%,增幅约25倍,实现向Ag₂S超级纳米颗粒的转化;相应荧光寿命由0.37 μs延长至2.31 μs(图3f),荧光衰减曲线见图3g。该寿命增强不受Ag₂S超级纳米颗粒浓度影响,排除自吸收对寿命测量的干扰(图3h–i)。
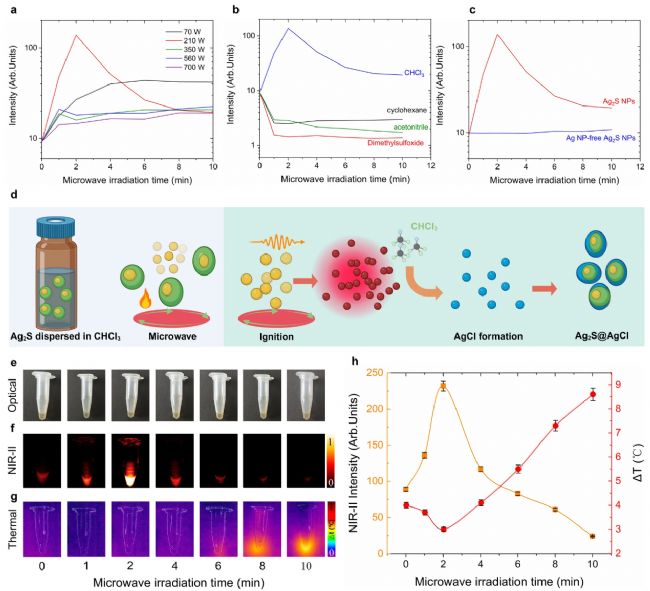
图4. 微波辐照Ag₂S纳米粒子增强机理探讨。
为探究微波诱导Ag₂S超级纳米颗粒的亮度增强机制与最优实验条件,开展系列关键实验,所有样品浓度均标准化为1.5 mg/mL。图4a为不同功率(70、210、350、560、700 W)、不同时间(0–10分钟)辐照下Ag₂S纳米颗粒的NIR‑II发射强度。70–210 W、辐照<4分钟时,发射强度随时间上升;超过阈值后趋于稳定。210 W下2分钟即可实现14倍强度增强,继续辐照则强度下降,源于长时间高功率微波导致Ag₂S降解与热猝灭。功率>210 W时,1分钟辐照增强有限,延长时间则强度下降并趋于稳定,一方面源于高功率热猝灭,另一方面源于高功率下溶剂CHCl₃快速蒸发导致反应不完全。各组样品颜色无明显差异,最优荧光增强条件为210 W、2分钟。
探究溶剂影响:选用环己烷、二甲基亚砜(DMSO)、乙腈等常用有机溶剂,结果显示仅在CHCl₃中可实现微波诱导转化,其他溶剂中NIR‑II荧光下降,主因是微波热效应与Ag₂S本征热猝灭共同作用(图4b)。探究Ag核心作用:无Ag核心的Ag₂S纳米颗粒经微波辐照荧光无增强(图4c)。因此,CHCl₃存在与Ag纳米颗粒存在是微波诱导纳米颗粒向超级纳米颗粒转化的必要条件。
综合实验结果,提出纳米颗粒向超级纳米颗粒转化机制(图4d):微波辐照下,Ag纳米颗粒吸收高能量发生降解,溶液中活性Ag⁺浓度快速上升;被Ag₂S包裹的Ag核心不受微波影响。Ag⁺与溶剂CHCl₃反应生成AgCl,在微波辅助下沉积于Ag₂S纳米颗粒表面。最终,窄带隙Ag₂S(0.9 eV)被宽带隙AgCl(5.13 eV)无机外壳保护性包覆。AgCl外壳一方面减少CHCl₃溶剂猝灭导致的非辐射跃迁,另一方面抑制表面/内部缺陷引发的非辐射退激发,同时显著降低Ag₂S超级纳米颗粒的光热转换效率(图4e–h),与低亮度商用Ag₂S纳米颗粒的光热对比实验也证实这一点。
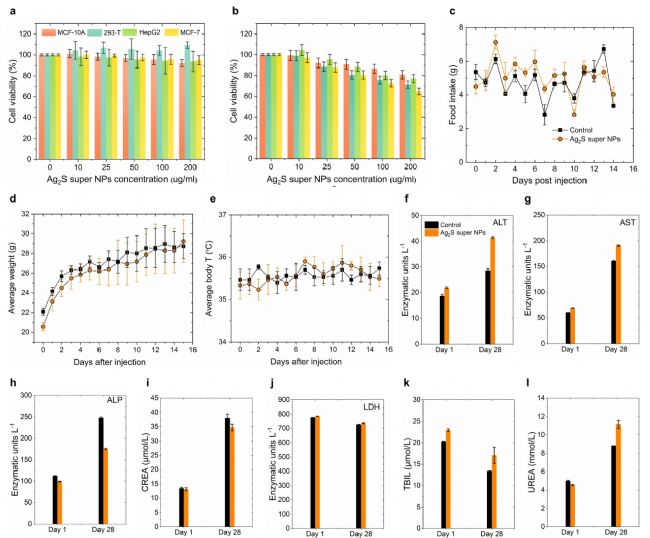
图5. PEG-Ag₂S超纳米粒的体内外细胞毒性研究。
为开展体内实验,首先对Ag₂S超级纳米颗粒进行理想的亲水表面修饰。采用配体交换法将HS‑PEG‑COOH修饰于颗粒表面,使其转移至磷酸盐缓冲液(PBS)中。细胞毒性实验:在MCF‑10A、293‑T、HepG2、MCF7细胞系中,分别用10、25、50、100、200 μg/mL的PEG‑Ag₂S超级纳米颗粒孵育24小时(图5a)和48 h(图5b)。MTT结果显示,200 μg/mL高浓度下48小时内无显著细胞毒性,适合体内应用。
体内生物相容性系统评价:4周龄昆明小鼠腹腔注射PEG‑Ag₂S超级纳米颗粒PBS分散液(300 μL,0.5 mg/mL,总剂量150 μg,~6 mg/kg),连续15天监测体重、摄食量、体温;对照组注射300 μL PBS。如图5c-e所示显示两组无显著差异,实验组体重平稳增长,与对照组一致,表明注射不影响正常代谢。综上,PEG‑Ag₂S超级纳米颗粒生物相容性高、无毒性,是理想的体内成像候选材料。
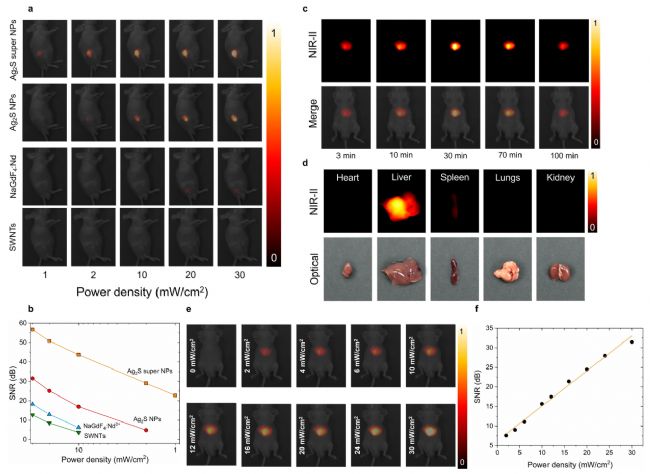
图6. PEG-Ag₂S超微粒子的体内成像性能。
体内性能直接对比实验:选用商用Ag₂S纳米颗粒、钕掺杂稀土氟化物纳米颗粒(NaGdF₄:Nd)、单壁碳纳米管(SWNTs)三种常用NIR成像探针。6周龄裸鼠分为四组,皮下注射100 μL 1.5 mg/mL各探针PBS溶液,剂量5 mg/kg。如图6a所示,在功率密度为1 mW/cm2至30 mW/cm2的808 nm激光照射下,为每组捕获活体NIR-II荧光图像。在相同的实验条件下,Ag2S超纳米粒的亮度明显高于其他近红外探针。根据之前的研究,在NIR-II成像观察期间,所有荧光探针的可见NIR发射性能差异可完全归因于亮度变化。因此,即使在1 mW/cm2的极低激光辐照功率密度下,Ag2S超级NPs的优异亮度也能够获得NIR信号,其中没有从任何其他选定的NIR探针检测到荧光信号。图6b量化了不同NIR探针的信噪比(SNR)值,显示了功率密度依赖性,这在静脉注射30 min后在不同功率密度下获得的NIR-II图像中进一步说明(图6e-f)。此外,图6a表明,合成的Ag2S超级NPs将最小励磁功率密度降低了30倍以上。
静脉注射(100 μL,0.15 mg/mL,总剂量15 μg~0.5 mg/kg)监测体内生物分布,该剂量远低于已有报道的6.6 mg/kg。在808 nm、30 mW/cm²激光下采集图像,该功率远低于国际非电离辐射防护委员会安全阈值(329 mW/cm²)。注射后3分钟,部分PEG‑Ag₂S超级纳米颗粒开始在肝脏聚集,荧光信号覆盖小范围区域;30分钟后,大部分颗粒被肝脏网状内皮系统捕获;100分钟后离体器官成像(图6d)与定量结果证实这一分布。肝脏在100分钟时荧光强度较30分钟下降约10%,源于Kupffer细胞与肝窦内皮细胞的部分清除作用。
研究表明,炎症急性期最主要的细胞是表达炎症趋化因子CXC配体9(CXCL9)的巨噬细胞。为实现精准靶向炎症成像,将特异性结合CXCL9的肽配体通过脱水缩合偶联于PEG‑Ag₂S超级纳米颗粒与商用PEG‑Ag₂S纳米颗粒表面,赋予探针炎症组织靶向能力。
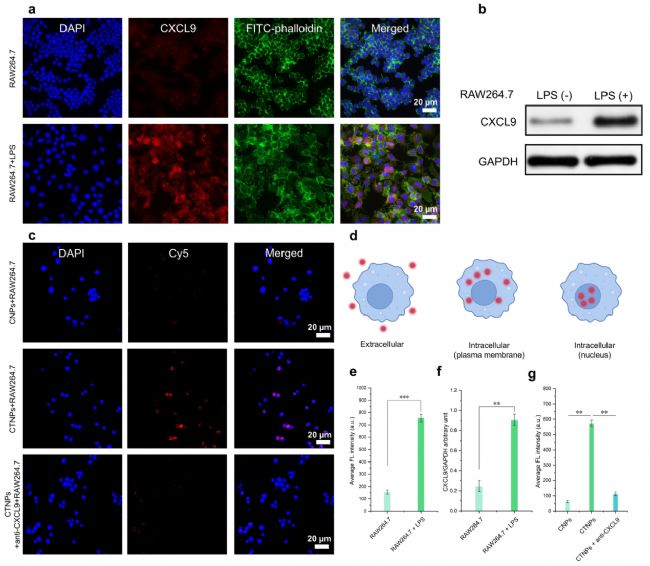
图7. LPS诱导巨噬细胞CXCL9的体外水平及Ag2S超核蛋白体外靶向结合的评价。
体外验证LPS诱导巨噬细胞中CXCL9表达:图7a免疫荧光图像显示,LPS处理的RAW 264.7小鼠巨噬细胞与抗CXCL9抗体孵育后呈现强红色荧光,细胞核蓝色、细胞骨架绿色;未处理组无明显红色荧光。统计分析显示两组CXCL9表达差异显著;蛋白质印迹(WB)结果一致(图7b和f)。图7d显示了细胞摄取的示意图。因共聚焦激光扫描显微镜(CLSM)无法检测NIR‑II信号,采用Cy5标记的靶向探针(Cy5‑T‑Ag₂S超级纳米颗粒,CTNPs)与非靶向探针(Cy5‑PEG‑Ag₂S超级纳米颗粒,CNPs)。将CNPs和CTNPs与LPS诱导的巨噬细胞共孵育,观察CNPs和CTNPs的细胞内化行为。CTNPs组的CLSM图像显示明显的红色荧光。然而,在CNPs组中,仅观察到极小的细胞内红色荧光(图7c)。此外,当LPS诱导的巨噬细胞用CXCL9抗体预处理时,细胞内的红色荧光强度显著减弱(图7g)。这些发现强调了CXCL9靶向在促进纳米探针与炎症细胞有效结合中的关键作用。因此,这表明T-Ag₂S超级NPs比PEG-Ag₂S超级NPs更容易被巨噬细胞吞噬,这可能是由于CXCL9介导的相互作用增强所致。这些结果为炎性靶向T-Ag₂S超纳米粒在体内炎症显像中的应用提供了坚实的实验基础。
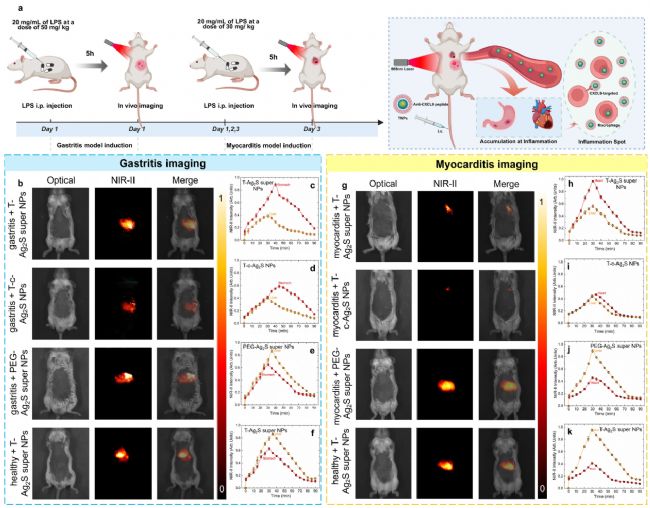
图8. 小鼠体内胃炎模型构建和成像。
胃炎模型构建:腹腔注射20 mg/mL LPS溶液(总剂量50 mg/kg),连续监测生理状态5小时,模型构建成功。组织病理学与血液分析证实胃黏膜结构损伤、炎症细胞浸润,炎症标志物(TNF‑α、IL‑6、PGE₂、CRP、MDA)显著升高。小鼠随机分为四组:(1)胃炎+T‑Ag₂S超级纳米颗粒;(2)胃炎+T‑商用Ag₂S纳米颗粒;(3)胃炎+PEG‑Ag₂S超级纳米颗粒;(4)健康+T‑Ag₂S超级纳米颗粒。静脉注射100 μL 0.15 mg/mL探针,连续90分钟采集NIR‑II图像(图8a)。图8b中包括的NIR-II图像在静脉注射后35 min获得,成像结果显示靶向修饰的Ag₂S NPs在胃中受胃炎影响的组织处优先聚集。值得注意的是,与注射T-c-Ag₂S NPs组(图8d)相比,注射T-Ag₂S super NPs组(图8c)的时间演化荧光强度明显高于胃炎炎症部位(图8d)。当使用非靶向PEG-Ag₂S超级NPs或在没有胃炎炎症的情况下,NIR-II图像显示,由于纳米颗粒在肝脏中的保留,注射的NPs优先累积以存活(图8b)。相应的时间演化NIR发射荧光强度(图8e-f)证实了该现象。NIR-II荧光图像显示T-Ag₂S超纳米粒和T-c-Ag₂S纳米粒对胃炎具有成功的体内靶向性。更重要的是,该结果进一步突出了Ag₂S超级纳米颗粒的优越体内成像性能,其特征是在低剂量注射条件下比市售Ag₂S纳米颗粒具有更高的亮度。
基于上述胃炎炎症成像结果,随后开展了体内心肌炎成像。以20 mg/mL浓度的LPS溶液(每只小鼠总剂量30 mg/kg)腹腔注射至小鼠体内,随后连续监测生理状态3天,直至心肌炎模型成功建立。为了实现明亮和靶向成像,将4周龄雌性小鼠随机分为四组:(1)心肌炎 + T-Ag₂S super NPs;(2)心肌炎 + T-commercial Ag₂S NPs(T-c-Ag₂S NPs);(3)心肌炎 + PEG-Ag₂S super NPs;(4)健康 + T-Ag₂S super NPs。每组小鼠静脉注射分散在PBS中的相应NPs(100 µL,0.15 mg/mL),并持续进行NIR-II成像,每5分钟一次,总时长90分钟。图8g中心肌炎成像所包含的NIR-II荧光图像是在静脉注射后30分钟获取的。正如预期,经靶向肽修饰的NPs,即T-Ag₂S super NPs和T-c-Ag₂S NPs,在发炎的心脏组织中表现出优先积累。一方面,通过心脏荧光强度随时间变化的观察(图8h-i),可以明显看出T-Ag₂S super NPs的亮度比T-c-Ag₂S NPs提高了90%以上。另一方面,未经靶向肽修饰的NPs则主要优先积累于肝脏(图8j-k)。以上所有结果进一步揭示了所合成的PEG-Ag₂S super NPs在低剂量、高亮度、高质量体内炎症成像中的卓越能力。
数十年来,Ag₂S纳米颗粒因优异光学性能被视为极具前景的NIR‑II光学探针,但其临床前应用受限于亮度偏低。本研究提出快速、低成本、高效的微波辐照策略,使Ag₂S纳米颗粒量子产率提升25倍,最优条件为210 W、2分钟。该增强需严格满足:Ag纳米颗粒与CHCl₃同时存在。增强机制为:微波使Ag纳米颗粒降解产生高活性Ag⁺,与CHCl₃反应生成AgCl并原位沉积于Ag₂S表面,大幅抑制非辐射过程,显著提升亮度与荧光寿命。
PEG修饰后的PEG‑Ag₂S超级纳米颗粒可实现低激发剂量、低给药剂量体内成像;MTT实验、28天生化与组织学分析证实其低毒性。偶联靶向肽后,在体内外炎症靶向成像中性能突出,荧光强度较商用Ag₂S纳米颗粒提升90%以上,为未来临床早期病灶检测奠定基础。本研究提供快速、低成本、均相原位策略制备超高亮度Ag₂S纳米颗粒,为开发更高亮度光学探针的合成方法提供新思路。研究结果为发光增强型Ag₂S纳米颗粒在转移瘤、神经炎症等复杂疾病模型中严格验证临床前成像效果、推动诊疗转化应用提供坚实基础。
参考文献
Ruan D, Hu C, Yang Z, et al. Rapid in situ microwave-assisted fabrication of ultrabright near-infrared probe for low-dose in vivo inflammatory imaging[J]. Journal of Nanobiotechnology, 2025, 23(1): 606.
⭐️ ⭐️ ⭐️
动物活体荧光成像系统 - MARS
In Vivo Imaging System
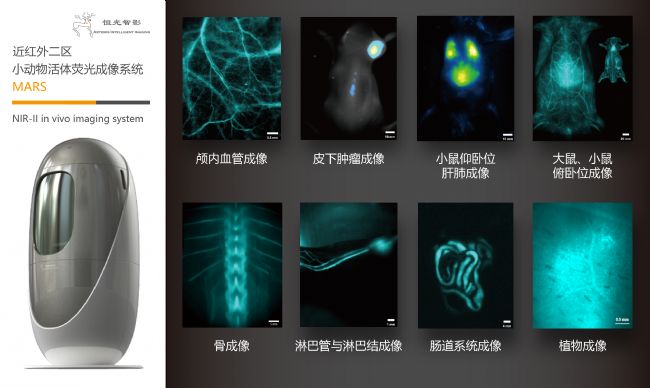
高分辨率 - 定制高分辨大光圈红外镜头,空间分辨率优于3um
荧光寿命 - 分辨率优于 5us
高速采集 - 速度优于1000fps (帧每秒)
多模态系统 - 可扩展X射线辐照、荧光寿命、光声和光热成像、原位成像光谱,CT等
显微镜 - 高分辨显微成像系统,兼容成像型光谱仪
⭐️ ⭐️ ⭐️
恒光智影
上海恒光智影医疗科技有限公司,被评为“国家高新技术企业”、“上海市专精特新中小企业”,获国家科技部“重大科学仪器研发专项”支持,荣获上海市“科技创新行动计划”科学仪器项目、上海市2025年度关键技术研发计划“计算生物学”项目。
恒光智影,致力于为生物医学、临床前和临床应用等相关领域的研究提供先进的、一体化的成像解决方案。
专注动物活体成像技术,成像范围覆盖 400-1700 nm,同时可整合CT, X-ray,超声,光声,光热成像等技术。
可为肿瘤药理、神经药理、心血管药理、大分子药代动力学等一系列学科的科研人员提供清晰的成像效果,为用户提供前沿的生物医药与科学仪器服务。

