NETs (中性粒细胞胞外诱捕网)助力理解心脑血管疾病的病理机制
2026-05-09 来源:本站 点击次数:28为什么有些心梗患者,大血管明明已经开通,心肌却依然在持续坏死——微循环里究竟藏着什么"隐形杀手"?
为什么部分缺血性卒中患者,在接受tPA溶栓后不仅难以有效再通,反而面临更高的出血转化风险?
为什么系统性红斑狼疮患者,在没有传统危险因素的情况下,心血管事件的发生率却远高于普通人群?
答案可能并不全在传统的血脂或经典血小板通路上,而是藏在血管微环境中的一张“隐形陷阱网”——中性粒细胞胞外诱捕网(Neutrophil Extracellular Traps, NETs)。
《Pharmacology & Therapeutics》《Eur Heart J》等期刊的最新高水平研究持续提示,NETs 在炎症-血栓轴中发挥着关键作用,越来越被认为是连接炎症、血栓形成与器官损伤的重要枢纽。随着血管生物学与免疫学的深度融合,NETs 正为我们理解心脑血管疾病的病理机制提供全新的视角。
核心概念:什么是 NETs?
简单来说,NETs 是中性粒细胞在受到外界刺激时,向外抛出的一张以自身染色质 DNA 为骨架、镶嵌着多种高活性蛋白的网状结构。
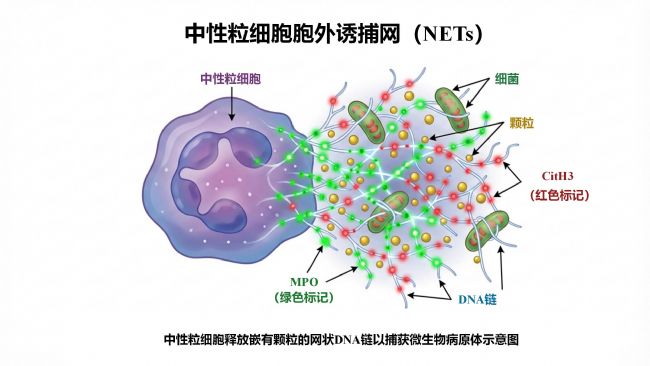
本文带您快速透视,这张“网”是如何在心脑血管疾病中推波助澜的。
机制揭秘:不仅是物理路障,更是生化火药桶
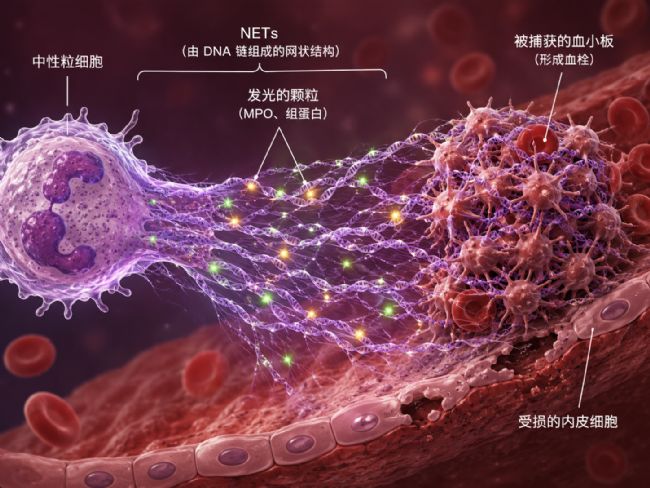
作为一张交织的“实体网”,NETs 最直观的危害是在血管内拦截红细胞与血小板,形成物理层面的机械堵塞。然而,其致病作用远不止于此,这实际上是一场由游离 DNA 骨架、组蛋白和颗粒蛋白共同参与的物理与生化“双重打击”:
1. 强效的血栓支架
NETs 带有负电荷的网状结构不仅在物理上捕获血小板,还能作为接触激活平台,促进凝血因子 XII(Factor XII, FXII)的激活。这种“DNA-纤维蛋白”交织结构,使血栓对内源性纤溶系统产生更强抵抗力。
2. 促炎级联的放大器
镶嵌在 NETs 上的各类酶,如髓过氧化物酶(Myeloperoxidase, MPO)和中性粒细胞弹性蛋白酶(Neutrophil Elastase, NE),可激活血管内皮及免疫细胞上的 Toll 样受体(TLR-4/9),从而放大局部炎症反应,形成持续激活的炎症微环境。
3. 细胞毒性与内皮损伤
NETs 携带的阳离子组蛋白(Cationic Histones)可直接破坏内皮细胞膜完整性,并诱导炎症性细胞死亡(如细胞焦亡等程序性细胞死亡形式)。这一过程被认为是促进斑块不稳定及破裂的重要触发因素。
心脑血管“病理推手”:从心脏到大脑的全域影响
NETs 在心、脑及外周血管中均扮演着“恶化微环境”的关键角色:
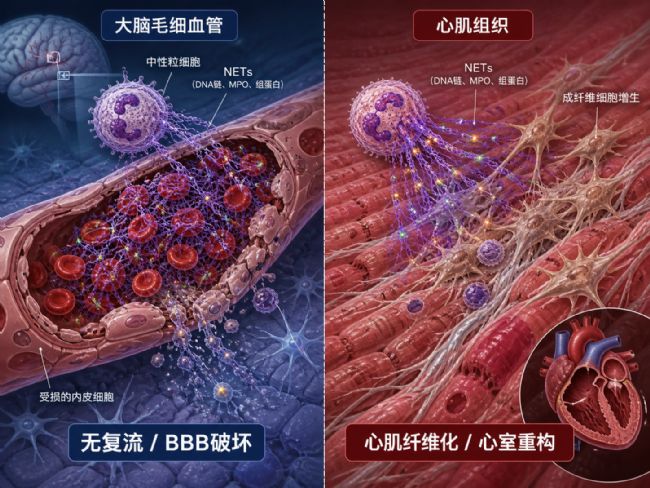
心脏领域:心衰与房颤的推手
-
心梗后重构:急性心梗后,大量涌入缺血区的 NETs 会显著降解细胞外基质,促使成纤维细胞过度分泌胶原。它是推动梗死后心室重构、进展为心力衰竭的关键推手之一。
-
房颤新底物:NETs 的局部沉积还被认为可参与心房电学重构,增加左心耳血栓风险,成为房颤的新型病理底物。
脑血管领域:无复流与出血转化
-
血脑屏障损伤:在缺血性卒中里,NETs 可通过多种机制破坏血脑屏障(Blood-Brain Barrier, BBB)完整性,包括损伤紧密连接蛋白。
-
溶栓抗性与出血:在 NETs 释放水平较高的病理背景下,使用组织型纤溶酶原激活剂(tPA)溶栓可能会增加微血管脆弱性,进而诱发出血转化。
-
无复流现象:微循环中充斥的 NETs“微血栓”会阻塞毛细血管,成为血管再通后无复流(No-reflow)现象的关键促发因素之一。
外周与代谢:DVT 与糖尿病
-
静脉血栓:在静脉低流速区,NETs 被认为是深静脉血栓(Deep Vein Thrombosis, DVT)形成的重要促发因素之一。
-
伤口难愈合:糖尿病的高血糖环境会让中性粒细胞处于“高敏状态”,极易释放 NETs。它们在足部创面形成致密的“病理屏障”,严重阻碍伤口愈合。
临床转化:NETs 检测的增量价值与未来边界
既然 NETs 在病理进程中如此关键,将其作为生物标志物在临床应用上究竟有何增量价值?相较于常规临床指标,其独特的机制属性带来了不可替代的补充价值:
1. 机制互补:NETs 带来的多维病理画像
临床上已有各种成熟的检测指标,关注 NETs 的意义并非替代现有检测,而是提供不可或缺的"微环境画像”:
对比心脑损伤“金标准”(如 cTn 肌钙蛋白 / NSE):
肌钙蛋白与神经元特异性烯醇化酶(NSE)是细胞已发生不可逆坏死破裂后的“结果宣告”;而 NETs 及其衍生标志物(如 MPO-DNA)主要反映微循环内急性免疫介导的局部破坏。高水平 NETs 可作为金标准的机制性补充,有助于提示微血栓活跃状态及斑块不稳定风险。
对比传统代谢危险因素(如 LDL-C):
低密度脂蛋白胆固醇(LDL-C)反映的是长期的“代谢底物”风险暴露(犹如燃料);而 NETs 释放引发的急剧炎症风暴更像是急性事件的“点火机制”。这为心血管领域常讲的“血脂已达标但仍突发血栓事件的残余风险(Residual Risk)”提供了免疫学层面的合理解释。
对比泛炎症与凝血指标(如 hs-CRP / D-Dimer):
超敏 C 反应蛋白(hs-CRP)提示系统性的非特异性炎症,而 NETs 标志物指向更具破坏性的血管壁特异性微环境;D-二聚体(D-Dimer)是血栓形成及纤溶亢进的产物,而评估 NETs 的释放水平则有助于预警该血栓对后续溶栓药物的潜在抵抗性。
2. 前沿临床应用的全景拓展
基于这一独特机制,NETs 的检测与干预正向多个前沿临床场景延伸:
评估“残余血栓风险”:
大量研究证实,NETs 可通过多种机制强效激活血小板——包括颗粒蛋白(如 cathepsin G)的直接作用、组蛋白经 TLR 通路的间接激活,以及 DNA 骨架对凝血因子的接触激活——为临床常见的残余血栓风险(Residual Thrombotic Risk)提供了抗血板治疗难以完全覆盖的免疫学解释。同时,NETs 释放水平较高时,往往预示着更强的 tPA 溶栓抵抗。快速评估 NETs,可为优化抗栓方案提供分子层面的辅助参考。
自身免疫病的心血管风险监控:
在系统性红斑狼疮(SLE)等自身免疫病患者中,过度活跃的 NETs 是导致其频发早发性心血管事件的关键免疫连接环节。在这一亚群中,NETs 检测的监控价值尤为突出。
靶向药伴随诊断的“试金石”:
目前,针对肽酰基精氨酸脱亚氨酶 4(PAD4)抑制剂等阻断 NETs 形成的创新药物正逐步推进临床试验。高灵敏度的 NETs 检测是评估靶点结合率、衡量药效学特征的核心工具。
从实验室到临床:检测破局与转化路径
心脑血管疾病的治疗,正在从单纯的"通血管"稳步迈向"靶向干预免疫微环境"的新方向。而这一转变能否真正落地,核心瓶颈之一在于:如何在临床场景中稳定、特异地量化 NETs 的释放水平?
如前所述,NETs 在心梗微循环障碍、卒中溶栓抵抗、自身免疫病心血管损伤等场景中均扮演关键角色。然而,现有检测手段能否真实反映这张"网"在血管微环境中的活跃程度,始终是横亘在科研与临床之间的方法学难题。血液游离 MPO-DNA 作为最常用的替代标志物,极易与循环 cfDNA(游离 DNA)产生混淆——在心梗、卒中等本身即伴随大量组织损伤的高炎症背景下,这一特异性不足的问题尤为突出。
回到细胞源头,是当下最具方法学说服力的答案。
与其依赖缺乏细胞学身份的游离碎片,不如直接在细胞层面锁定活化状态——这正是奎克泰 NETs 流式检测试剂盒的核心设计逻辑。通过"细胞身份+效应产物"的双重锚定,有效规避了传统 ELISA 假阳性与特异性不足的固有缺陷:
-
CD45 / CD66c:精准圈门活化态中性粒细胞。CD66c 表达上调可作为 NETosis 启动的预警参考,从细胞源头确保检测特异性
-
MPO / DNA:在锚定特定细胞群的基础上,提供 NETs 核心酶与染色质骨架的直接功能学证据
-
50μL 微量血,40 分钟出结果:适配围手术期、ICU 急救及动物模型等高时效性场景的动态连续监测需求。

参考文献:
Krishnamoorthy NK, et al. NETosis in ischemic stroke: Mechanisms, implications, and therapeutic prospects. Pharmacol Ther. 2026;281:108999.
Shetty S, Subramanian M. Neutrophil Extracellular Traps (NETs) as drivers of atherosclerosis: Pathogenic mechanisms and therapeutic opportunities. Pharmacol Ther. 2025;274:108917.
Shahzad A, et al. Neutrophil Extracellular Traps (NETs) in health and disease. Mol Biomed. 2025;6(1):130.
Döring Y, Soehnlein O, Weber C. Neutrophil Extracellular Traps in Atherosclerosis and Atherothrombosis. Circ Res. 2017;120(4):736-743.
Stakos DA, Kambas K, Konstantinidis T, et al. Expression of functional tissue factor by neutrophil extracellular traps in culprit artery of acute myocardial infarction. Eur Heart J. 2015;36(22):1405-1414.
Mangold A, Aliahmad H, Metzler B, et al. Coronary neutrophil extracellular trap burden and deoxyribonuclease activity in ST-elevation acute myocardial infarction are predictors of ST-segment resolution and infarct size. Circ Res. 2015;116(7):1182-1192.
Borissoff JI, Joosen IA, Versteylen MO, et al. Elevated levels of circulating DNA and chromatin are independently associated with severe coronary atherosclerosis and a prothrombotic state. Arterioscler Thromb Vasc Biol. 2013;33(8):2032-2040.
Kaplan MJ, Radic M. Neutrophil extracellular traps: double-edged swords of innate immunity. J Immunol. 2012;189(6):2689-2695.
Fuchs TA, Brill A, Duerschmied D, et al. Extracellular DNA traps promote thrombosis. Proc Natl Acad Sci U S A. 2010;107(36):15880-15885.

