单细胞测序解码肝癌免疫微环境:MAIT细胞可塑性及促癌机制的新见解
2026-05-15 来源:本站 点击次数:72
影响因子:19.8
通讯单位作者:中国科学技术大学白丽等
伯豪技术服务:单细胞转录组测序
导语
肝细胞癌(HCC)是全球癌症相关死亡的第三大原因,其免疫微环境的复杂性是导致免疫治疗疗效异质性的关键因素。黏膜相关恒定T细胞(MAITs)在人类肝脏中高度富集,但其在HCC中的作用存在“抗肿瘤”与“促肿瘤”的长期争议。这种争议很大程度上源于MAIT细胞的功能异质性和可塑性——传统的群体水平分析难以区分不同MAIT亚群的独特贡献。
近日,中国科学技术大学白丽、张慧敏、王华、刘连新、傅思成及安徽医科大学第一附属医院钱叶本为共同通讯在Cellular & Molecular Immunology 在线发表题为“MAIT cell plasticity generates CD4+ MAIT cells that promote HCC progression via metabolic crosstalk with tumor cells”的研究论文。利用单细胞RNA测序(scRNA-seq) 技术,结合流式细胞术、体外功能实验和动物模型,系统揭示了MAIT细胞可塑性产生的CD4⁺ Th17极化亚群通过代谢串扰促进HCC进展的新机制。本文将从单细胞转录组学的视角,深度解析该研究中RNA-seq分析如何破解MAIT细胞异质性难题,并为肿瘤免疫代谢提供全新见解。
技术服务
单细胞转录组测序
(技术服务由伯豪生物提供)
主要研究
1. 单细胞测序精准解析肝癌中MAIT细胞的亚群异质性
研究团队首先对7例未经治疗的HCC患者的肿瘤组织及配对癌旁组织中分选的T细胞进行了单细胞RNA测序(10x Genomics平台)。经过严格的质量控制和聚类分析,他们鉴定出多个T细胞亚群,其中MAIT细胞(定义为CD3E⁺ SLC4A10⁺ ZBTB16⁺ RORC⁺)主要聚集在cluster 6和cluster 14 (Supplementary Fig. 3a, b)。
为了进一步解析MAIT细胞的内部异质性,研究者对MAIT细胞进行了基于差异表达基因的再聚类。结果令人振奋:MAIT细胞被明确分为三个转录组特征迥异的亚群:CD4⁺ MAIT簇、CD8⁺ MAIT簇和双阴性(DN)MAIT簇 (Supplementary Fig. 3c, d)。热图显示,这些亚群具有独特的基因表达谱 (Supplementary Fig. 3e)。
2. 单细胞转录组学揭示CD4⁺ MAIT细胞的Th17极化特征
CD4⁺ MAIT亚群最显著的特征是高表达Th17相关基因。如图1F所示,与CD8⁺ MAIT和DN MAIT相比,CD4⁺ MAIT簇中IL17A、IL17F、IL1R1、IL6R、IL23R、IL21、ICOS、AHR和HIF1A的表达水平显著升高。更令人信服的是,研究团队利用另一独立发表的scRNA-seq数据集(Zheng et al., Cell 2017)进行了验证,结果显示CD4⁺ MAITs(CD3E⁺ SLC4A10⁺ CD4⁺ CD8A⁻)同样表现出更高的Th17特征基因表达 (Fig. 1G)。这种跨数据集的重复性验证充分体现了单细胞测序数据的可重复性和生物学稳健性。
此外,研究者将单细胞数据与TCGA大样本bulk RNA-seq数据相结合,发现CD4⁺ MAIT特征基因(包括CD4、SLC4A10、KLBR1、NCR3等)与Th17相关基因在HCC肿瘤样本中呈显著正相关(Pearson相关系数显示高度一致性) (Fig. 1E)。这一从单细胞到群体水平的跨尺度分析,有力证明了CD4⁺ MAIT亚群在肝癌中的Th17极化特性,而这一结论在传统流式细胞术中仅能通过少数表面标记间接推断。
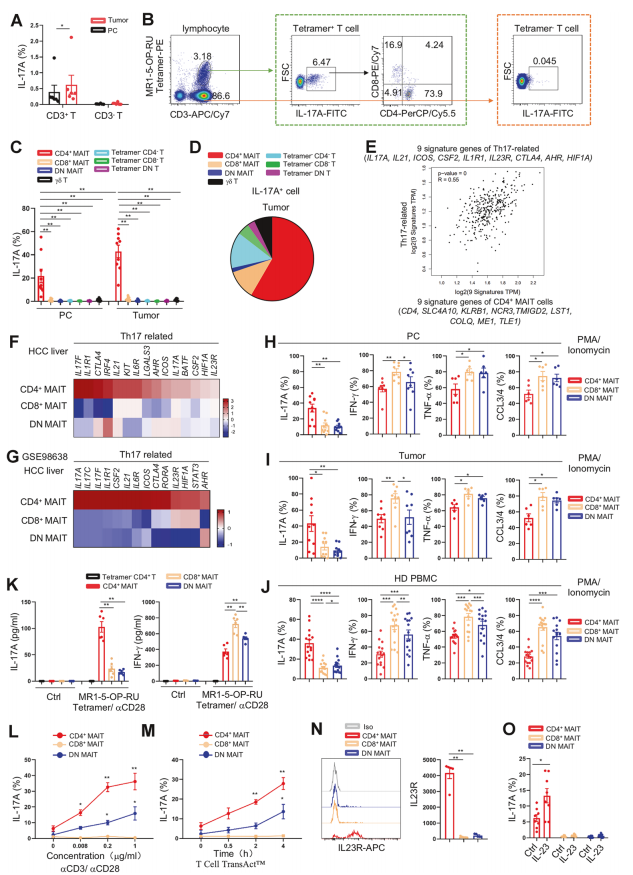
图1. CD4⁺ MAIT是人类HCC中主要的IL-17A来源
3. 单细胞TCR追踪与拟时序分析揭示MAIT细胞分化轨迹
MAIT细胞是否具有谱系可塑性?CD4⁺ MAIT从何而来?为回答这一问题,研究者利用了scRNA-seq数据中的T细胞受体(TCR)信息。通过分析已发表的单细胞数据,他们发现在同一患者的肿瘤和癌旁组织中,CD4⁺ MAITs与CD8⁺ MAITs共享完全相同的TCRβ克隆型 (Fig. 2E)。这一结果强有力地证明:CD4⁺ MAITs并非一个独立的发育谱系,而是由CD8⁺ MAITs在肿瘤微环境诱导下分化而来。
进一步的拟时序(pseudotime)轨迹分析(使用Monocle 2等算法)直观地展示了MAIT细胞的分化动态。如图2F-H所示,基于研究团队自己的scRNA-seq数据(Supplementary Fig. 3),CD4⁺ MAITs主要位于分化轨迹的末端,而CD8⁺ MAITs和DN MAITs则处于更早期或中间位置。这一计算生物学方法无需干扰细胞自然状态,即可推断细胞分化路径,是单细胞测序独有的优势。结合体外诱导实验(图2A-D),单细胞数据为“CD8⁺ MAIT → DP MAIT → CD4⁺ MAIT”的转分化模型提供了强有力的转录组学支持。
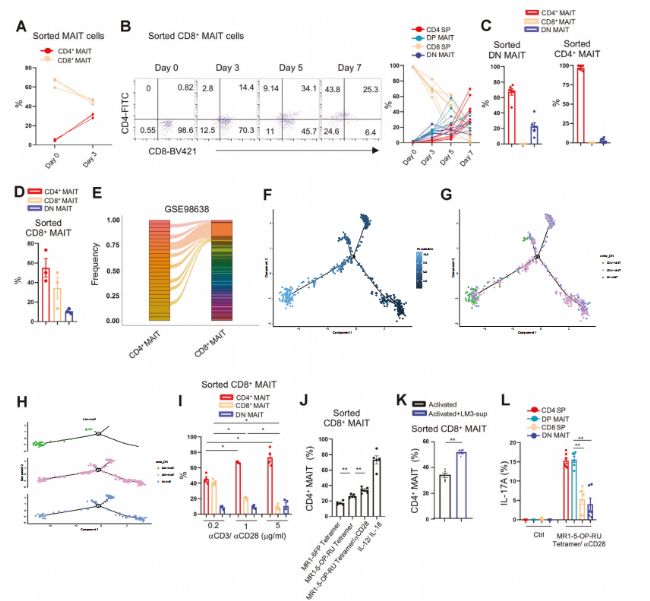
图2. CD4⁺ Th17极化MAIT由CD8⁺ MAIT分化而来
4. 整合分析:从单细胞特征到临床预后关联
单细胞测序的最终价值在于将分子特征与临床意义相连接。研究者提取了CD4⁺ Th17极化MAIT的特征基因集(包括CD4、SLC4A10、ZBTB16、AHR、PKM、IL23R、CTLA4、IL17A等),在TCGA的批量RNA-seq数据中进行相关性分析和生存分析。
结果显示,该特征基因集的表达水平与脂质储存相关基因(PPARA、ABCA12、FABP52、ELOVL4等)呈显著正相关 (Fig. 4J),与免疫抑制细胞特征基因(Treg、耗竭T细胞、MAITreg、MDSC)也呈正相关 (Fig. 4K-N)。更重要的是,高表达CD4⁺ Th17极化MAIT特征基因的HCC患者,其总生存期显著缩短(Log-rank检验,P < 0.0001) (Fig. 4O)。这一从单细胞数据挖掘到人群预后验证的分析流程,为CD4⁺ MAITs的促癌作用提供了临床层面的有力证据。
此外,研究者还利用TCGA数据发现Th17相关基因与MK167(增殖标记)及PPARA脂质储存基因的正相关关系 (Fig. 3S, T),并绘制了Kaplan-Meier曲线,证实高表达Th17基因或脂质储存基因的患者预后更差 (Fig. 3U, V)。这些分析充分展示了单细胞测序与公共数据库整合的生物信息学范式。
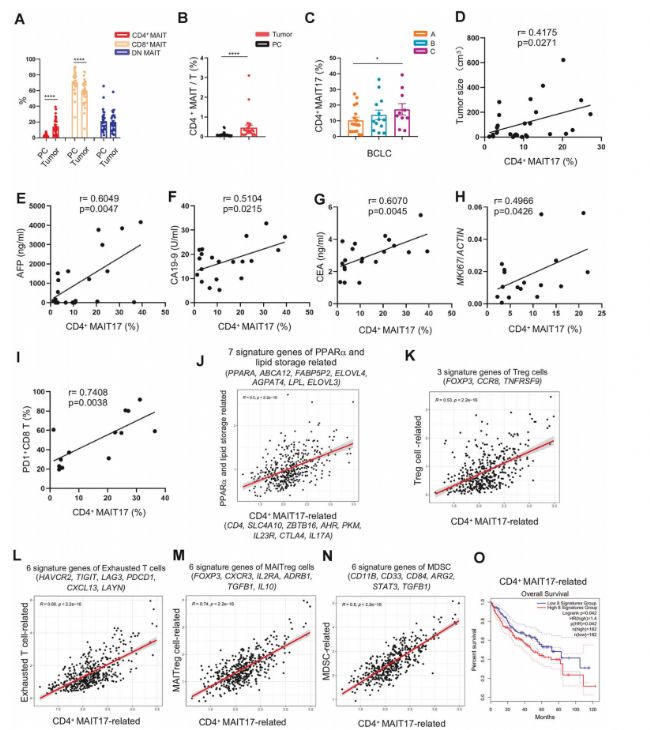
图4. CD4⁺ Th17极化MAIT与HCC肿瘤进展正相关
5. 单细胞测序揭示CD4⁺ MAIT中AHR及糖酵解基因的协同上调
研究者进一步利用单细胞转录组数据探索CD4⁺ MAITs功能极化的上游调控机制。差异表达分析显示,与CD8⁺ MAITs或DN MAITs相比,CD4⁺ MAIT簇中AHR(芳基烃受体)基因表达显著上调 (Fig. 6A, B)。同时,糖酵解相关基因集(包括SLC2A1、HK2、PFKL、PKM、ENO1、ALDOA等)在CD4⁺ MAIT中也呈现一致的高表达模式 (Fig. 6G, H)。来自Zheng实验室的单细胞数据同样验证了这一发现 (Fig. 6H)。
为了量化这些差异,研究者从健康供者外周血中分选出CD4⁺ MAITs、CD8⁺ MAITs和DN MAITs,通过qPCR验证了单细胞测序的关键发现:CD4⁺ MAITs中HK2、HK3、PFKL、PFKP、PKM1/2、ENO1、ALDOA、ALDOC及SLC2A1的mRNA水平均显著高于其他亚群 (Fig. 6I)。这种“单细胞发现 + 靶向验证”的策略,最大程度地避免了假阳性,体现了单细胞测序作为探索性工具的强大功能。
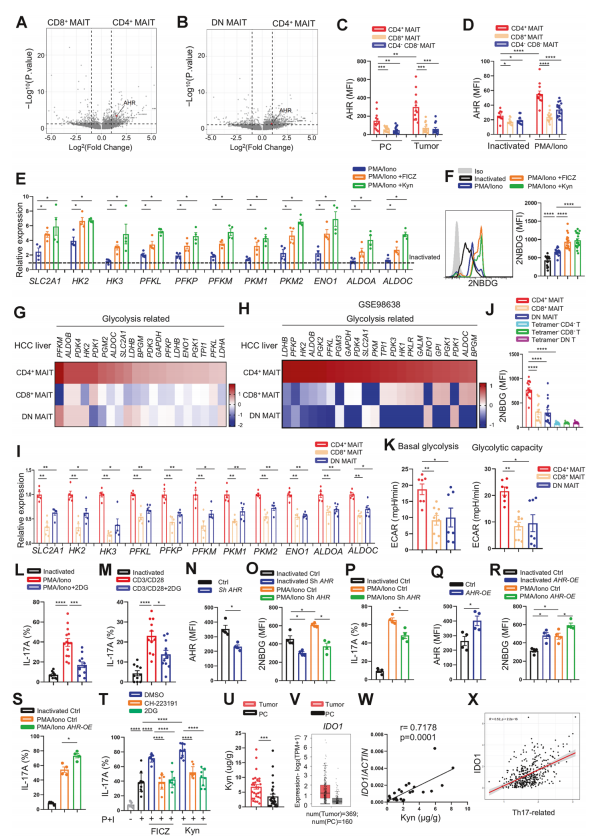 图6. 肿瘤细胞分泌的犬尿氨酸通过AHR起始CD4⁺ Th17极化MAIT的糖酵解和IL-17A分泌
图6. 肿瘤细胞分泌的犬尿氨酸通过AHR起始CD4⁺ Th17极化MAIT的糖酵解和IL-17A分泌
结语
该研究之所以能够精准定义肝癌中MAIT细胞的三个功能亚群、揭示CD4⁺ MAIT的Th17极化特征、追踪其从CD8⁺ MAIT转分化的谱系轨迹,并发现AHR与糖酵解基因的协同上调,关键在于**高质量的单细胞RNA测序数据。从独立数据集的交叉验证,到TCR克隆型共享分析,再到拟时序分化重建,单细胞转录组学贯穿了从“发现”到“验证”再到“临床关联”的完整证据链。正是单细胞分辨率下对转录组的无偏倚解析,才使研究者得以突破传统群体分析的局限,捕捉到MAIT细胞可塑性的真实面貌。对于肿瘤免疫微环境等高度异质性的研究领域,单细胞测序已成为揭示稀有亚群、推断分化路径和连接分子特征与临床预后的核心技术工具。
参考文献:
Fu, S., Tang, M., Zhao, C. et al. MAIT cell plasticity generates CD4+ MAIT cells that promote HCC progression via metabolic crosstalk with tumor cells. Cell Mol Immunol 23, 491–504 (2026). https://doi.org/10.1038/s41423-026-01409-8

