740 Y-P作为PI3K通路激动剂在细胞增殖凋亡自噬及动物模型中的应用
2025-09-12 来源:本站 点击次数:42
740 Y-P是一种具有细胞渗透性的多肽类激动剂,通过特异性激活磷脂酰肌醇3-激酶(PI3K) 信号通路,在细胞信号转导研究中发挥重要作用。大量研究表明,740 Y-P(AbMole,M9389)在多种细胞模型中可有效促进细胞增殖、抑制凋亡过程并调节代谢活动,同时在阿尔茨海默等神经退行性病变研究模型中调控氧化应激。AbMole为全球科研客户提供高纯度、高生物活性的抑制剂、细胞因子、人源单抗、天然产物、荧光染料、多肽、靶点蛋白、化合物库、抗生素等科研试剂,全球大量文献专利引用。
一、740 Y-P(740YPDGFR)的作用机制
740 Y-P(AbMole,M9389)是一种人工设计的多肽化合物,含有25个氨基酸,在第21位的酪氨酸残基被磷酸化修饰,形成关键的p-Tyr结构单元,这一修饰对其生物活性至关重要,使其能够有效模拟天然磷酸化蛋白质,进而与带有SH2结构域的蛋白相互作用。740 Y-P的其余结构也是经过特殊设计的,其N端的16个氨基酸衍生自Antennapedia蛋白的第三螺旋结构,这一区域赋予了它出色的细胞膜穿透能力;C端9个氨基酸则来源于血小板衍生生长因子受体(PDGFR)上的高亲和力p85结合位点,该位点负责特异性识别并激活PI3K的调节亚基--p85。这种巧妙的嵌合设计使740YP兼具细胞渗透性和靶向特异性,成为研究细胞内PI3K信号通路的理想分子工具[1]。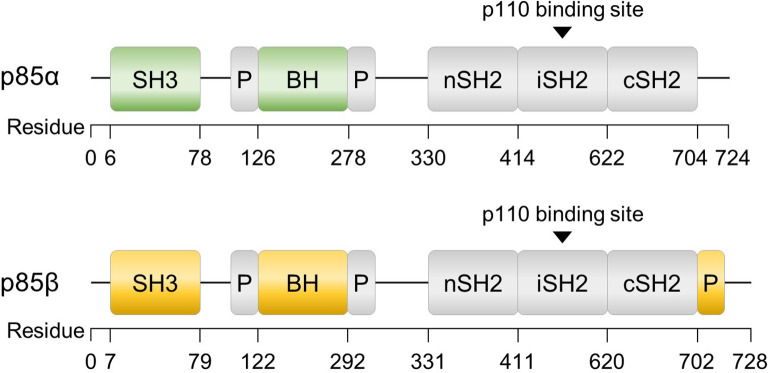

当740 Y-P(AbMole,M9389)进入细胞内部后,C端氨基酸可模拟PDGFR受体的磷酸化酪氨酸基序,与PI3K的p85调节亚基结合,同时磷酸化的Tyr21则与p85中的SH2结构域结合,这种结合将解除p85对PI3K的抑制。进而引发下游Akt的募集和激活。激活的Akt通过磷酸化多种底物蛋白,最终协调促进细胞增殖、抑制凋亡、增强代谢活动等一系列生物学效应[1]。
二、740 Y-P(740YPDGFR)的研究应用
1. 740 Y-P(740YPDGFR)用于细胞增殖与周期调控研究
740 Y-P(AbMole,M9389)在多种细胞模型中展现出显著的促有丝分裂活性。在一项研究中,研究者对C2成肌细胞进行了血清饥饿处理,随后给予不同浓度(0-100 μg/mL)的740 Y-P处理48小时。结果发现,该激动剂在最低测试浓度(1 μg/mL)下即可刺激细胞增殖,而在50 μg/mL浓度时达到最大效应,使S期细胞比例提高至48.3%。值得注意的是,这种促增殖效应在无血清条件下(0.5% FBS)仍然存在,表明其作用不依赖于血清中的生长因子[1]。并且740 Y-P的促有丝分裂活性表现出了高度特异性:这种效应可被PI3K特异性抑制剂LY294002和Wortmannin (SL-2052)阻断,证实其作用机制依赖于PI3K通路的激活[1]。
2. 740 Y-P(740YPDGFR)用于细胞凋亡调控研究
在INS-1大鼠胰腺β细胞模型中,740 Y-P 对细胞凋亡过程表现出显著调控作用。Western blot分析显示,经740 Y-P处理的细胞中,磷酸化Akt(p-Akt)蛋白表达水平显著升高,同时促凋亡蛋白Caspase-3的表达则明显降低(P<0.05)[3]。这一发现表明,740 Y-P通过激活PI3K-Akt信号通路,能够有效抑制细胞凋亡过程,促进细胞存活。同时这一机制对于理解代谢调节过程中β细胞的功能维持具有重要启示意义。在代谢应激条件下,PI3K-Akt信号通路的活性下降可能导致β细胞凋亡增加,而740YP通过特异性激活这一通路,可有效拮抗这一过程。
3. 740 Y-P(PDGFR 740Y-P)用于细胞自噬与应激反应调节
在PC12神经细胞模型中,740 Y-P 展现出对氧化应激诱导的自噬过程的调节能力。研究表明,当PC12细胞暴露于氧化石墨烯(GO)诱导的应激环境时,740 Y-P(30 μM,处理24小时)能够显著抑制GO引起的LC3-II/LC3-I比值变化。LC3蛋白的脂化形式LC3-II是自噬体形成的关键标志物,其水平变化反映了自噬流的活跃程度。这一发现表明,740 Y-P通过激活PI3K-Akt通路,可调节自噬网络[4]。2014年,AbMole的两款抑制剂分别被西班牙国家心血管研究中心和美国哥伦比亚大学用于动物体内实验,相关科研成果发表于顶刊 Nature 和 Nature Medicine。
4. 740 Y-P在动物实验中的研究应用
在动物模型研究中,740 Y-P 展现出良好的体内生物活性和组织穿透能力。740 Y-P不仅能在体外培养细胞中内化,还能在实验动物内与p85亚基发生特异性相互作用。这一特性为其在整体动物水平研究PI3K-Akt信号通路功能奠定了基础。在阿尔茨海默病(AD)大鼠模型中,740 Y-P显示出显著的神经保护潜力。研究采用Aβ(25-32)肽段诱导AD样病理变化,并通过腹膜内注射给予740 Y-P(10 mg/kg剂量,持续6周)。结果显示,740 Y-P能够显著降低海马组织中的活性氧(ROS)水平,同时增强PI3K和Akt的磷酸化程度。这一研究结果表明,740 Y-P可能通过激活PI3K-Akt信号通路,增强神经细胞的抗氧化防御能力,从而减轻氧化应激对神经组织的损伤[5]。在神经病理性疼痛的动物模型研究中,740 Y-P作为PI3K的特异性激活剂,可通过鞘内注射的方式给药。研究发现,740 Y-P在CCI(坐骨神经慢性压迫损伤)模型小鼠中表现出镇痛效果,能够减轻小鼠的触觉和热觉过敏,该机制同样涉及740 Y-P对PI3K信号通路的调节[6]。
三、范例详解
Cell Biol Toxicol. 2022 Apr;38(2):291-310.
中山大学、四川大学华西医学院的科研团队在上述论文中研究了BaP的终代谢产物BPDE诱导滋养层细胞功能异常的机制。主要发现如下:一种新型长链非编码 RNA--lnc-HZ08,被鉴定为在BPDE处理的滋养层组织细胞中高表达。其分子机制是:lnc-HZ08 作为 RNA 支架,与 PI3K 及其泛素连接酶 CBL 结合,增强二者相互作用,促进 PI3K 泛素化降解。进一步研究发现lnc-HZ08 通过下调 PI3K/p-AKT/p-P21/CDK2 通路,抑制滋养层细胞的增殖和迁移。在实验中,AbMole的740 Y-P(AbMole,M9389)被用于验证lnc-HZ08对该通路的调控作用,发现740 Y-P处理可激活PI3K/p-AKT/p-P21/CDK2通路,促进滋养层细胞的增殖;但这种激活效应可被lnc-HZ08过表达减弱,证实lnc-HZ08通过抑制该通路发挥作用[7]。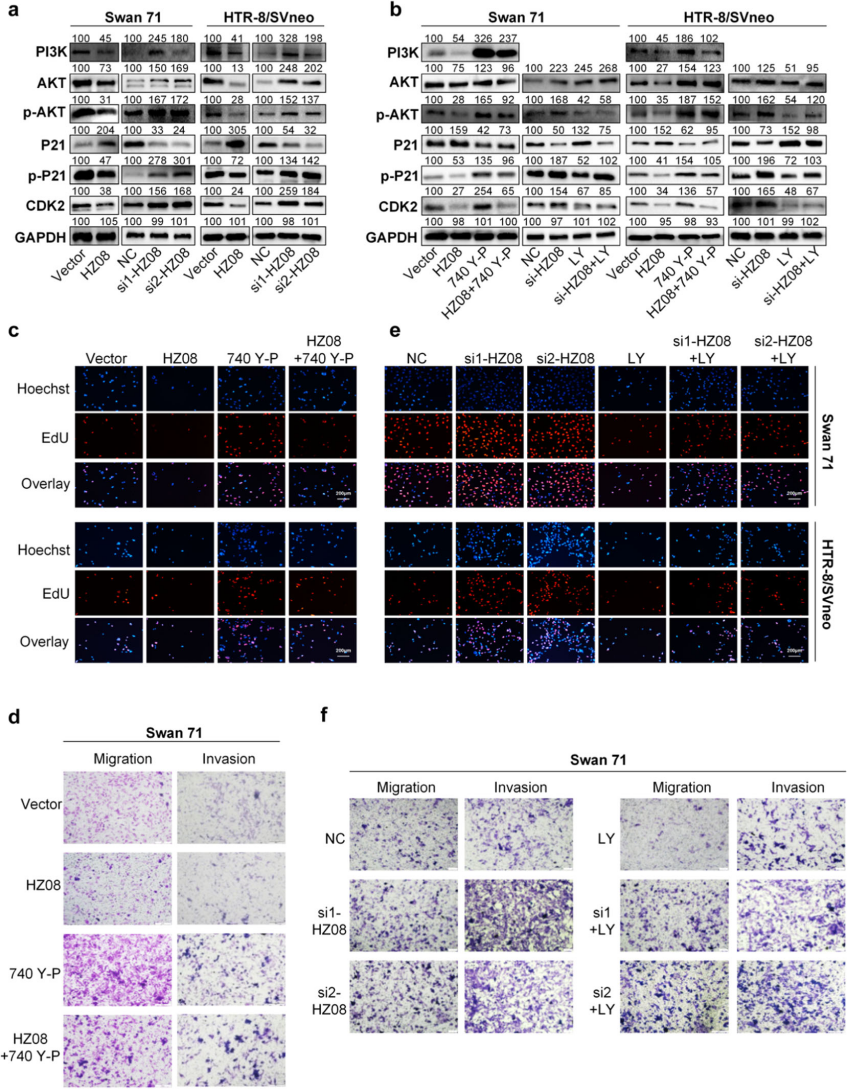

AbMole是ChemBridge中国区官方指定合作伙伴。


参考文献及鸣谢
[1] D. Derossi, E. J. Williams, P. J. Green, et al., Stimulation of mitogenesis by a cell-permeable PI 3-kinase binding peptide, Biochemical and biophysical research communications 251(1) (1998) 148-52.
[2] C. W. Kim, J. M. Lee, S. W. Park, Divergent roles of the regulatory subunits of class IA PI3K, Frontiers in endocrinology 14 (2023) 1152579.
[3] 赵思婷, 王洋洋, 陈玉甜, et al., PI3K-Akt激动剂740 Y-P对INS-1细胞的作用及机制研究, 25(17) (2019) 3.
[4] 冯晓黎, 氧化石墨烯损害自噬流和溶酶体功能诱导PC12细胞系发生p62蛋白依赖性凋亡的机制研究, 南方医科大学.
[5] José A. Barela, Newton Tesima, Vitor Da Silva Amaral, et al., Visually guided eye movements reduce postural sway in dyslexic children, 725 (2020) 134890.
[6] Katarzyna Ciapała, Ewelina Rojewska, Katarzyna Pawlik, et al., Analgesic Effects of Fisetin, Peimine, Astaxanthin, Artemisinin, Bardoxolone Methyl and 740 Y-P and Their Influence on Opioid Analgesia in a Mouse Model of Neuropathic Pain, 24(10) (2023) 9000.
[7] J. Xie, T. Liang, J. Zhao, et al., Lnc-HZ08 regulates BPDE-induced trophoblast cell dysfunctions by promoting PI3K ubiquitin degradation and is associated with miscarriage, Cell biology and toxicology 38(2) (2022) 291-310.
一、740 Y-P(740YPDGFR)的作用机制
740 Y-P(AbMole,M9389)是一种人工设计的多肽化合物,含有25个氨基酸,在第21位的酪氨酸残基被磷酸化修饰,形成关键的p-Tyr结构单元,这一修饰对其生物活性至关重要,使其能够有效模拟天然磷酸化蛋白质,进而与带有SH2结构域的蛋白相互作用。740 Y-P的其余结构也是经过特殊设计的,其N端的16个氨基酸衍生自Antennapedia蛋白的第三螺旋结构,这一区域赋予了它出色的细胞膜穿透能力;C端9个氨基酸则来源于血小板衍生生长因子受体(PDGFR)上的高亲和力p85结合位点,该位点负责特异性识别并激活PI3K的调节亚基--p85。这种巧妙的嵌合设计使740YP兼具细胞渗透性和靶向特异性,成为研究细胞内PI3K信号通路的理想分子工具[1]。


图 1. p85亚基中的SH2结构域[2]
当740 Y-P(AbMole,M9389)进入细胞内部后,C端氨基酸可模拟PDGFR受体的磷酸化酪氨酸基序,与PI3K的p85调节亚基结合,同时磷酸化的Tyr21则与p85中的SH2结构域结合,这种结合将解除p85对PI3K的抑制。进而引发下游Akt的募集和激活。激活的Akt通过磷酸化多种底物蛋白,最终协调促进细胞增殖、抑制凋亡、增强代谢活动等一系列生物学效应[1]。
二、740 Y-P(740YPDGFR)的研究应用
1. 740 Y-P(740YPDGFR)用于细胞增殖与周期调控研究
740 Y-P(AbMole,M9389)在多种细胞模型中展现出显著的促有丝分裂活性。在一项研究中,研究者对C2成肌细胞进行了血清饥饿处理,随后给予不同浓度(0-100 μg/mL)的740 Y-P处理48小时。结果发现,该激动剂在最低测试浓度(1 μg/mL)下即可刺激细胞增殖,而在50 μg/mL浓度时达到最大效应,使S期细胞比例提高至48.3%。值得注意的是,这种促增殖效应在无血清条件下(0.5% FBS)仍然存在,表明其作用不依赖于血清中的生长因子[1]。并且740 Y-P的促有丝分裂活性表现出了高度特异性:这种效应可被PI3K特异性抑制剂LY294002和Wortmannin (SL-2052)阻断,证实其作用机制依赖于PI3K通路的激活[1]。
2. 740 Y-P(740YPDGFR)用于细胞凋亡调控研究
在INS-1大鼠胰腺β细胞模型中,740 Y-P 对细胞凋亡过程表现出显著调控作用。Western blot分析显示,经740 Y-P处理的细胞中,磷酸化Akt(p-Akt)蛋白表达水平显著升高,同时促凋亡蛋白Caspase-3的表达则明显降低(P<0.05)[3]。这一发现表明,740 Y-P通过激活PI3K-Akt信号通路,能够有效抑制细胞凋亡过程,促进细胞存活。同时这一机制对于理解代谢调节过程中β细胞的功能维持具有重要启示意义。在代谢应激条件下,PI3K-Akt信号通路的活性下降可能导致β细胞凋亡增加,而740YP通过特异性激活这一通路,可有效拮抗这一过程。
3. 740 Y-P(PDGFR 740Y-P)用于细胞自噬与应激反应调节
在PC12神经细胞模型中,740 Y-P 展现出对氧化应激诱导的自噬过程的调节能力。研究表明,当PC12细胞暴露于氧化石墨烯(GO)诱导的应激环境时,740 Y-P(30 μM,处理24小时)能够显著抑制GO引起的LC3-II/LC3-I比值变化。LC3蛋白的脂化形式LC3-II是自噬体形成的关键标志物,其水平变化反映了自噬流的活跃程度。这一发现表明,740 Y-P通过激活PI3K-Akt通路,可调节自噬网络[4]。2014年,AbMole的两款抑制剂分别被西班牙国家心血管研究中心和美国哥伦比亚大学用于动物体内实验,相关科研成果发表于顶刊 Nature 和 Nature Medicine。
4. 740 Y-P在动物实验中的研究应用
在动物模型研究中,740 Y-P 展现出良好的体内生物活性和组织穿透能力。740 Y-P不仅能在体外培养细胞中内化,还能在实验动物内与p85亚基发生特异性相互作用。这一特性为其在整体动物水平研究PI3K-Akt信号通路功能奠定了基础。在阿尔茨海默病(AD)大鼠模型中,740 Y-P显示出显著的神经保护潜力。研究采用Aβ(25-32)肽段诱导AD样病理变化,并通过腹膜内注射给予740 Y-P(10 mg/kg剂量,持续6周)。结果显示,740 Y-P能够显著降低海马组织中的活性氧(ROS)水平,同时增强PI3K和Akt的磷酸化程度。这一研究结果表明,740 Y-P可能通过激活PI3K-Akt信号通路,增强神经细胞的抗氧化防御能力,从而减轻氧化应激对神经组织的损伤[5]。在神经病理性疼痛的动物模型研究中,740 Y-P作为PI3K的特异性激活剂,可通过鞘内注射的方式给药。研究发现,740 Y-P在CCI(坐骨神经慢性压迫损伤)模型小鼠中表现出镇痛效果,能够减轻小鼠的触觉和热觉过敏,该机制同样涉及740 Y-P对PI3K信号通路的调节[6]。
三、范例详解
Cell Biol Toxicol. 2022 Apr;38(2):291-310.
中山大学、四川大学华西医学院的科研团队在上述论文中研究了BaP的终代谢产物BPDE诱导滋养层细胞功能异常的机制。主要发现如下:一种新型长链非编码 RNA--lnc-HZ08,被鉴定为在BPDE处理的滋养层组织细胞中高表达。其分子机制是:lnc-HZ08 作为 RNA 支架,与 PI3K 及其泛素连接酶 CBL 结合,增强二者相互作用,促进 PI3K 泛素化降解。进一步研究发现lnc-HZ08 通过下调 PI3K/p-AKT/p-P21/CDK2 通路,抑制滋养层细胞的增殖和迁移。在实验中,AbMole的740 Y-P(AbMole,M9389)被用于验证lnc-HZ08对该通路的调控作用,发现740 Y-P处理可激活PI3K/p-AKT/p-P21/CDK2通路,促进滋养层细胞的增殖;但这种激活效应可被lnc-HZ08过表达减弱,证实lnc-HZ08通过抑制该通路发挥作用[7]。


图 2. Lnc-HZ08 suppresses PI3K/p-AKT/p-P21/CDK2 path way in human trophoblast cells[7]
AbMole是ChemBridge中国区官方指定合作伙伴。


参考文献及鸣谢
[1] D. Derossi, E. J. Williams, P. J. Green, et al., Stimulation of mitogenesis by a cell-permeable PI 3-kinase binding peptide, Biochemical and biophysical research communications 251(1) (1998) 148-52.
[2] C. W. Kim, J. M. Lee, S. W. Park, Divergent roles of the regulatory subunits of class IA PI3K, Frontiers in endocrinology 14 (2023) 1152579.
[3] 赵思婷, 王洋洋, 陈玉甜, et al., PI3K-Akt激动剂740 Y-P对INS-1细胞的作用及机制研究, 25(17) (2019) 3.
[4] 冯晓黎, 氧化石墨烯损害自噬流和溶酶体功能诱导PC12细胞系发生p62蛋白依赖性凋亡的机制研究, 南方医科大学.
[5] José A. Barela, Newton Tesima, Vitor Da Silva Amaral, et al., Visually guided eye movements reduce postural sway in dyslexic children, 725 (2020) 134890.
[6] Katarzyna Ciapała, Ewelina Rojewska, Katarzyna Pawlik, et al., Analgesic Effects of Fisetin, Peimine, Astaxanthin, Artemisinin, Bardoxolone Methyl and 740 Y-P and Their Influence on Opioid Analgesia in a Mouse Model of Neuropathic Pain, 24(10) (2023) 9000.
[7] J. Xie, T. Liang, J. Zhao, et al., Lnc-HZ08 regulates BPDE-induced trophoblast cell dysfunctions by promoting PI3K ubiquitin degradation and is associated with miscarriage, Cell biology and toxicology 38(2) (2022) 291-310.
相关文章
更多 >

