光遗传学的原理、关键要素和操作步骤
2026-04-13 来源:本站 点击次数:120光遗传学(Optogenetics)是将光敏感蛋白基因转入特定细胞(主要是神经元),再通过特定波长光照,精准、快速地控制细胞兴奋或抑制的技术。
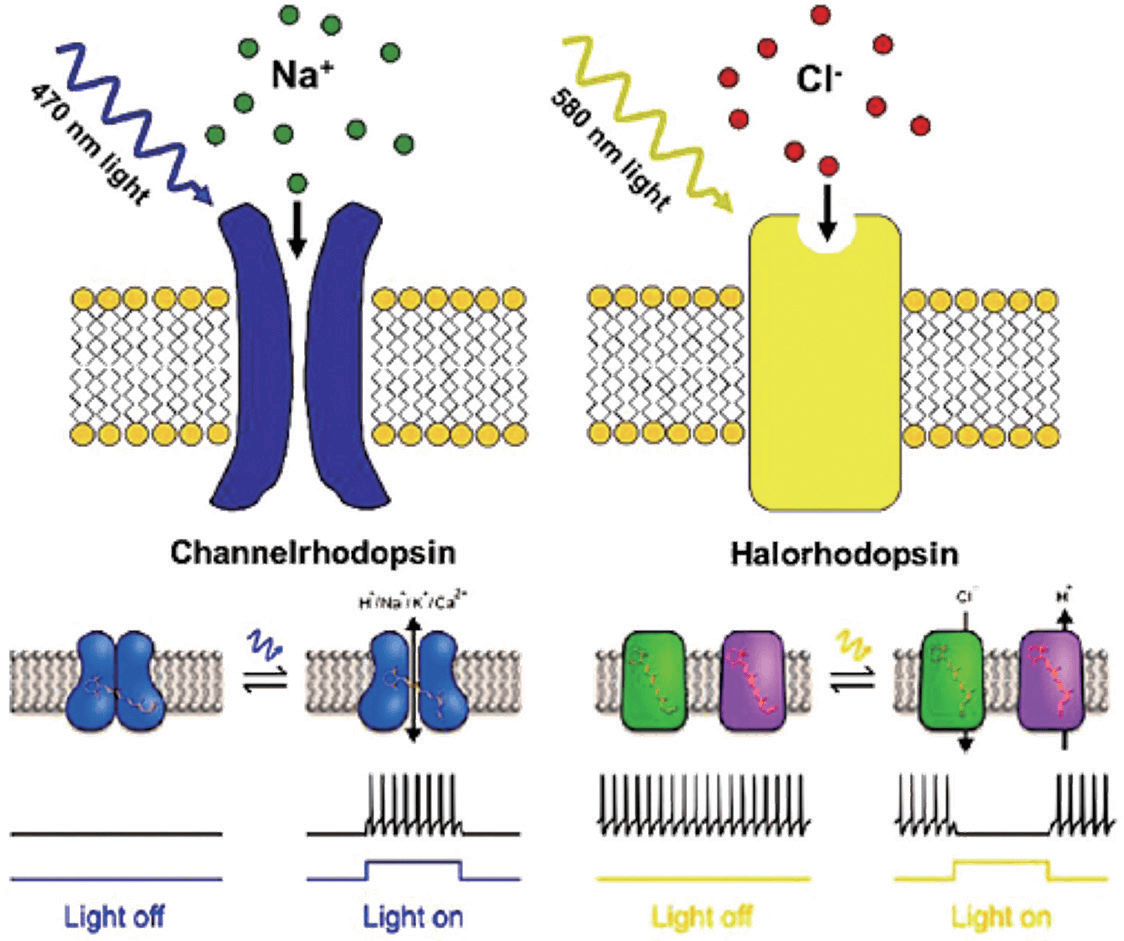 光遗传学的基本原理
光遗传学的基本原理
一、关键要素
1、光敏感蛋白(视蛋白):
激活型:ChR2(通道视紫红质),蓝光(~470 nm)开放,阳离子内流→细胞兴奋
抑制型:NpHR、Arch,黄光 / 绿光开放,氯离子内流或质子外流→细胞抑制
2、光 + 基因
光控开关 + 细胞特异性表达,实现时空精准调控。
二、完整实验操作步骤
在光遗传操作中,细胞会表达特定的编码光敏蛋白的基因,然后使用光来改变细胞的行为。光遗传学技术的应用主要包括以下几个关键步骤:
1. 寻找合适的光敏蛋白
光敏蛋白(也称为视蛋白)是细胞膜上能够感受某一波长光照刺激而产生特定效应的一类膜蛋白,
分为激活型和抑制型两种,能够引起神经元兴奋或抑制。通过多种工程方法对光敏蛋白进行修饰,
形成了光敏感通道视紫红质 (ChR)、嗜盐菌视紫红质 (HR) 和细菌视紫红质 (BR) 等光敏蛋白家族。
① ChR2 由 475 nm 的蓝光激活,是阳离子选择性通道,允许阳离子(如 Na+ )大量内流,
产生动作电位,使神经元处于兴奋状态。此外,ChR 的不同变体也已被开发,包括 CatCh、
ChIEF、ChETA 和 VChR1 等。
② NpHR 氯泵,在 593 nm 的黄光激活下会将氯离子打进神经元内,而抑制神经元活动。
③ Arch 质子泵,在 575 nm 处被黄光或绿光激活,将带正电的质子转移到细胞外。在特定条
件下,可用于增加细胞内 pH 或减少细胞外基质的 pH。
2. 将遗传信息传递给靶细胞
通过转基因动物、转染、病毒感染等方式,将体外合适的光敏蛋白基因靶向导入到受体活细胞中。
目前光遗传学研究中广泛应用的方法为借助病毒载体输送光敏蛋白基因,AAV凭借其低免疫原性、
高组织特异性及无致病性等优势,在光遗传研究中更具吸引力。
3. 可控性演示
通过导入光纤,控制激光实现对神经元活动的精确控制。
4. 实验方法的有效性验证
一般采用电极记录神经元细胞膜内外电压变化,以此来验证光遗传的有效性。
5. 表型检测
通过行为学测试来评估神经元活动对动物行为的影响。

