Biofluidix压电式纳升喷头在3D肿瘤模型构建中的应用与性能优化
2026-04-16 来源:微信公众号 点击次数:169近年来,3D肿瘤模型已成为癌症生物学、药物开发和医学研究的新工具。常见的3D模型包括肿瘤球、类器官、微流体装置等。肿瘤球和类器官是最常用的两种模型,基于不同的细胞来源和制备方案,模拟肿瘤微环境如结构组织、细胞分层、营养和氧气梯度等特征。
然而,这些方法仍存在不足,比如构建初期的肿瘤模型,其细胞密度明显低于天然组织,无法真实模拟肿瘤细胞与基质细胞的相互作用;多需要等待几天甚至几周,后期模型的细胞密度才能与天然组织相当,增加了研究周期。

美国印第安纳州的西拉斐特普渡大学机械工程学院于2023年在《Materials Today Advances》发表该文章,研究开发了一种新的3D肿瘤模型构建方法。利用该方法能够快速制备3D肿瘤模型,细胞密度和生理特性与自然组织类似,同时还可调整墨水成分及打印条件构建不同类型的肿瘤模型。
一、实验方法:
1. 墨水制备
将肿瘤细胞与一种含有I 型大鼠尾胶原蛋白和聚合物(N-异丙基丙烯酰胺-共甲基丙烯酸甲酯)的溶液进行油墨混合,构成含有肿瘤细胞的生物墨水。再将肿瘤基质组织中的主要成分癌症相关成纤维细胞( cancer-associated fibroblasts ,CAFs)用同样方法制成含有CAFs的生物墨水。
2. 喷墨打印
德国Biofluidix公司的纳升级压电式点样喷头Pipejet安装在载物台控制器上,将上述两种墨水用Pipejet点样头以线阵列的方式点印在玻璃孔板中并在37℃固化。固化完成后加入细胞培养基进行培养。(图1)
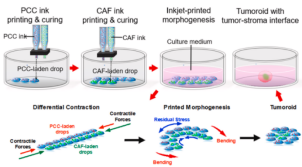
图1 喷墨打印过程的示意图以及组织压缩应力假设机理
3. 组织学观察
取不同时间点的肿瘤模型做免疫荧光染色,通过共聚焦显微镜观察不同时间点肿瘤模型的变化。
二、实验结果:
常规肿瘤球形成验证
已有研究表明,相比于肿瘤细胞,CAF细胞的收缩性更强,因此预期加入培养基后,CAF细胞将收缩得更为紧密,而肿瘤细胞包裹在其周围。最终形成基质细胞在内、肿瘤细胞在外侧的结构(图1)。
在实际实验中,如预期所示,随着时间变化,逐渐形成CAF细胞为致密核心,肿瘤细胞将其完全包裹的肿瘤球(图2,A),且在接下来两个月内持续稳定存在(图2,D)。
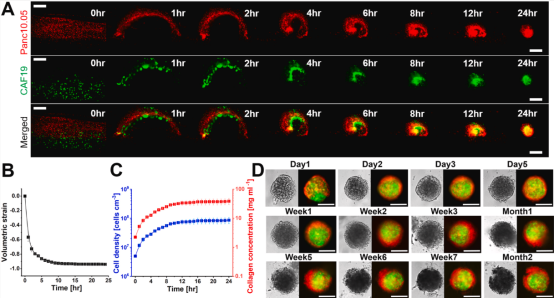
图2 喷墨打印快速形成肿瘤球
(A)主动收缩,0–24 小时延时图像(红色通道:肿瘤细胞,绿色通道:CAF细胞);(B)量化体积应变;(C)细胞密度和胶原浓度的定量;(D)肿瘤球在1天-2个月不同时期的明场和荧光图像(比例尺:500μm)。
通过分析延时图像中细胞占比的面积,可计算出肿瘤球的体积以及响应的细胞密度(图2 ,B-C)。结果显示,在培养24小时后,3D 类肿瘤细胞密度已达到 108 cells/cm³,接近天然组织中肿瘤的细胞密度。说明这种方法可以快速形成类似天然组织细胞密度的肿瘤球。
其他类型肿瘤球形成验证
在上述实验基础上,作者改变打印方式、调整打印温度等,又成功构建了具有3D腔体形状的肿瘤球,以及肿瘤细胞在内侧、CAF细胞在外侧的肿瘤球。
三、实验结论
利用德国Biofluidix公司的纳升级压电式点样喷头Pipejet制备的肿瘤球,可在短时间内形成类似天然组织的细胞密度,大大提升实验效率,还可推广到其他不同类型的细胞和肿瘤球模型,有广泛的应用空间。
更多资讯请访问文章全文链接:https://doi.org/10.1016/j.mtadv.2023.100408
Biofluidix成立于2005年,位于德国,技术源自德国弗莱堡大学微量系统工程学院。
* 专注非接触式的精准纳升和皮升的超微量点样和分液;
* 点样喷头可第三方自动化整合;
* 提供微量分液、芯片点样设备与定制化服务
* 用于微孔板微量移液、微流控快检芯片、生物传感器芯片、电化学芯片、光电芯片以及微阵列生物芯片,包括:核酸芯片,基因芯片,蛋白芯片,多肽芯片、多糖芯片、小分子化合物芯片、细胞芯片。
 |
 |
 |

