脂肪特异性MCP-1缺失调控高脂饮食小鼠肝脏代谢组重塑
2026-04-30 来源:波茨坦仪器 点击次数:142
摘要
单核细胞趋化蛋白 - 1(MCP-1)是介导肥胖相关慢性低 - grade 炎症的核心趋化因子,其在脂肪组织中特异性缺失对肝脏代谢谱的调控作用及与体成分的关联尚未明确。本研究以脂肪特异性 Mcp-1 敲除小鼠为模型,结合 EchoMRI 无创体成分定量与非靶向代谢组学,系统解析脂肪来源 MCP-1 在高脂饮食诱导代谢紊乱中的作用,证实其可独立于体脂表型调控肝脏氨基酸代谢通路,为肥胖相关炎症与代谢综合征干预提供新机制。

图1:论文封面概要
方法
本研究选取野生型(WT)与脂肪特异性 Mcp-1⁻/⁻小鼠,随机分为标准饮食组(AIN93G)与高脂饮食组(HFD),连续干预 12 周。采用EchoMRI-100 体成分分析仪对清醒小鼠进行无创、快速、精准检测,规避麻醉应激干扰,客观量化全身脂肪量与瘦体重;同步采用 ELISA 检测血浆 MCP-1、胰岛素及瘦素水平,利用 GC-TOF-MS 开展肝脏非靶向代谢组学分析,并通过生物信息学挖掘差异代谢物与关键通路。
体成分分析仪应用情况
EchoMRI-100 体成分分析仪为本研究提供核心量化支撑。在清醒无创状态下快速、精准测定小鼠全身脂肪量与瘦体重,避免麻醉应激干扰,客观评估 MCP-1 缺失与高脂饮食对体成分的影响,明确体成分与肝脏代谢组重塑的关联性,是验证代谢表型的关键技术手段。
体成分研究结果
体成分检测结果显示,高脂饮食可使小鼠体脂率显著升高约 50%,瘦体重比例下降 9%,成功构建肥胖相关代谢紊乱模型。在相同饮食条件下,WT 与 Mcp-1⁻/⁻小鼠的体重、体脂量及瘦体重均无统计学差异,表明脂肪特异性 MCP-1 缺失不改变高脂诱导的体成分表型,为后续独立分析代谢组效应排除了体脂干扰。
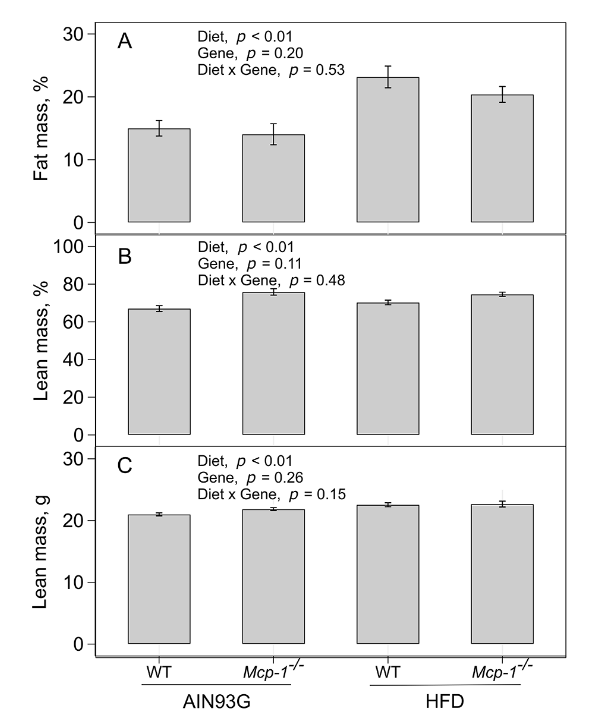
图 2(原文 Fig.2A):高脂饮食显著升高小鼠体脂量,Mcp-1⁻/⁻与 WT 小鼠无明显差异
研究结果
高脂饮食显著上调脂肪组织 MCP-1 表达与血浆水平,脂肪 MCP-1 敲除有效阻断该效应;共鉴定出 87 种有效代谢物,高脂饮食主要下调氨基酸、核苷酸代谢物,Mcp-1⁻/⁻则显著上调上述代谢物,二者作用相反。通路分析显示,MCP-1 缺失显著影响氨酰 - tRNA 生物合成、苯丙氨酸 / 酪氨酸 / 色氨酸合成通路,且不依赖体脂变化。
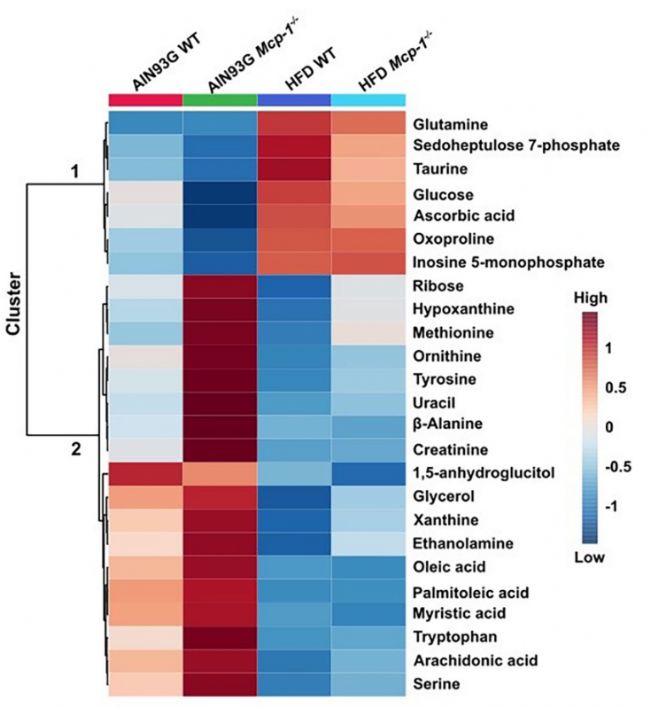
图 3(原文 Fig.5):热图清晰展示 4 组小鼠肝脏差异代谢物,Mcp-1⁻/⁻逆转高脂诱导的代谢紊乱
结论
本研究证实脂肪组织来源 MCP-1 参与调控高脂饮食诱导的肝脏代谢紊乱,且该调控作用独立于体脂表型。高脂饮食抑制肝脏氨基酸代谢,而脂肪特异性 MCP-1 缺失可显著逆转该抑制效应,重塑氨基酸、能量、脂质及核苷酸代谢稳态。EchoMRI 无创精准量化为排除体成分干扰、明确代谢组独立调控效应提供关键技术支撑。
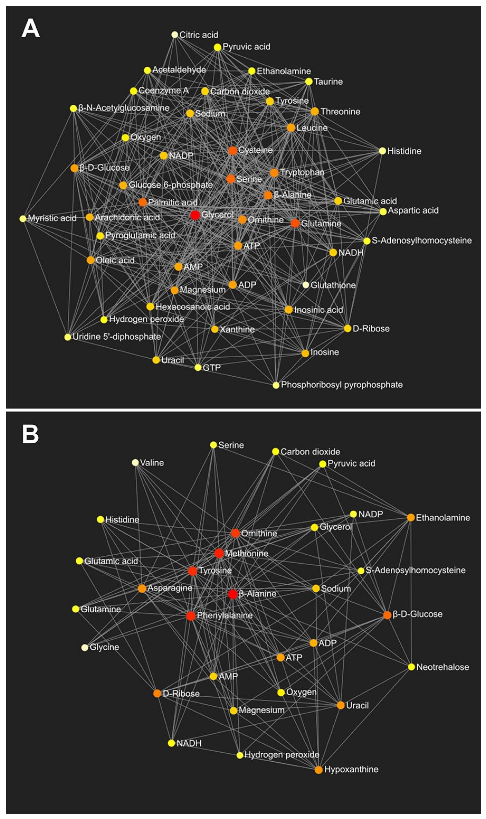
图 4(原文 Fig.7B): Mcp-1⁻/⁻调控的核心代谢网络,聚焦氨基酸代谢通路
文献解决的核心问题
1. 明确脂肪特异性 MCP-1 缺失不改变高脂诱导体成分表型,建立体脂无关的代谢组研究范式。
2. 揭示 MCP-1 可独立调控肝脏氨基酸代谢通路,阐明脂肪炎症影响肝脏代谢的新机制。
3. 发现 MCP-1 缺失能逆转高脂饮食所致代谢紊乱,为肥胖、2 型糖尿病等提供抗炎干预新靶点。
4. 验证 EchoMRI 在代谢组学研究中排除体成分混杂因素的关键价值,完善代谢研究技术体系
原文出处DOI:10.1177/11786388241280859
单核细胞趋化蛋白 - 1(MCP-1)是介导肥胖相关慢性低 - grade 炎症的核心趋化因子,其在脂肪组织中特异性缺失对肝脏代谢谱的调控作用及与体成分的关联尚未明确。本研究以脂肪特异性 Mcp-1 敲除小鼠为模型,结合 EchoMRI 无创体成分定量与非靶向代谢组学,系统解析脂肪来源 MCP-1 在高脂饮食诱导代谢紊乱中的作用,证实其可独立于体脂表型调控肝脏氨基酸代谢通路,为肥胖相关炎症与代谢综合征干预提供新机制。

图1:论文封面概要
方法
本研究选取野生型(WT)与脂肪特异性 Mcp-1⁻/⁻小鼠,随机分为标准饮食组(AIN93G)与高脂饮食组(HFD),连续干预 12 周。采用EchoMRI-100 体成分分析仪对清醒小鼠进行无创、快速、精准检测,规避麻醉应激干扰,客观量化全身脂肪量与瘦体重;同步采用 ELISA 检测血浆 MCP-1、胰岛素及瘦素水平,利用 GC-TOF-MS 开展肝脏非靶向代谢组学分析,并通过生物信息学挖掘差异代谢物与关键通路。
体成分分析仪应用情况
EchoMRI-100 体成分分析仪为本研究提供核心量化支撑。在清醒无创状态下快速、精准测定小鼠全身脂肪量与瘦体重,避免麻醉应激干扰,客观评估 MCP-1 缺失与高脂饮食对体成分的影响,明确体成分与肝脏代谢组重塑的关联性,是验证代谢表型的关键技术手段。
体成分研究结果
体成分检测结果显示,高脂饮食可使小鼠体脂率显著升高约 50%,瘦体重比例下降 9%,成功构建肥胖相关代谢紊乱模型。在相同饮食条件下,WT 与 Mcp-1⁻/⁻小鼠的体重、体脂量及瘦体重均无统计学差异,表明脂肪特异性 MCP-1 缺失不改变高脂诱导的体成分表型,为后续独立分析代谢组效应排除了体脂干扰。

图 2(原文 Fig.2A):高脂饮食显著升高小鼠体脂量,Mcp-1⁻/⁻与 WT 小鼠无明显差异
研究结果
高脂饮食显著上调脂肪组织 MCP-1 表达与血浆水平,脂肪 MCP-1 敲除有效阻断该效应;共鉴定出 87 种有效代谢物,高脂饮食主要下调氨基酸、核苷酸代谢物,Mcp-1⁻/⁻则显著上调上述代谢物,二者作用相反。通路分析显示,MCP-1 缺失显著影响氨酰 - tRNA 生物合成、苯丙氨酸 / 酪氨酸 / 色氨酸合成通路,且不依赖体脂变化。

图 3(原文 Fig.5):热图清晰展示 4 组小鼠肝脏差异代谢物,Mcp-1⁻/⁻逆转高脂诱导的代谢紊乱
结论
本研究证实脂肪组织来源 MCP-1 参与调控高脂饮食诱导的肝脏代谢紊乱,且该调控作用独立于体脂表型。高脂饮食抑制肝脏氨基酸代谢,而脂肪特异性 MCP-1 缺失可显著逆转该抑制效应,重塑氨基酸、能量、脂质及核苷酸代谢稳态。EchoMRI 无创精准量化为排除体成分干扰、明确代谢组独立调控效应提供关键技术支撑。

图 4(原文 Fig.7B): Mcp-1⁻/⁻调控的核心代谢网络,聚焦氨基酸代谢通路
文献解决的核心问题
1. 明确脂肪特异性 MCP-1 缺失不改变高脂诱导体成分表型,建立体脂无关的代谢组研究范式。
2. 揭示 MCP-1 可独立调控肝脏氨基酸代谢通路,阐明脂肪炎症影响肝脏代谢的新机制。
3. 发现 MCP-1 缺失能逆转高脂饮食所致代谢紊乱,为肥胖、2 型糖尿病等提供抗炎干预新靶点。
4. 验证 EchoMRI 在代谢组学研究中排除体成分混杂因素的关键价值,完善代谢研究技术体系
原文出处DOI:10.1177/11786388241280859
相关文章
更多 >

