文献解读:慢性压力通过ADRB2破坏肝脏稳态并加速肝癌进展的研究
2026-05-13 来源:本站 点击次数:72
2026 年 5 月 1 日,上海科技大学胡霁团队、上海交通大学李露团队与华南理工大学兰月团队合作,在Science Advances上发表题为“Chronic stress disrupts hepatic homeostasis and accelerates liver cancer progression through ADRB2 signaling”的研究论文,该研究借助单细胞核 RNA 测序、组织病理评估、原位肝癌模型构建、药理干预与临床样本验证等多种技术手段,系统揭示慢性应激可从细胞组成、分子通路、生理功能与组织病理等多个层面破坏肝脏稳态,促使肝脏向促肿瘤微环境转变;同时证实慢性应激能够不依赖驱动基因类型,显著加速肝癌恶性进展。机制上,该研究明确 β2 - 肾上腺素能受体 ADRB2 介导的肾上腺素能信号是慢性应激促进肝癌进展的核心通路,肝细胞上的 ADRB2 可直接调控肿瘤细胞增殖,在压力促癌过程中发挥关键作用。临床样本分析进一步验证 ADRB2 在肝癌组织中高表达且与患者不良预后密切相关,阻断 ADRB2 信号能够有效逆转应激对肝癌的促进作用。该研究构建了完整的脑 - 肝轴调控理论,为阐释心理应激与肝脏疾病的关联提供了全新理论依据,同时为肝癌的预后评估与临床干预提供了新型靶点,也凸显了压力管理在肝脏疾病防治中的重要临床价值。
01 研究方法
1.1 实验动物与模型构建
选用C57BL/6J 小鼠作为实验对象,构建慢性束缚应激模型模拟慢性压力,通过长期束缚处理使小鼠呈现稳定的应激状态;构建慢性不可预知应激模型,用于模拟肿瘤形成后持续的心理压力状态。采用两种原位肝癌模型,分别为 Akt;Nras 驱动型肝癌模型与 ΔN90-β-catenin;c-Met 驱动型肝癌模型,通过流体动力学尾静脉注射将相关质粒导入小鼠肝细胞,诱导肝脏原位成瘤。构建肝细胞特异性 ADRB2 敲除小鼠,结合腺相关病毒递送 Cre 重组酶,实现肝细胞中 ADRB2 的特异性敲除。
1.2 组织与细胞检测技术
对小鼠肝脏组织进行病理染色,包括油红O 染色、苏木精 - 伊红染色,观察肝脏组织形态、脂滴沉积与肿瘤病变情况;采用免疫荧光染色检测肝脏组织中目标蛋白的表达与定位,包括肿瘤增殖标志物、肾上腺素能受体、神经纤维标志物等。利用流式细胞术分析肿瘤微环境中免疫细胞的组成及 ADRB2 在免疫细胞上的表达水平;通过磁激活细胞分选技术分离纯化肝细胞与肝脏非实质细胞,用于后续分子检测。
1.3 转录组学与生物信息学分析
运用单细胞核RNA 测序技术,解析正常肝脏与应激状态下肝脏的细胞组成及各类细胞的转录组变化,明确压力对肝脏不同细胞类型的调控效应;开展批量 RNA 测序,分析应激组与对照组肝脏组织的差异表达基因,进行功能富集与基因集富集分析,挖掘关键调控通路。借助 TCGA 数据库分析人类肝癌样本中 ADRB2 信号通路的表达水平,及其与患者临床预后的相关性。
1.4 药理干预与生理生化检测
使用 ADRB2 抑制剂普萘洛尔进行药理干预,通过饮水给药方式阻断 ADRB2 信号,验证该信号在压力促肝癌进程中的作用。检测小鼠血清中肝功能相关指标,评估肝脏损伤程度;检测小鼠血糖、凝血功能等生理指标,分析压力对肝脏代谢与凝血功能的影响;统计小鼠肿瘤负荷、增殖水平与生存情况,评估压力与药物干预对肝癌进展的作用。
02 研究内容
2.1 慢性压力损伤肝脏稳态
研究首先探究慢性压力对肝脏正常生理功能的影响,通过慢性束缚应激处理小鼠后,开展肝脏转录组解析、组织病理检测与血液生化分析。单细胞核RNA 测序结果显示,慢性压力改变了肝脏的细胞组成比例,肝细胞占比上升,肝脏巨噬细胞等非实质细胞比例下降,提示肝脏免疫微环境发生紊乱。
对肝细胞的转录组富集分析表明,对照组肝细胞富集正常肝脏生理功能相关通路,而应激组肝细胞激活大量应激响应与疾病相关通路,说明压力从分子层面改变肝细胞功能状态。生理生化检测显示,慢性压力引发小鼠血糖升高、凝血功能异常,肝脏组织出现明显脂肪变性,呈现脂肪肝早期病变特征;同时肝功能损伤指标显著上升,证实慢性压力造成实质性肝脏损伤。
批量 RNA 测序的基因集富集分析进一步验证,应激状态下肝脏组织中非酒精性脂肪肝与肝癌进展相关基因集显著富集,表明慢性压力不仅破坏肝脏稳态,还促使肝脏向促肿瘤的病理状态转变。
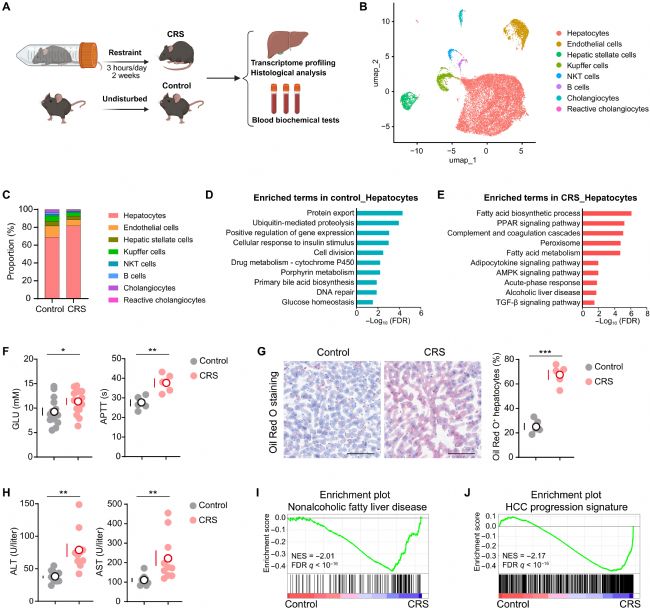
图 1:慢性压力损害肝脏稳态
2.2 慢性压力加速 Akt;Nras 驱动型肝癌进展
为明确慢性压力对肝癌的作用,研究构建 Akt;Nras 驱动的原位肝癌模型,先对小鼠进行慢性束缚应激,再诱导肝癌形成。结果显示,应激组与对照组小鼠初始体重无显著差异,但应激处理后小鼠体重明显下降,证明应激模型构建有效。
两组小鼠均形成肝脏肿瘤,但应激组小鼠的肿瘤占肝脏面积比例、肿瘤数量与肿瘤大小均显著高于对照组,提示慢性压力显著增加肿瘤负荷。免疫荧光检测肿瘤增殖标志物显示,应激组肿瘤细胞的增殖活性明显更高,进一步证实压力促进肝癌细胞增殖。同时,应激组小鼠的肝功能损伤指标显著升高,说明慢性压力在加速肿瘤进展的同时,加重肝脏功能损伤。
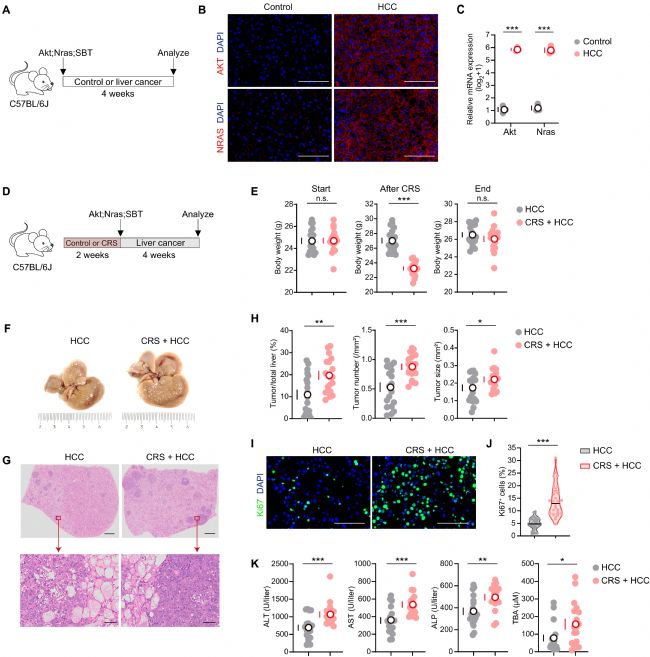
图 2:慢性压力加速 Akt;Nras 驱动型肝癌的进展
2.3 慢性压力加速 ΔN90-β-catenin;c-Met 驱动型肝癌进展
为验证上述结果的普适性,研究更换肝癌驱动基因,构建ΔN90-β-catenin;c-Met 驱动的原位肝癌模型。实验设计与前一模型一致,先施加慢性应激再诱导肝癌。结果显示,应激组小鼠同样出现体重下降,且生存时间显著缩短,提示压力加速肝癌恶性进展,降低小鼠存活率。
病理分析结果表明,应激组小鼠的肿瘤负荷同样显著高于对照组,肿瘤增殖活性也明显增强,肝功能损伤程度更严重。该结果证实,无论肝癌由何种驱动基因诱发,慢性压力均能发挥促癌作用,说明压力加速肝癌进展具有不依赖驱动基因类型的普遍性。
此外,研究还在肿瘤形成后施加慢性应激,结果显示即使肿瘤已建立,慢性压力仍能显著增加肿瘤负荷,证明压力在肝癌发生的全周期均能发挥促进展作用。
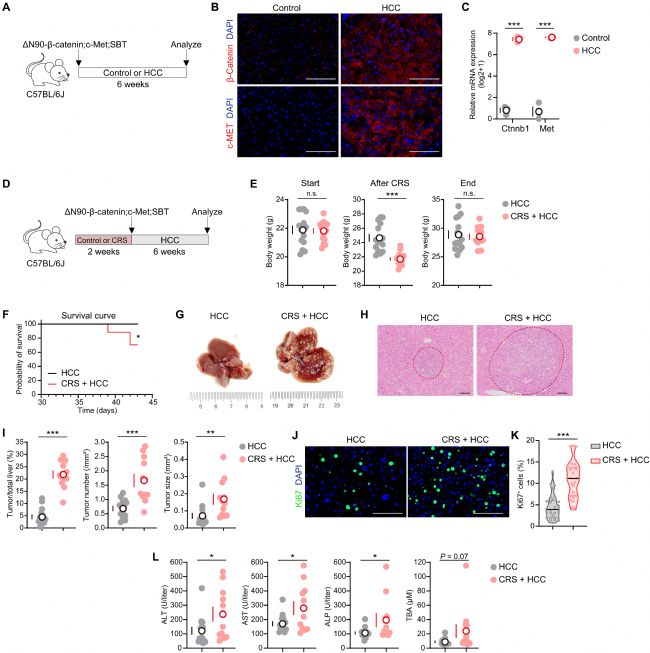
图 3:慢性压力加速 ΔN90-β-catenin;c-Met 驱动型肝细胞癌的进展
2.4 肾上腺素能信号参与压力介导的肝癌进展
为挖掘压力促肝癌的分子机制,研究对应激肝癌组与单纯肝癌组开展转录组对比分析。功能富集结果显示,单纯肝癌组富集代谢相关通路,而应激肝癌组富集促肿瘤发生与神经信号相关通路,提示交感神经信号参与其中。免疫荧光检测证实,应激状态下肝脏交感神经纤维密度增加,交感神经激活释放的儿茶酚胺可能是关键调控分子。
基因集富集分析显示,肾上腺素能信号通路在肝癌组织中显著富集,提示该信号参与肝癌进程。进一步筛查肾上腺素能受体家族表达发现,ADRB2 是肝癌组织中显著高表达且上调最显著的受体,免疫荧光也证实 ADRB2 在肝癌细胞上高表达。
药理阻断实验显示,使用普萘洛尔抑制 ADRB2 后,应激组小鼠的肿瘤负荷显著降低,肿瘤细胞增殖受到抑制,肝功能损伤得到缓解,证明 ADRB2 信号是慢性压力加速肝癌进展的关键通路。
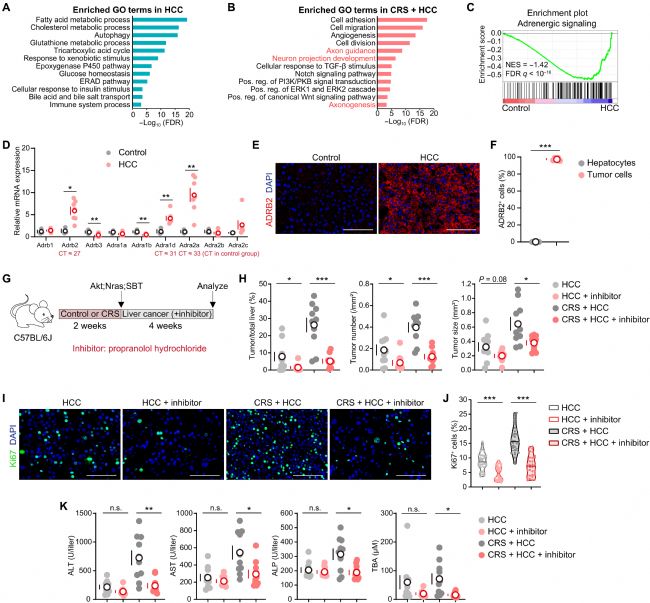
图 4:肾上腺素能信号参与 Akt;Nras 驱动型肝癌的进展
2.5 肝细胞 ADRB2 直接调控肝癌进展
为明确ADRB2 的细胞作用靶点,研究分析肿瘤微环境中 ADRB2 的表达分布,发现 ADRB2 不仅表达于肝癌细胞,也表达于多种免疫细胞表面。为排除免疫细胞的间接影响,研究构建肝细胞特异性 ADRB2 敲除模型。
转录组分析显示,敲除肝细胞ADRB2 后,细胞增殖相关通路显著下调,提示 ADRB2 通过调控增殖信号影响肝癌进展。功能实验证实,肝细胞特异性敲除 ADRB2 后,慢性压力介导的肿瘤负荷增加、细胞增殖增强效应均被显著逆转,证明肝细胞 ADRB2 是压力促肝癌的关键介导分子。
临床样本验证显示,人类肝癌组织中 ADRB2 高表达比例显著高于癌旁组织,TCGA 数据库分析表明,ADRB2 信号通路高表达的肝癌患者,总生存期与无病生存期均显著缩短,证实 ADRB2 信号与人类肝癌恶性进展及不良预后密切相关。
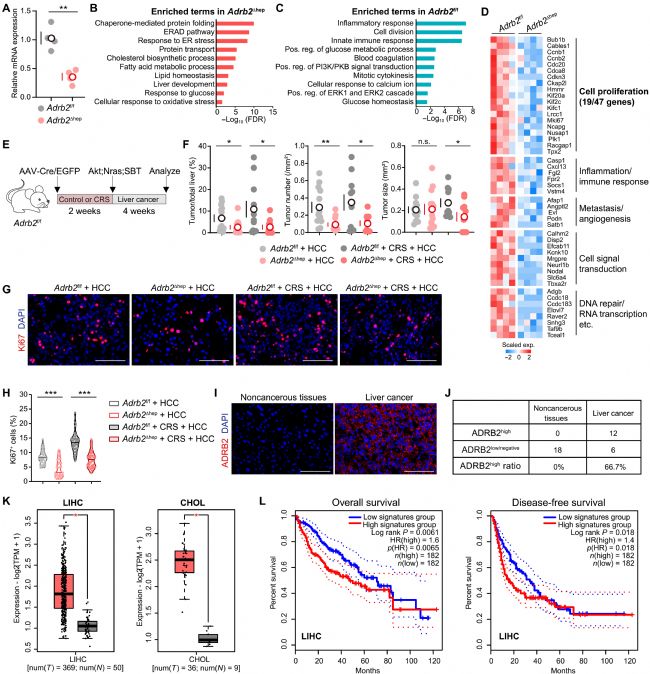
图 5:肝脏 ADRB2 促进肝癌进展
03 创新点
采用原位肝癌模型模拟生理状态下的肿瘤发生,还原肝脏天然微环境与神经支配特征,弥补既往皮下移植模型无法模拟生理压力调控的缺陷,使研究结论更贴近人类肝癌病理过程。系统揭示慢性压力对肝脏稳态的全方位损伤,从细胞组成、分子通路、生理功能到组织病理,完整阐明压力诱导肝脏向促肿瘤状态转变的过程。
明确ADRB2 是慢性压力加速肝癌进展的核心分子,建立完整的 “慢性压力 - 交感神经激活 - 儿茶酚胺释放 - ADRB2 激活 - 肝癌进展” 调控轴,完善脑 - 肝轴调控肝脏肿瘤的理论体系。突破既往压力主要通过免疫抑制促癌的认知,证实肝细胞 ADRB2 的直接促增殖作用是压力加速肝癌的关键机制,明确肿瘤细胞内在调控的核心地位。
实现基础研究与临床转化的紧密结合,证实ADRB2 可作为肝癌预后标志物,且经典 β 受体阻滞剂可有效逆转压力的促癌效应,为肝癌临床干预提供可快速转化的新策略。结合单细胞核 RNA 测序技术,精准解析压力对肝脏不同细胞类型的调控效应,实现细胞水平的机制解析,提升研究的精细度与可信度。
04 启发
临床诊疗中应重视心理状态对肝脏疾病与肝癌的影响,将压力评估与管理纳入肝癌患者的常规诊疗流程,通过心理干预缓解患者慢性压力,降低压力对肿瘤进展的促进作用。ADRB2 可作为肝癌预后评估的新型分子标志物,通过检测肿瘤组织中 ADRB2 的表达水平,辅助判断患者预后,指导临床治疗方案的选择。
β 受体阻滞剂这类已临床应用的成熟药物,可尝试用于高压力水平或 ADRB2 高表达的肝癌患者,作为辅助治疗手段阻断压力介导的促癌信号,为肝癌治疗提供新的联合用药思路。神经 - 内分泌 - 肿瘤调控网络是肿瘤研究的重要方向,肝脏作为受交感神经密集支配的器官,其器官特异性的神经调控机制值得进一步深入挖掘,为其他肿瘤的神经调控研究提供参考。
基础肿瘤研究应优先选择原位、自发肿瘤模型,最大程度还原体内生理病理状态,提升研究结果的临床转化价值;同时应注重心理、神经等系统因素对肿瘤的影响,突破单纯聚焦肿瘤细胞的研究局限。慢性压力是肝脏疾病发生发展的重要危险因素,保持良好的心理状态、减少长期应激暴露,对维持肝脏稳态、预防肝脏疾病及延缓肝癌进展具有重要意义。
参考文献:
Huimin Qin et al. ,Chronic stress disrupts hepatic homeostasis and accelerates liver cancer progression through ADRB2 signaling.Sci. Adv.12,eaec0825(2026).DOI:10.1126/sciadv.aec0825
团队介绍:
本研究由三支优势互补团队联合完成:上海科技大学胡霁团队专注应激神经生物学与神经环路调控,为研究提供神经机制支撑;上海交通大学李露团队主攻肝脏疾病与脑 - 肝互作调控,负责肝脏病理与肿瘤机制研究;华南理工大学兰月团队聚焦神经康复与身心应激干预,提供临床转化视角。三团队协同攻关,系统揭示慢性压力通过 ADRB2 信号破坏肝脏稳态、加速肝癌进展的新机制,为肝癌防治与压力管理提供重要理论基础。
厚谱实验室(脑体互作研究—神经药效评价实验室)专注于脑体互作机制解析与神经药效精准评价的尖端实验技术高地。可以开展清醒动物小分子取样分析、神经递质代谢产物实时分析、癫痫睡眠脑电采集分析、在体电生理记录分析、脑机接口方案评价(大动物脑部手术)、神经调控、组织透明化、脊髓损伤康复验证实验电生理(SEP)、脑立体定位给药、自动无接触采血分析、葡萄糖钳夹实验、行为学迷宫实验和动物造模等各种动物实验服务!
-END-


想了解更多内容,获取相关咨询请联系
电 话:+86-0731-84428665
伍经理:+86-180 7516 6076
工程师:+86-180 7311 8029
邮 箱:consentcs@163.com


