双效硒纳米药物经“肝 - 脑轴”修复线粒体治疗帕金森病的研究
2026-05-15 来源:本站 点击次数:88
2026 年 4 月 25 日,贵州医科大学张春林教授、汤磊教授,联合中国科学院上海药物研究所于海军研究员等团队,在《Advanced Composites and Hybrid Materials》在线发表了题为“Dual-action selenium nanodrugs confer synergistic protection against Parkinson’s Disease via mitochondrial-targeted antioxidant therapy and selenoprotein p-mediated selenium mobilization”的研究论文。该研究构建了谷胱甘肽修饰的硒纳米药物(GSe NPs),系统阐明其通过线粒体靶向直接清除活性氧与肝脏上调 SelP 实现内源性抗氧化激活的双重协同机制,有效阻断“线粒体损伤 - ROS - 神经炎症”的病理循环,在细胞、线虫及小鼠帕金森模型中显著保护多巴胺神经元、改善运动与认知功能障碍,并展现出良好的生物安全性。
该研究不仅揭示了“肝脏 - SelP - 脑”调控轴在帕金森病治疗中的关键作用,也提出了“外源直接抗氧化 + 内源硒动员”的新型协同治疗范式,为帕金森病的疾病修饰治疗提供了安全、高效且具备临床转化潜力的纳米药物新策略,对推动神经退行性疾病的靶向递送与机制干预具有重要参考价值。
01 研究方法
1.1 纳米药物的合成与表征
以谷胱甘肽为还原剂,采用一步法室温合成 G-Se NPs,通过透析纯化获得终产物。利用扫描电镜、透射电镜、原子力显微镜观察纳米颗粒形貌与尺寸,动态光散射检测水合粒径与电位,X 射线光电子能谱与傅里叶变换红外光谱分析化学组成与键合方式,紫外-可见光谱表征光学特性,电子自旋共振评估自由基清除能力,电感耦合等离子体质谱检测硒元素释放行为。
1.2 体外细胞水平研究
选用 PC12 与 SH-SY5Y 细胞构建 6-OHDA 损伤帕金森病细胞模型,通过 CCK-8 法与活 / 死染色评估细胞活力与纳米药物生物相容性,溶血实验检测血液相容性。利用荧光探针与激光共聚焦显微镜观察纳米药物细胞摄取、内吞途径与细胞器共定位,透射电镜观察线粒体形态,荧光染色检测线粒体活性氧、线粒体膜电位与线粒体 DNA 氧化损伤,生化试剂盒检测氧化应激相关指标,免疫荧光与蛋白免疫印迹检测 α-突触核蛋白、酪氨酸羟化酶及凋亡相关蛋白表达。
1.3 线虫水平研究
以 6 - OHDA 诱导构建帕金森病线虫模型,通过荧光成像观察纳米药物在虫体内的蓄积情况,荧光探针检测虫体活性氧水平,转基因线虫观察线粒体形态与多巴胺神经元完整性,记录线虫寿命变化,并通过基础运动减缓、乙醇规避、区域限制性搜索等行为学评估运动功能改善效果。
1.4 小鼠体内分布与代谢研究
构建 MPTP 诱导的帕金森病小鼠模型,通过尾静脉、腹腔、灌胃、鼻腔四种途径给药,利用活体荧光成像与离体器官荧光成像,观察纳米药物在脑、肝、肾等主要器官的分布特征,通过脑组织冰冻切片与免疫荧光验证纳米药物在黑质区的富集与线粒体共定位情况。
1.5 小鼠行为学与病理评价
通过旷场实验、转棒实验、爬杆实验评估小鼠运动功能,Y 迷宫、高架十字迷宫、水迷宫检测认知与焦虑相关行为。利用尼氏染色观察神经元形态,免疫组化与免疫荧光检测酪氨酸羟化酶、α-突触核蛋白、胶质纤维酸性蛋白、小胶质细胞标记物及炎症因子表达,蛋白免疫印迹检测硒蛋白 P 与凋亡相关蛋白表达。通过血常规、血生化与主要脏器苏木精伊红染色评估体内生物安全性。
1.6 分子机制研究
对小鼠脑组织进行转录组测序,通过差异基因分析、基因本体富集与京都基因与基因组百科全书通路分析,筛选关键调控通路与硒蛋白相关基因。结合蛋白免疫印迹、酶联免疫吸附实验验证肝脏与脑内硒蛋白 P 的表达变化,明确纳米药物通过肝脏调控硒蛋白 P 合成并介导脑内神经保护的核心机制。
02 研究内容
2.1 G - Se NPs 的合成与抗氧化活性表征
研究采用谷胱甘肽一步还原亚硒酸钠,成功制备出形貌均一、分散性良好的球形 G-Se NPs,颗粒尺寸适宜,胶体稳定性优异,符合脑部递送的基本要求。元素分布分析证实硒元素在纳米颗粒中均匀分布,化学键合分析表明谷胱甘肽与硒成功结合,形成稳定的纳米结构。
抗氧化实验结果显示,G-Se NPs 具有类超氧化物歧化酶与过氧化氢酶活性,可高效清除羟基自由基、超氧阴离子与过氧化氢等多种活性氧,在氧化应激环境下可实现硒元素的响应性释放,既能保证抗氧化效果,又可避免游离硒过量导致的毒性。
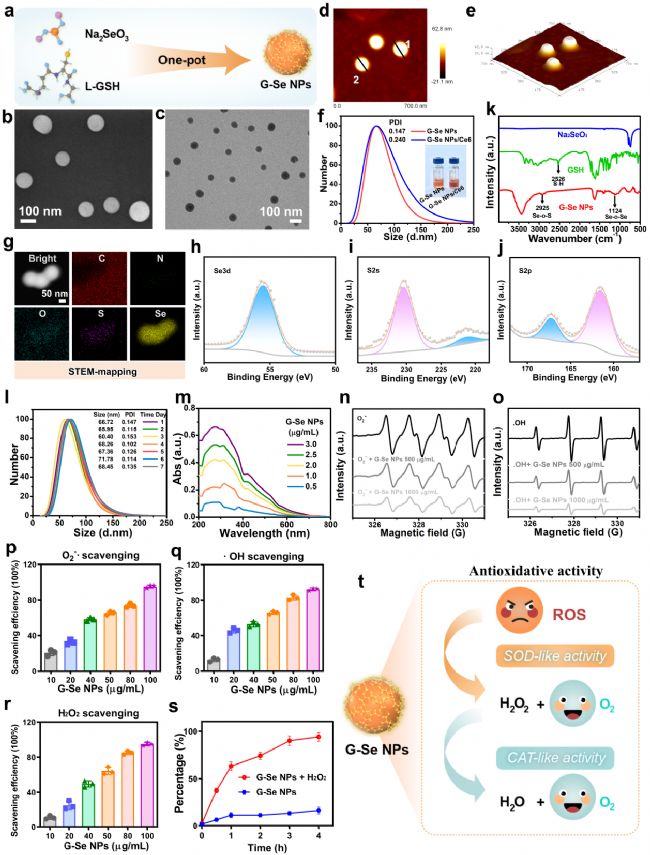
图1:G-Se NPs 具备优异的物理化学稳定性与抗氧化能力。
2.2 G-Se NPs 的细胞摄取、靶向定位与体外保护作用
生物相容性实验证实,G-Se NPs 在有效治疗浓度范围内对神经细胞无明显毒性,血液相容性良好,满足体内应用的安全要求。细胞摄取实验表明,G-Se NPs 主要通过网格蛋白介导的能量依赖型内吞途径进入细胞,且可特异性富集于神经元线粒体,少量分布于溶酶体,实现精准的线粒体靶向递送。
在 6-OHDA 诱导的帕金森病细胞模型中,G-Se NPs 可显著降低细胞与线粒体活性氧水平,恢复线粒体膜电位,减轻线粒体肿胀与结构损伤,减少线粒体 DNA 氧化损伤。同时可降低脂质过氧化水平,恢复细胞内抗氧化系统功能,抑制 α-突触核蛋白异常聚集,提升酪氨酸羟化酶表达,减少细胞凋亡,显著提高神经元存活率。
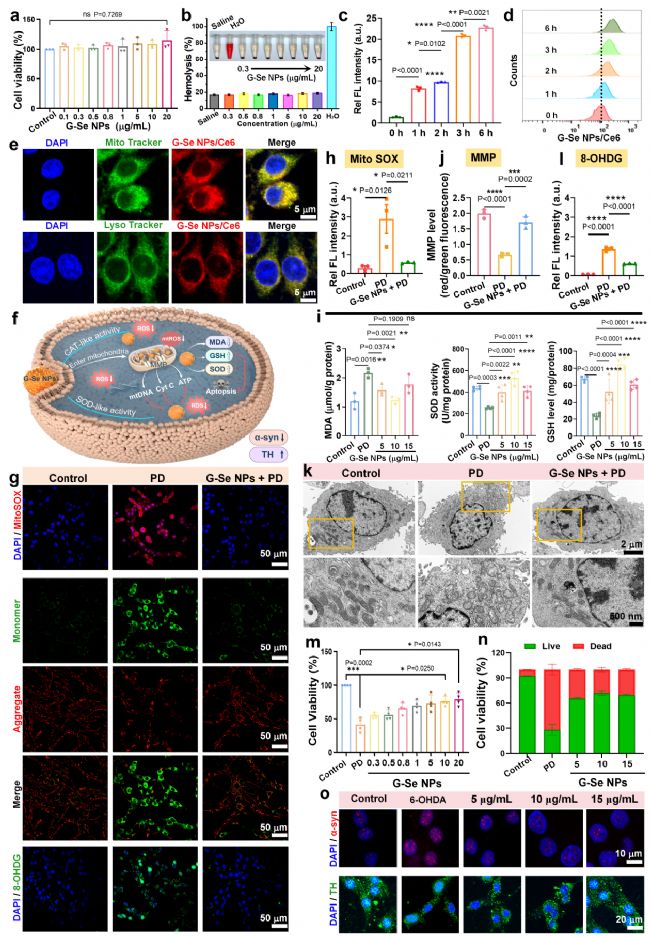
图2:G-Se NPs 可通过线粒体靶向清除活性氧,实现体外神经保护作用。
2.3 G-Se NPs 对线虫帕金森模型的保护作用
在线虫模型中,G-Se NPs 可通过摄食与皮肤渗透两种途径进入虫体,且不影响线虫正常生长发育,生物相容性良好。G-Se NPs 可显著降低 6-OHDA 诱导的线虫体内活性氧堆积,保护线粒体结构完整性与功能稳定性,有效逆转多巴胺神经元损伤与轴突退化。
同时,G-Se NPs 可显著延长帕金森病线虫的寿命,改善多巴胺能神经元依赖的运动行为缺陷,恢复线虫正常的探索、觅食与规避能力。
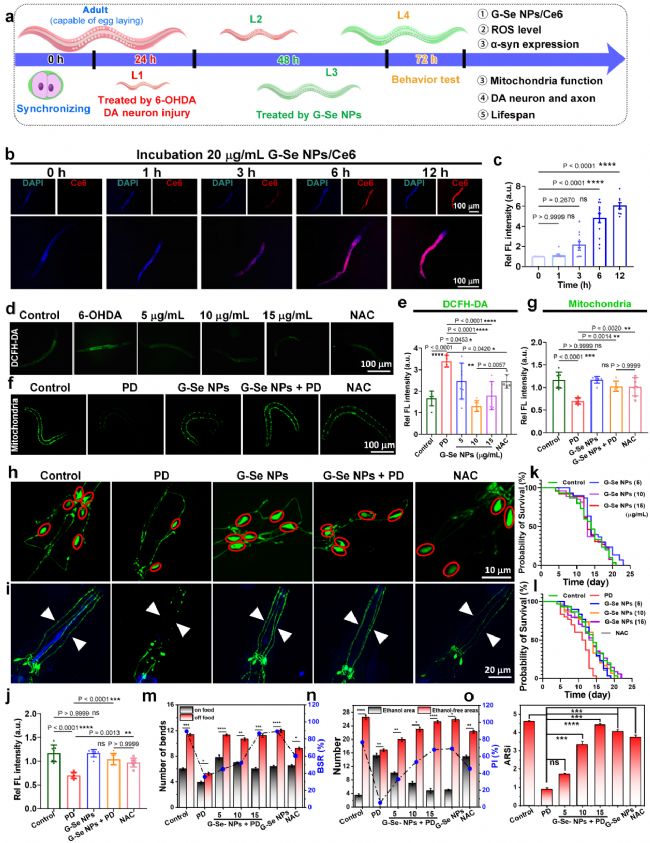
图3:G-Se NPs 在整体动物水平可发挥抗氧化、线粒体保护与神经修复作用。
2.4 G-Se NPs 在小鼠体内的靶向分布特征
不同给药途径对比结果显示,尾静脉注射可使 G-Se NPs 更高效地穿透血脑屏障进入脑组织,是最优的脑部递送方式。在帕金森病小鼠体内,G-Se NPs 可快速富集于脑组织,并在黑质区特异性聚集,同时可大量分布于肝脏组织,为肝脏调控硒蛋白合成提供结构基础。
纳米药物在脑内的蓄积具有时间依赖性,在帕金森病小鼠脑中的富集量显著高于正常小鼠,具备疾病靶向优势。亚细胞定位证实 G-Se NPs 在脑内可与神经元线粒体共定位,进一步支持其线粒体靶向保护机制。
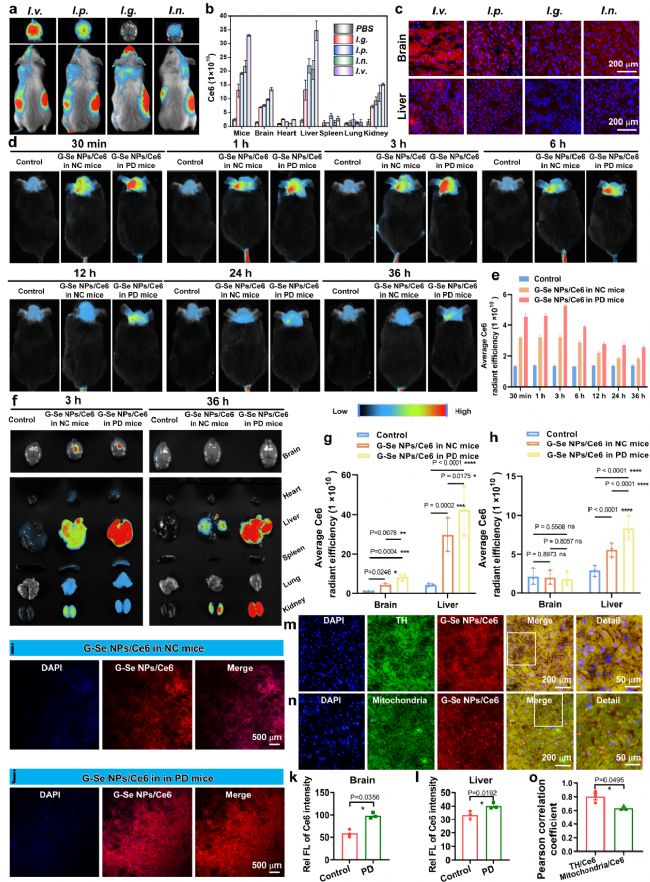
图4:明确了 G-Se NPs 可跨越血脑屏障、靶向脑内损伤区域的体内递送特征。
2.5 G-Se NPs 对小鼠运动与认知功能的改善作用
在 MPTP 诱导的帕金森病小鼠模型中,G-Se NPs 可显著改善模型小鼠的运动功能障碍,提升自主活动能力、运动协调能力与平衡能力,缓解运动迟缓症状。同时可有效逆转模型小鼠的认知损伤,改善工作记忆、空间学习与记忆能力,缓解焦虑样行为。
在整个行为学评估过程中,单纯给予 G-Se NPs 对正常小鼠无不良影响,证实该纳米药物在发挥治疗作用的同时不干扰正常神经功能。
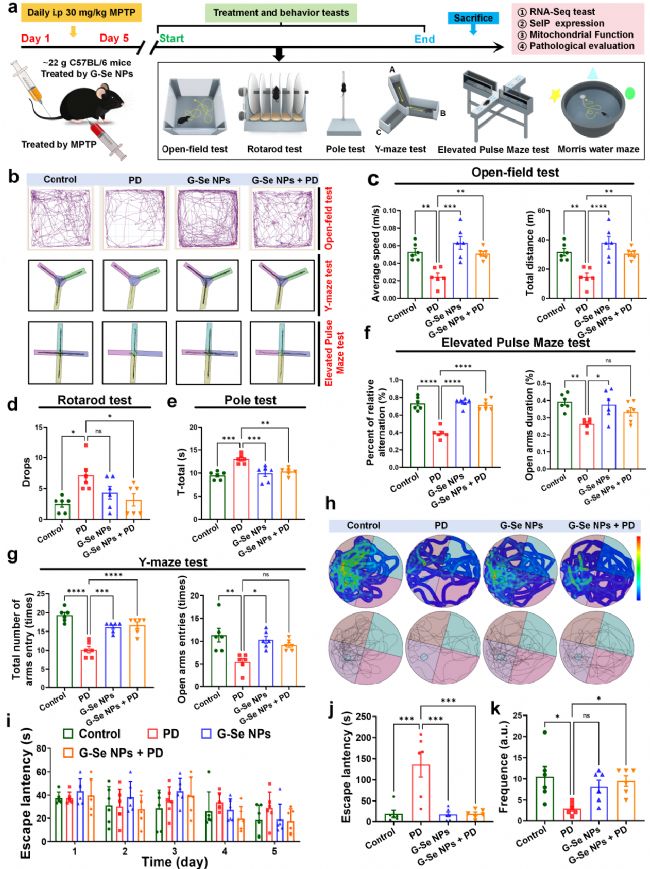
图5:G-Se NPs 可全面改善帕金森病相关的运动与非运动症状。
2.6 G-Se NPs 对小鼠脑组织病理损伤的修复作用
病理染色结果显示,G-Se NPs 可显著减轻帕金森病小鼠海马区与黑质区神经元损伤,维持神经元形态完整与数量稳定。免疫组化与荧光结果证实,G-Se NPs 可显著提升黑质区酪氨酸羟化酶表达,保护多巴胺神经元功能,抑制 α-突触核蛋白异常聚集,阻断核心病理进程。
体内安全性评价表明,G-Se NPs 对小鼠肝肾功能、血常规指标无明显影响,主要脏器无病理性改变,具备良好的体内生物安全性,适合长期给药。
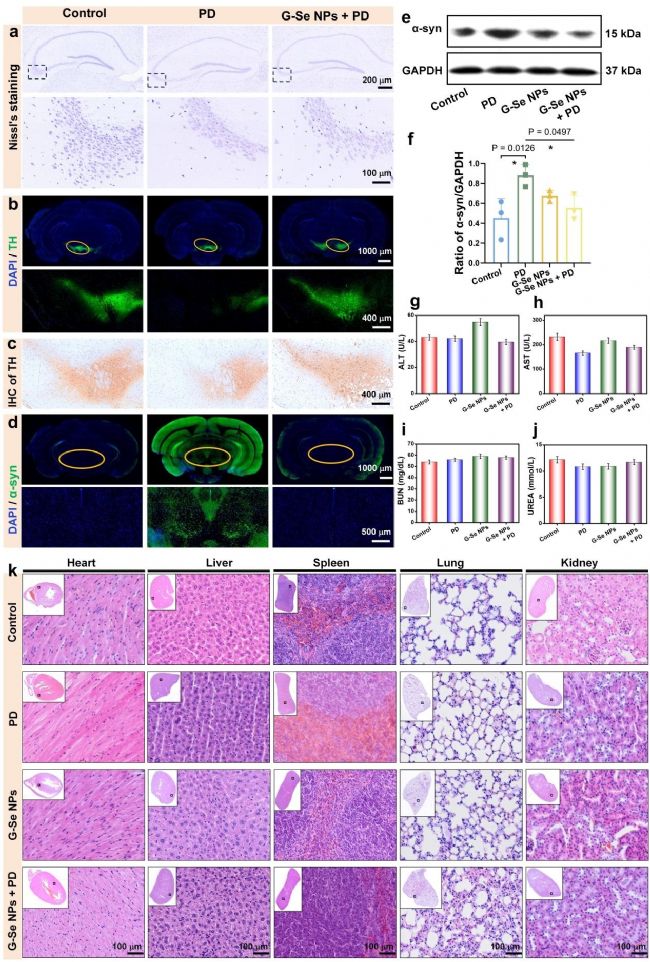
图6: G-Se NPs 的治疗潜力与转化价值。
2.7 转录组学揭示 G-Se NPs 的核心调控通路
转录组测序结果显示,G-Se NPs 可显著调控帕金森病小鼠脑组织的基因表达谱,差异基因主要富集于神经发生、神经元分化、氧化应激、炎症反应与线粒体功能相关的生物学过程与信号通路,包括肿瘤坏死因子信号通路、白介素 17 信号通路、磷脂酰肌醇 3-激酶 / 蛋白激酶 B 信号通路、核因子 κB 信号通路等。
同时,G-Se NPs 可显著上调多种硒蛋白相关基因的表达,其中硒蛋白 P 的上调最为显著,提示硒蛋白 P 是介导 G-Se NPs 神经保护作用的关键分子。
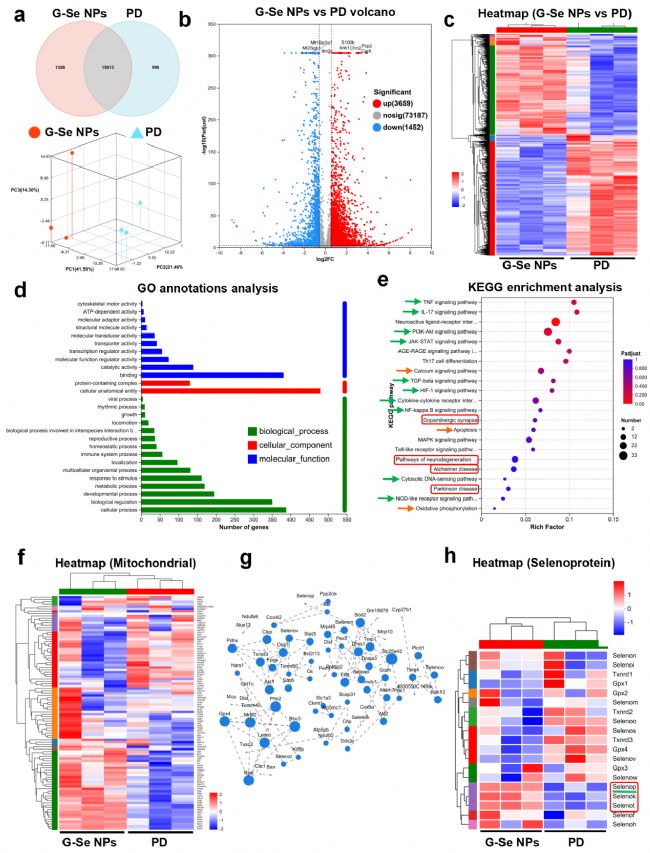
图7:G-Se NPs 的多通路协同调控机制。
2.8 G-Se NPs 通过硒蛋白 P 阻断氧化应激神经炎症循环
机制验证结果证实,G-Se NPs 不直接调控神经元内硒蛋白 P 的表达,而是通过在肝脏富集,显著促进肝脏合成与分泌硒蛋白 P。肝脏来源的硒蛋白 P 可跨越血脑屏障,将硒元素转运至脑组织,既可以直接清除活性氧,又可为脑内硒蛋白合成提供原料,激活内源性抗氧化系统。
G-Se NPs 可通过硒蛋白 P 介导的通路,显著抑制小胶质细胞与星形胶质细胞过度活化,促进小胶质细胞向抗炎表型转化,提升抗炎因子表达,降低促炎因子水平,阻断活性氧诱导的神经炎症级联反应。同时可调控线粒体凋亡相关蛋白表达,抑制神经元凋亡,维持线粒体结构与功能稳定。
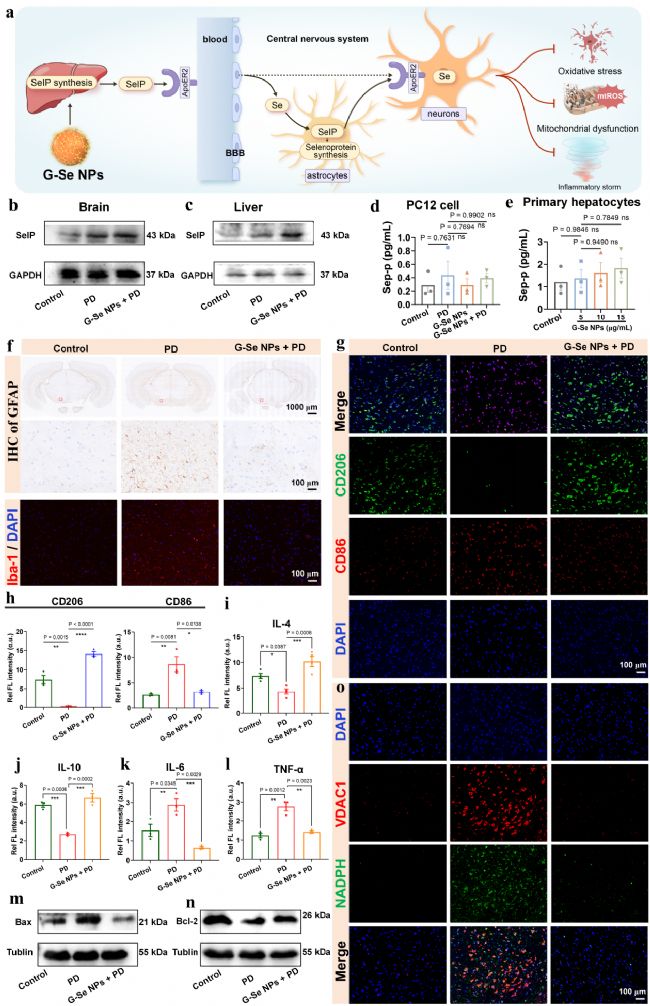
图8:阐明 G-Se NPs 外源抗氧化与内源激活协同作用的核心分子机制。
03 创新点
本研究最大创新点在于首次提出并验证外源线粒体靶向抗氧化联合内源硒蛋白 P 介导硒动员的双效协同帕金森病纳米治疗策略,突破传统单一抗氧化或单一靶向治疗的局限性,实现从症状缓解到疾病修饰的转变。
研究明确肝脏合成的硒蛋白 P 是连接外周纳米药物递送与脑内神经保护的关键枢纽,揭示“肝脏 - 硒蛋白 P - 脑” 轴在帕金森病治疗中的核心作用,完善硒元素抗神经退行性疾病的分子机制链条。同时,构建的 G-Se NPs 兼具血脑屏障穿透、黑质区富集、线粒体靶向、响应性释硒与高生物安全性多重优势,以极低剂量即可实现显著的神经保护与病理逆转效果,为神经退行性疾病纳米药物设计提供全新思路与可借鉴范式。
04 启发
在中枢神经系统疾病药物研发中,靶向细胞器与激活全身调控通路相结合的策略,优于单一靶点干预模式,可同时阻断多环节病理损伤,提升治疗效果。以人体必需微量元素为核心构建纳米药物,可显著降低免疫原性与急性毒性,提高生物安全性,降低临床转化门槛。
肝脏作为重要的分泌与代谢器官,可通过合成功能性转运蛋白远程调控脑部微环境,为中枢疾病提供外周干预新途径,拓展脑部疾病治疗的靶器官选择。纳米药物研究应兼顾递送效率与机制深度,结合多组学技术明确分子调控网络,避免仅聚焦材料性能而忽视病理机制的短板。
帕金森病治疗应聚焦早期病理循环阻断,以线粒体保护、氧化应激抑制、神经炎症消退为核心方向,而非单纯补充神经递质,更符合疾病修饰治疗的发展趋势。本研究的双效协同设计思路,可推广应用于阿尔茨海默病、肌萎缩侧索硬化等其他氧化应激相关神经退行性疾病,具有广泛的借鉴意义。
参考文献:
Lei, L., Song, L., Ao, Q. et al. Dual-action selenium nanodrugs confer synergistic protection against Parkinson’s Disease via mitochondrial-targeted antioxidant therapy and selenoprotein p-mediated selenium mobilization. Adv Compos Hybrid Mater (2026). https://doi.org/10.1007/s42114-026-01809-4
团队介绍:
张春林团队(贵州医科大学)长期聚焦神经退行性疾病发病机制与纳米药物研发,围绕帕金森病氧化应激、线粒体损伤及 α‑突触核蛋白聚集开展系统性研究,构建多种脑靶向纳米递送系统,成果发表于材料与药学领域权威期刊。
汤磊团队(贵州医科大学)专注化学创新药与天然功效成分研究,主持国家级与省部级项目,聚焦药物分子设计、合成及成果转化,搭建药物研发与成果转化平台,推动纳米药物与神经保护药物的临床前研究。
于海军团队(中科院上海药物所)主攻智能纳米递药系统与靶向递送,围绕跨屏障给药、细胞器靶向与响应性释药开展研究,为纳米药物的设计、安全性与转化提供关键技术支撑
厚谱实验室(脑体互作研究—神经药效评价实验室)专注于脑体互作机制解析与神经药效精准评价的尖端实验技术高地。可以开展清醒动物小分子取样分析、神经递质代谢产物实时分析、癫痫睡眠脑电采集分析、在体电生理记录分析、脑机接口方案评价(大动物脑部手术)、神经调控、组织透明化、脊髓损伤康复验证实验电生理(SEP)、脑立体定位给药、自动无接触采血分析、葡萄糖钳夹实验、行为学迷宫实验和动物造模等各种动物实验服务!
-END-


想了解更多内容,获取相关咨询请联系
电 话:+86-0731-84428665
伍经理:+86-180 7516 6076
工程师:+86-180 7311 8029
邮 箱:consentcs@163.com


