Akk菌驱动肠-膀胱共病新机制的研究
2026-05-11 来源:本站 点击次数:110
2026年5月8日,南方医科大学吴芃、程必盛、赵洁团队在Experimental & Molecular Medicine在线发表研究论文“Akkermansia muciniphila drives viscero-visceral crosstalk via 5-HT₃ₐR-mediated sensitization of dichotomizing gut–bladder neurons”,以 OAB–IBS 临床队列与 TNBS 诱导的炎症后小鼠模型为研究对象,系统解析了肠–膀胱轴功能共病的微生物–神经机制。该研究证实,OAB–IBS 共病伴随以 Akkermansia muciniphila 富集为核心的肠道菌群失调,这种菌群特征可通过调控宿主色氨酸代谢,促使色氨酸向血清素(5-HT)通路偏移,进而激活结肠高表达的 5-HT₃ₐ受体,使同时支配结肠与膀胱的双支背根神经节(DRG)神经元异常兴奋,最终引发内脏高敏感与膀胱功能异常。研究通过粪菌移植、神经逆行示踪、膜片钳电生理、药物干预与手术阻断等手段,完整构建了“Akk 菌 — 色氨酸代谢 — 5-HT₃ₐ受体 — 共用DRG致敏 — 肠 — 膀胱共病”的调控通路,证实该过程为非感染、非炎症扩散的神经交叉致敏模式,并明确肠道特异性 5-HT₃ₐ受体是可药物干预的关键靶点。该研究不仅揭示了 OAB–IBS 共病的全新机制,也为理解 Akk 菌的情境依赖性功能、开发靶向肠–膀胱轴的功能性疾病治疗策略提供了重要理论与实验依据。
01 研究方法
1.1 临床样本收集与评估
研究纳入 OAB–IBS 共病患者与健康对照人群,对所有受试者进行标准化症状评分,全面评估膀胱症状、肠道症状与内脏敏感性水平。严格按照纳入与排除标准筛选受试者,排除感染、手术史、妊娠等干扰因素,保证样本的同质性。收集受试者的粪便与尿液样本,低温保存用于后续微生物与分子检测,所有研究流程均通过伦理审批并获得受试者知情同意。
1.2 动物模型构建与分组
选用雌性 C57BL/6J 小鼠作为实验动物,在标准化环境下饲养。采用 TNBS 直肠灌注构建结肠炎后模型,模拟肠道慢性敏感状态,对照组仅给予溶剂处理。将小鼠随机分为正常对照组、TNBS 模型组、Akk 菌移植组、患者粪菌移植组、药物干预组与手术干预组,各组在相同环境下饲养并同步进行检测。
1.3 肠道菌群分析
对临床样本与小鼠粪便样本进行 16S rDNA 测序,分析菌群的 α 多样性与 β 多样性,筛选差异表达的菌群。采用种特异性 qPCR 对 Akkermansia muciniphila 进行定量检测,验证其在共病状态下的丰度变化。同时检测尿液样本中的 Akk 菌含量,排除泌尿系统直接定植的可能性。
1.4 神经解剖与电生理检测
通过逆行神经示踪技术,分别向结肠与膀胱壁注射荧光示踪剂,定位并观察同时支配两个器官的双支背根神经节(DRG)神经元。分离小鼠 L6–S1 段 DRG 神经元进行原代培养,采用全细胞膜片钳技术检测神经元兴奋性,记录动作电位发放频率、阈强度等电生理指标。通过免疫荧光染色观察神经激活标志物与受体的表达与定位。
1.5 代谢与分子生物学检测
采用靶向代谢组学分析肠道代谢物变化,重点关注色氨酸代谢通路。通过 ELISA、qPCR 与 Western blot 等技术,检测色氨酸、犬尿氨酸、5-羟色胺(5-HT)及其代谢产物的含量,以及 5HT 合成关键酶、转运蛋白、降解酶与多种 5HT 受体的表达水平,明确代谢与分子调控变化。
1.6 器官功能与敏感性评估
采用尿流动力学检测、排尿斑点实验评估小鼠膀胱功能,判断是否出现膀胱过度活动表型。通过结肠扩张刺激下的腹壁肌电记录与腹壁撤退反射评分,评估小鼠内脏敏感性;采用 Von Frey 测试检测躯体机械痛阈,全面反映内脏与躯体的敏感状态。
1.7 干预实验
在模型小鼠上开展两种干预方式,一是通过肠系膜动脉注射 5-HT₃ₐ受体拮抗剂昂丹司琼,特异性阻断肠道 5-HT₃ₐ受体;二是通过外科手术切断结肠肠系膜神经,阻断肠道传入信号。干预后重复检测功能、敏感性、分子与神经指标,验证通路的必要性。
02 研究内容
2.1 肠–膀胱共病模型的建立与表型验证
研究首先通过 TNBS 诱导成功构建了稳定的肠–膀胱共病小鼠模型。模型小鼠在急性期出现体重下降、肠道炎症评分升高等表现,随后进入慢性敏感状态,结肠长度显著缩短,肠道呈现持续性低度炎症。在功能层面,模型小鼠表现出明显的内脏高敏感,对结肠扩张刺激的反应显著增强,同时耻骨上区域躯体机械痛阈降低。膀胱功能检测结果显示,模型小鼠排尿频率显著增加,尿流动力学检测提示排尿收缩与非排尿收缩频率升高,排尿阈值压力降低,呈现典型的膀胱过度活动表型。同时,模型小鼠膀胱组织无明显病理损伤与炎症因子升高,说明膀胱功能异常并非局部炎症导致,而是由肠道信号介导的功能性改变,成功复制出人类 OAB–IBS 共病的核心特征。
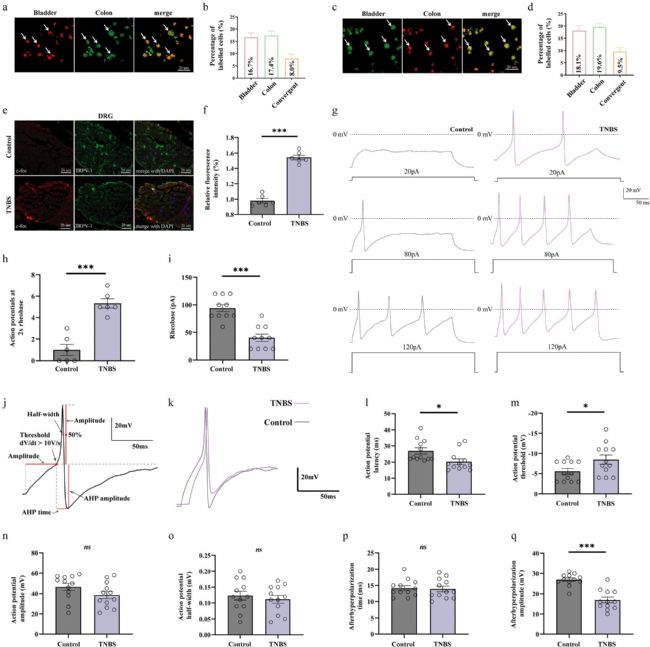
图 1: TNBS 诱导的结肠炎构建出伴随内脏高敏感与膀胱过度活动症的肠–膀胱共病小鼠模型
2.2 肠–膀胱共用神经通路的解剖证实
为明确肠–膀胱交叉对话的解剖基础,研究采用双逆行示踪技术,分别标记支配结肠与膀胱的感觉神经。结果在腰骶段 DRG 中观察到大量被双重标记的神经元,证实存在同时支配结肠与膀胱的双支感觉神经元,这类神经元构成了肠道信号向膀胱传递的直接解剖通路。进一步检测发现,模型小鼠 DRG 中神经元激活标志物表达显著升高,且主要分布在伤害性感觉神经元上。膜片钳电生理结果显示,模型小鼠 DRG 神经元兴奋性明显增强,动作电位发放频率增加、阈强度降低,动作电位相关参数呈现典型的致敏特征,说明肠道炎症后,共用 DRG 神经元处于过度兴奋状态,为肠–膀胱交叉致敏提供了细胞与神经基础。
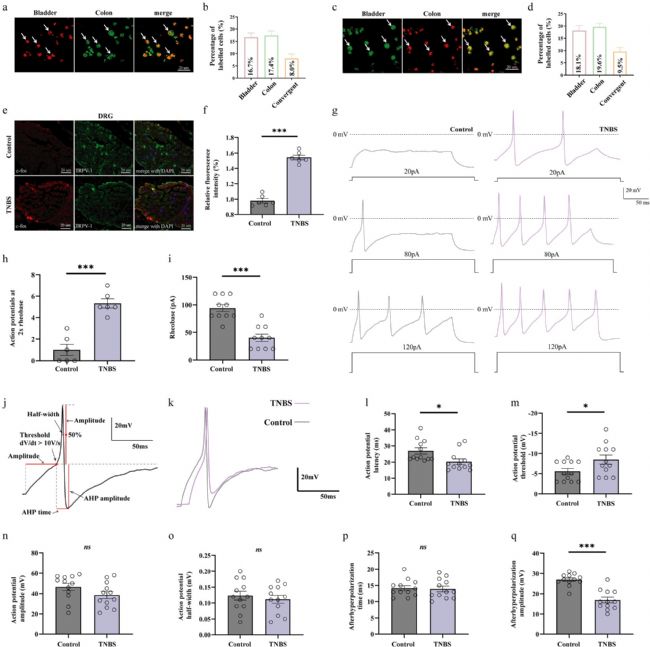
图 2:结肠炎症增强同时支配结肠与膀胱的腰骶段背根神经节(DRG)神经元的兴奋性
2.3 共病状态下肠道菌群特征与 Akk 菌的核心作用
对临床样本与小鼠模型的肠道菌群进行分析,结果显示 OAB–IBS 患者与模型小鼠的菌群结构均发生显著改变,菌群组成与健康对照存在明显分离。在菌群差异分析中,Akkermansia muciniphila 的丰度在共病状态下显著升高,是最具代表性的差异菌群,且其丰度与内脏高敏感、膀胱症状严重程度呈显著相关。同时,在受试者尿液与小鼠尿液中均未检测到 Akk 菌的定植,排除了该菌通过泌尿系统直接影响膀胱功能的可能性,提示 Akk 菌通过肠道内信号调控肠–膀胱轴功能,而非直接感染膀胱。
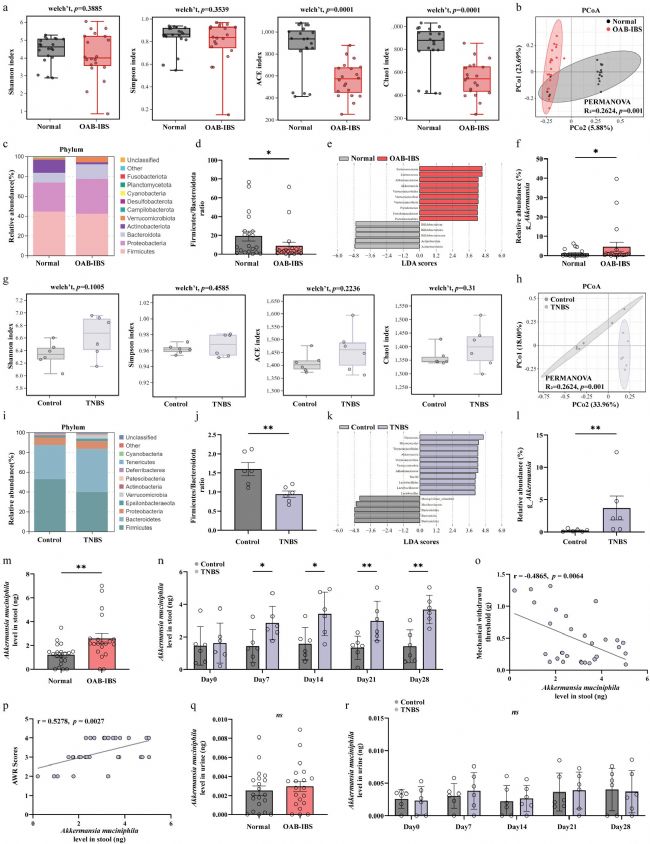
图 3:OAB–IBS 共病与 TNBS 小鼠模型均以 Akkermansia muciniphila 富集为特征的肠道菌群失调
2.4 Akk 菌与患者粪菌移植可加剧肠–膀胱功能异常
为验证 Akk 菌的因果作用,研究对小鼠进行肠道菌群清除后,分别移植 Akk 菌或 OAB–IBS 患者粪菌。结果显示,与单纯模型组相比,Akk 菌移植与患者粪菌移植均未加重肠道结构损伤,反而在一定程度上促进肠道炎症的组织学修复,但显著加剧了内脏高敏感与膀胱过度活动表型,使小鼠内脏敏感性进一步升高,膀胱排尿频率与收缩频率进一步增加。同时,移植后小鼠 DRG 神经元兴奋性进一步增强,激活标志物表达更高,说明 Akk 菌与共病相关菌群并非通过加重炎症发挥作用,而是通过调控神经兴奋性,独立驱动肠–膀胱功能异常。
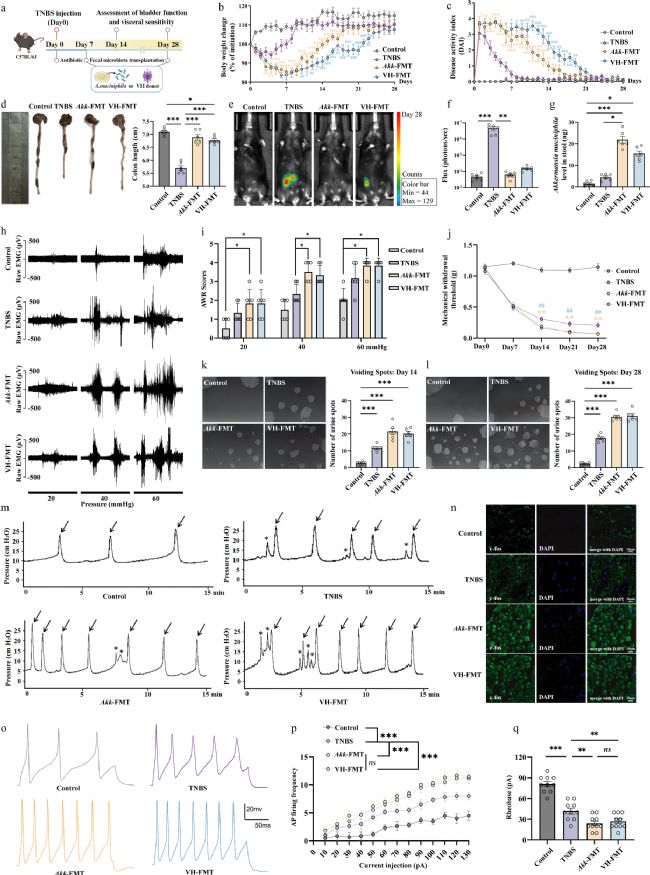
图 4:移植 Akk 菌或 OAB–IBS 患者粪菌通过促进 DRG 神经元高兴奋性加剧内脏高敏感与膀胱功能异常
2.5 Akk 菌通过色氨酸代谢激活 DRG 神经元
体外实验将 Akk 菌上清与原代 DRG 神经元共培养,结果显示 Akk 菌上清可显著激活 DRG 神经元,使神经元激活标志物表达升高,并促进神经营养因子与神经肽的分泌,且该效应呈剂量依赖性。靶向代谢组学分析显示,Akk 菌上清中色氨酸代谢通路发生显著改变,色氨酸含量明显富集,提示色氨酸是 Akk 菌调控神经元功能的关键代谢物。该结果证实 Akk 菌可通过代谢产物直接作用于感觉神经元,为后续体内代谢通路研究提供依据。
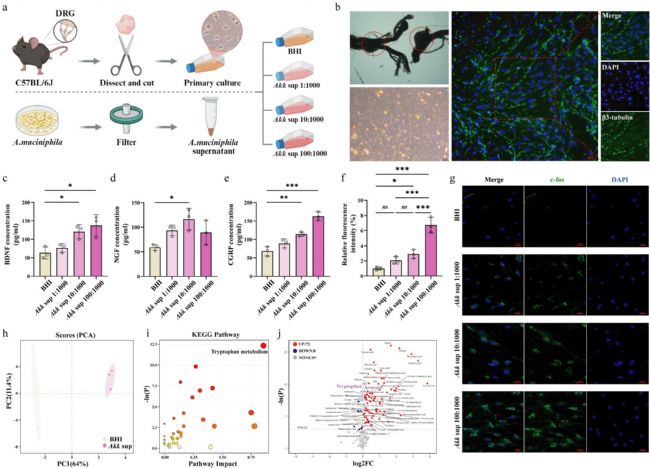
图 5:富含色氨酸代谢物的 Akk 菌上清直接诱导原代 DRG 神经元激活与致敏状态
2.6 Akk 菌重塑色氨酸代谢并上调肠道 5HT₃ₐ受体
体内代谢检测结果显示,Akk 菌移植与患者粪菌移植使宿主色氨酸代谢发生偏移,色氨酸含量升高,犬尿氨酸通路无明显变化,而 5-HT 合成通路显著激活,肠道 5-HT 水平明显升高,5HT 代谢转化率降低。分子检测显示,肠道 5-HT 合成限速酶表达上调,转运蛋白与降解酶表达下调,共同导致肠道 5-HT 累积。在多种 5-HT 受体中,仅 5-HT₃ₐ受体在肠道组织中特异性高表达,且该受体定位于支配结肠的感觉神经纤维上,说明 5-HT 通过结合肠道感觉神经上的 5-HT₃ₐ受体传递信号,而非作用于肠道局部上皮细胞。
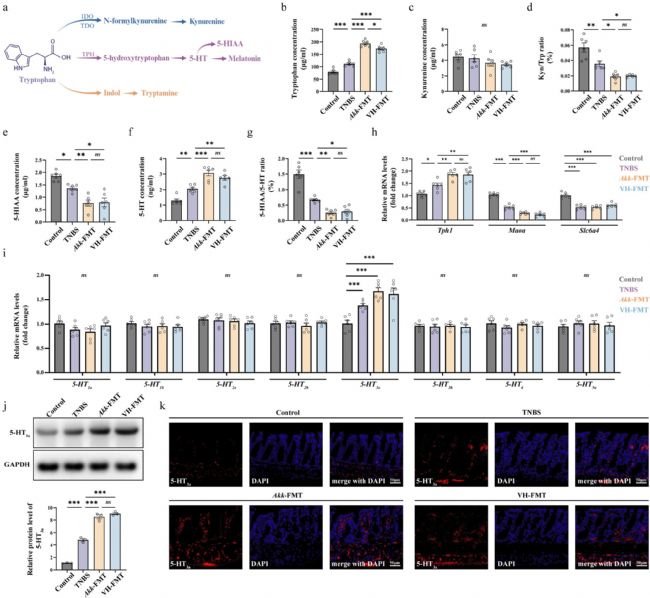
图 6:Akk 菌与 OAB–IBS 菌群使肠道色氨酸代谢向血清素(5HT)通路偏移并上调 5HT₃ₐ 受体
2.7 阻断 5HT₃ₐ受体或切断肠系膜神经可逆转共病表型
为验证通路的必要性,研究对模型小鼠进行药物与手术干预。肠系膜动脉注射 5-HT₃ₐ受体拮抗剂昂丹司琼,或手术切断肠系膜传入神经,均不会改变小鼠肠道炎症程度与结肠损伤情况,但可显著缓解内脏高敏感,降低小鼠对结肠扩张的反应,恢复躯体机械痛阈。同时,两种干预方式均可显著改善膀胱过度活动表型,使排尿频率、膀胱收缩频率恢复至接近正常水平。神经电生理检测显示,干预后 DRG 神经元兴奋性显著降低,动作电位发放频率与阈强度恢复正常,证实肠道来源的 5HT-5-HT₃ₐ受体信号经肠系膜传入神经传递至 DRG,是介导肠–膀胱共病的必需通路。
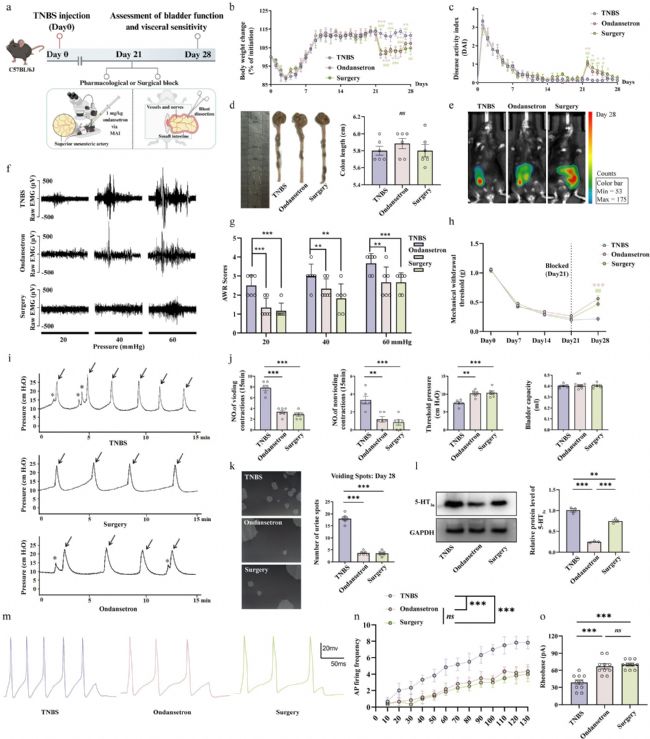
图 7:肠道特异性 5HT₃ₐ 受体阻断或肠系膜神经切断术可改善 TNBS 诱导的内脏高敏感与膀胱功能异常
2.8 5-HT₃ₐ受体特异性介导 Akk 菌诱导的肠–膀胱功能异常
在 Akk 菌移植小鼠中进一步使用昂丹司琼干预,结果显示阻断 5-HT₃ₐ受体可完全逆转 Akk 菌加剧的内脏高敏感与膀胱过度活动表型,使膀胱功能、内脏敏感性恢复正常。分子检测显示,干预后肠道 5-HT₃ₐ受体表达回落,DRG 神经元兴奋性恢复至正常水平。该结果直接证实,Akk 菌对肠–膀胱轴的调控作用完全依赖于 5-HT₃ₐ受体介导的信号通路,明确了 Akk 菌与 5-HT₃ₐ受体之间的直接因果关系。
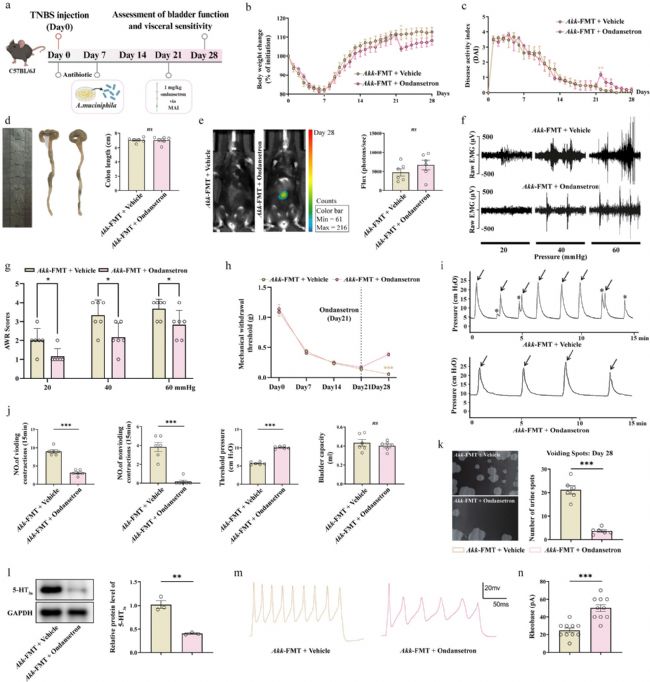
图 8:5HT₃ₐ 受体阻断特异性逆转 Akk 菌驱动的肠–膀胱功能异常加剧
03 创新点
本研究首次完整构建并验证了肠–膀胱轴的微生物–代谢–神经完整因果通路,从特定肠道菌群、关键代谢通路、特异性受体、共用感觉神经元到跨器官功能异常,形成闭环式机制,清晰解析了 OAB–IBS 共病的核心调控路径。研究颠覆了 Akkermansia muciniphila 作为绝对有益菌的传统认知,证实该菌在特定病理微环境下具有情境致病性,可驱动内脏高敏感与跨器官功能异常,拓展了肠道菌群功能多样性的认知。研究明确了肠道特异性 5HT₃ₐ受体是介导肠–膀胱交叉致敏的关键可药物干预靶点,证实膀胱功能异常可通过调控肠道信号实现逆转,提出“治肠而愈膀胱”的全新治疗策略。第四,研究证实 OAB–IBS 共病是神经交叉致敏的结果,而非炎症扩散或直接感染所致,完善了肠–膀胱轴的理论体系,为功能性盆腔器官共病研究提供了新范式。
04 启发
在基础研究层面,盆腔多器官共病的机制解析应优先关注共用感觉神经通路与肠道微生物的调控作用,微生物的功能具有高度情境依赖性,不能简单以益生菌或致病菌进行二元划分,需结合具体疾病与微环境综合判断。在机制研究思路上,跨器官功能性疾病的研究应注重上游调控轴的探索,而非仅聚焦于病变器官本身,微生物–代谢–神经轴是解析这类疾病的重要方向。在临床转化层面,OAB 与 IBS 的诊疗应重视器官关联性,对单一症状患者应评估另一器官功能,可将肠道菌群特征与色氨酸5HT 通路作为共病筛查与风险预测的指标。在治疗开发上,5-HT₃ₐ受体拮抗剂具备用于 OAB–IBS 共病治疗的潜力,靶向肠道菌群、调控色氨酸代谢、阻断肠道传入信号,可为临床难治性共病提供全新的非传统干预策略。
参考文献:
Sun, Q., Gao, Y., Zheng, J. et al. Akkermansia muciniphila drives viscero-visceral crosstalk via 5-HT3aR-mediated sensitization of dichotomizing gut–bladder neurons. Exp Mol Med (2026). https://doi.org/10.1038/s12276-026-01720-4
作者介绍:
吴芃教授,南方医科大学南方医院泌尿外科主任、教授、博导,哈佛医学院博士后。专注于微生物组学与泌尿系统疾病的科学研究,主持国家自然科学基金4项、广东省自然科学基金、广东省科技计划项目及各类校、院级科研项目共20余项,以第一或通讯作者身份发表SCI及核心期刊论文三十余篇并获得专利多项。现担任《中国泌尿外科及男科疾病诊断治疗指南》编委,《中华泌尿外科杂志》编委,《机器人外科学杂志》青年编委,《AsianJoumnalofUrology》青年编委。担任多个国际重要学术期刊客座编辑及审稿人,如《European Urology》、《Neurourology andUrodynamics>审稿人,、客座编辑等。荣获科技期刊顶尖学术论文、广东省职工经济技术创新能手、广东省医学会泌尿外科分会金闸奖、广东省千百十人才工程培养对象等人才项目。团队聚焦肠–膀胱轴、肠道菌群与神经调控,为 OAB–IBS 共病机制与临床转化提供重要理论支撑。
研究领域:
(一)微生物组学与泌尿系统肿瘤的科学研究
1.肠道及泌尿道菌群与膀胱肿瘤的临床及基础研究
2.肠道及泌尿道菌群与前列腺癌微环境研究
3.肠道菌群与泌尿系肿瘤免疫治疗的相关研究
(二)功能泌尿外科的科学研究
1.微生物组学与泌尿道功能性疾病的临床及基础研究
2.脊髓及外周神经刺激器与膀胱功能性疾病的临床及基础研究
3.全息影像技术应用于泌尿外科手术的临床研究
厚谱实验室(脑体互作研究—神经药效评价实验室)专注于脑体互作机制解析与神经药效精准评价的尖端实验技术高地。可以开展清醒动物小分子取样分析、神经递质代谢产物实时分析、癫痫睡眠脑电采集分析、在体电生理记录分析、脑机接口方案评价(大动物脑部手术)、神经调控、组织透明化、脊髓损伤康复验证实验电生理(SEP)、脑立体定位给药、自动无接触采血分析、葡萄糖钳夹实验、行为学迷宫实验和动物造模等各种动物实验服务!
-END-


想了解更多内容,获取相关咨询请联系
电 话:+86-0731-84428665
伍经理:+86-180 7516 6076
工程师:+86-180 7311 8029
邮 箱:consentcs@163.com


