基于中医外治表型揭示ALDH3A1-雌激素信号的分子机制与转化前景
2025-10-21 来源:本站 点击次数:46慢性创面是糖尿病患者最严重的并发症之一,常伴随持续性炎症、严重感染,最终可能导致下肢截肢,其死亡率甚至与癌症相当。尽管近年来对糖尿病创面愈合障碍的理解有所加深,但皮肤修复细胞功能障碍的分子机制仍不清楚,现有治疗策略也非常有限。中医外治法因“非手术”、“瘢痕较少”等优势,在慢性创面修复领域展现出广阔的临床应用前景。
近日,上海中医药大学附属岳阳中西医结合医院、上海市皮肤病医院/同济大学附属皮肤病医院、同济大学医学院合作发表的一项研究“Polyphenol-synthesized nanoparticles with ALDH3A1 delivery ability for activating estrogen signaling for diabetic wound healing”,基于岐黄学者、全国老中医药专家学术经验继承工作指导老师、上海市名中医李斌教授经验方生肌化瘀膏的临床疗效,通过整合单细胞及其他多组学研究结果,确认ALDH3A1为一种具有愈创潜力的蛋白,阐明ALDH3A1-雌激素信号在慢性伤口愈合过程中促进角质形成细胞增殖/迁移;并针对蛋白质递送障碍的瓶颈难题,开发了一种由金属-多酚网络合成的纳米系统AL@FG,以增强糖尿病小鼠的创面愈合。
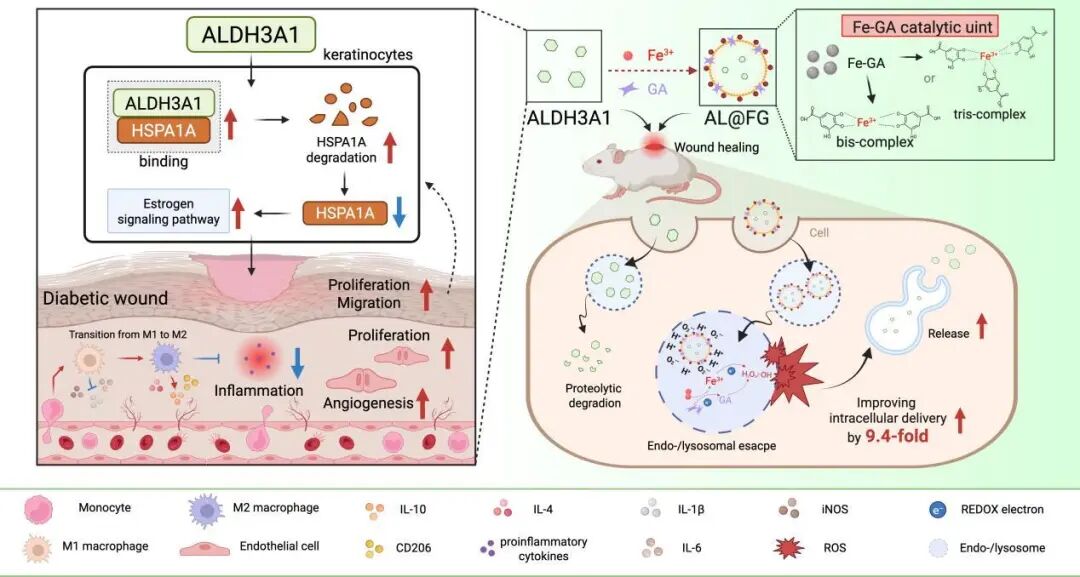
该研究中单细胞转录组学
4D蛋白组、IP-蛋白质谱实验及
分析工作由SBC提供
一、文章详情
文章题目:Polyphenol-synthesized nanoparticles with ALDH3A1 delivery ability for activating estrogen signaling for diabetic wound healing
中文题目:具有ALDH3A1递送能力的多酚合成的纳米颗粒可激活雌激素信号传导以促进糖尿病伤口愈合
发表时间:2025.9
期刊名称:Chemical Engineering Journal
研究样本:糖尿病小鼠模型、野生型小鼠、ALDH3A1基因敲除小鼠、人永生化角质形成细胞、人表皮角质形成细胞、人脐静脉内皮细胞
组学技术:单细胞转录组、蛋白组、转录组、免疫组化、免疫荧光等
二、技术路线
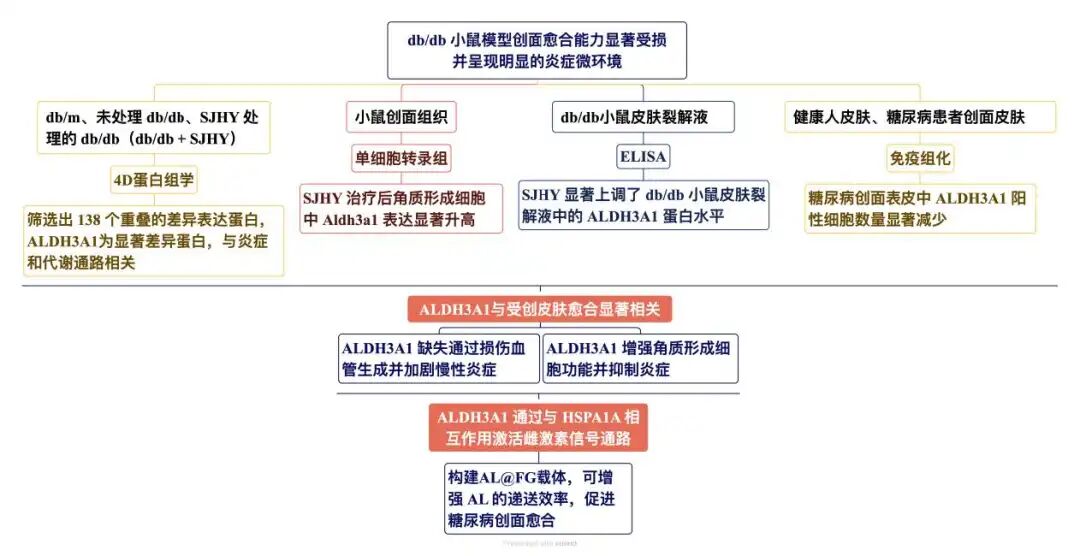
三、研究内容
1. ALDH3A1 被确定为缓解糖尿病创面炎症的潜在调控因子
与以往认知一致,2型糖尿病小鼠模型的创面愈合能力显著受损,且创面呈现明显的炎症环境。中医外治法对于慢性伤口炎症反应的改善具有一定优势,外用“生肌化瘀膏”(SJHY)可显著降低创面部位的炎症浸润(图1A)。此外,研究者对db/m、未处理 db/db、SJHY 处理的 db/db的三组小鼠伤口创面组织进行了4D非靶向蛋白质谱检测,共筛选出138个重叠的差异表达蛋白(图1B-C),KEGG富集分析提示这些蛋白与炎症和代谢通路相关,提示其为糖尿病创面潜在的抗炎靶点,其中ALDH3A1为优选的差异性蛋白(图1D)。
单细胞转录组测序结果显示SJHY治疗后角质形成细胞中Aldh3a1表达显著升高(图1E),ELISA 结果显示SJHY亦显著上调了db/db小鼠皮肤伤口裂解液中的ALDH3A1蛋白水平(图1F)。临床免疫组化结果提示,糖尿病创面表皮中ALDH3A1阳性细胞数量显著减少(图1G-H)。
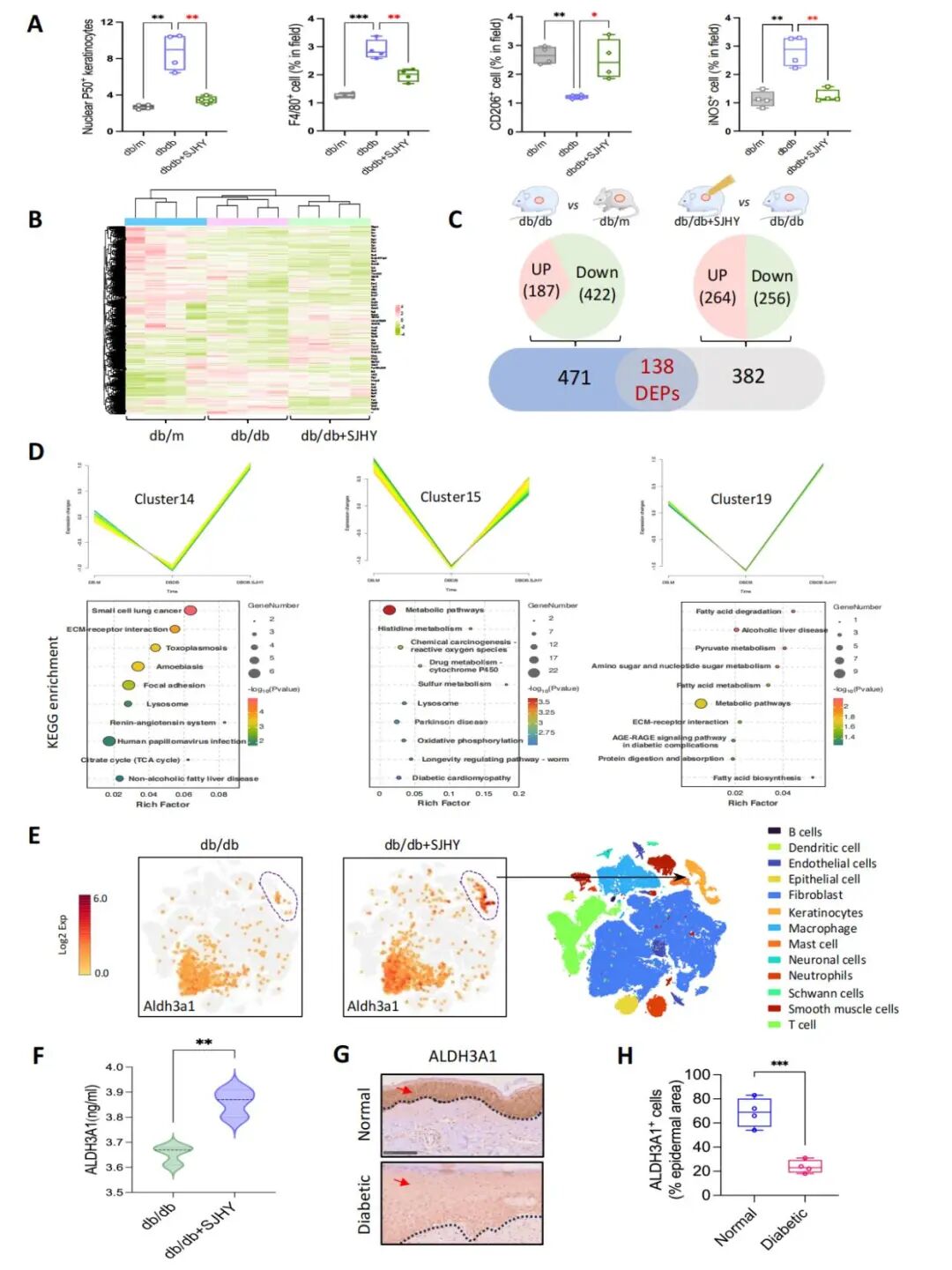 图1 ALDH3A1在糖尿病创面中表达下调
图1 ALDH3A1在糖尿病创面中表达下调2. ALDH3A1缺失通过损伤血管生成并加剧慢性炎症,恶化糖尿病创面病理进程,过表达ALDH3A1可增强角质形成细胞功能并抑制炎症,从而促进创面愈合
为了明确ALDH3A1在创面愈合中的作用,研究者构建了ALDH3A1基因敲除小鼠(图2A),ALDH3A1 KO小鼠的愈合速度显著慢于WT对照。进一步构建STZ诱导的糖尿病小鼠模型,发现与WT-STZ小鼠相比,ALDH3A1KO-STZ小鼠的创面50 %闭合时间延迟约2天(图2B-C),且初始创面闭合缓慢、不完全(图2D-E)。免疫组化结果表明,ALDH3A1KO-STZ小鼠新生血管明显减少、再上皮化明显减慢、创面炎症浸润显著,伴随M1巨噬细胞向M2型极化障碍(图2F-N)。
体外实验显示,ALDH3A1过表达可显著促进人永生化角质形成细胞系HaCaT和正常人表皮角质形成细胞NHEK的增殖(图3A-C),并显著增强了细胞的迁移能力(图3D-G)。此外,ALDH3A1过表达显著抑制了晚期糖基化终末产物(AGEs)的关键前体MGO诱导模拟糖尿病伤口环境下的炎症因子IL-6 和IL-1β的表达(图3H-I)。
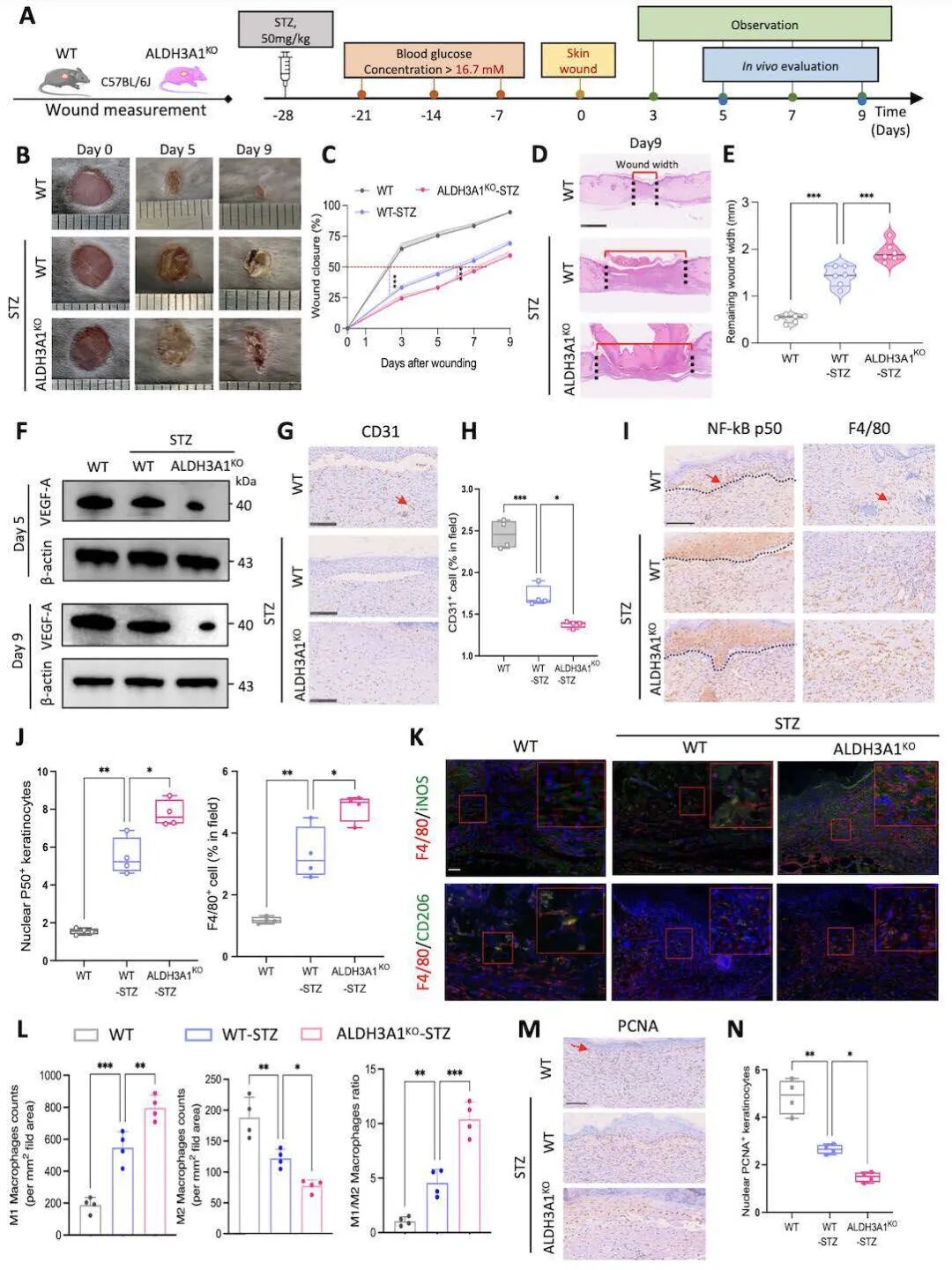
图2 ALDH3A1在糖尿病小鼠体内愈合过程中发挥积极作用
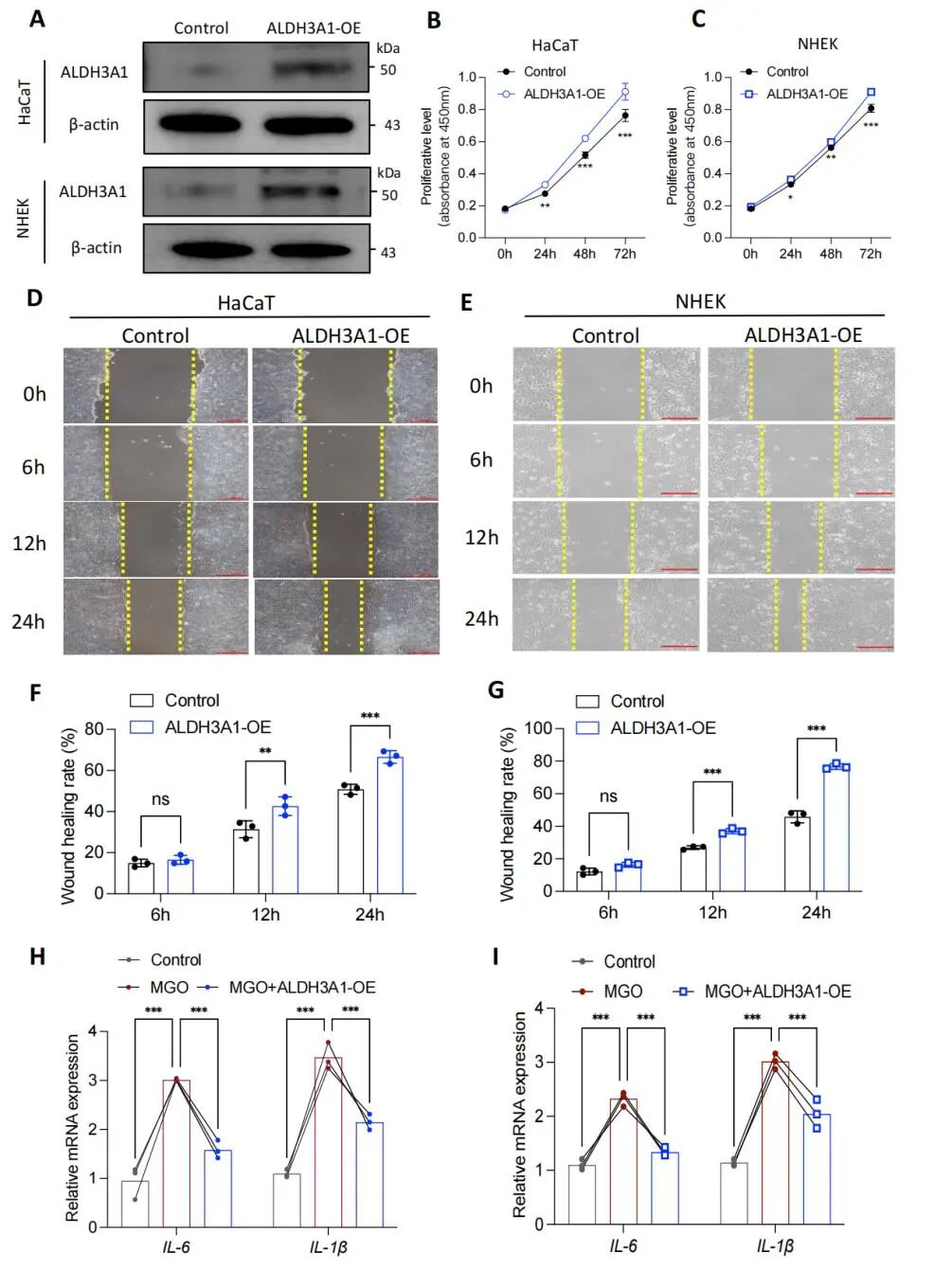 图3 ALDH3A1促进角质形成细胞功能修复
图3 ALDH3A1促进角质形成细胞功能修复3. ALDH3A1 通过与 HSPA1A 相互作用激活雌激素信号通路
对转录组数据进行GSEA分析,将ALDH3A1与雌激素信号通路关联起来(图4A-C)。进一步发现,在MGO干预HaCaT细胞诱导模拟的糖尿病伤口环境中,雌激素信号通路关键标志物CTSD和EBAG9表达下降,而ALDH3A1过表达可逆转这一趋势(图4D-E)。同样地,在糖尿病小鼠创面组织中发现雌激素受体ESR1和ESR2表达的降低,而ALDH3A1KO会加剧这一现象(图4F)。临床免疫组化显示,糖尿病患者创面组织中ESR1和ESR2阳性细胞明显减少(图4G-H)。进而使用雌激素信号抑制剂ICI 182780干预HaCaT细胞,发现抑制雌激素信号会阻碍HaCaT细胞的增殖和迁移,并增加炎症因子的表达(图4I-L)。
同时,共免疫沉淀联合质谱(Co-IP/MS)发现ALDH3A1可能与HSPA1A相互作用(图5A)。HSPA1A在细胞应激时被激活,是难愈性糖尿病创面的标志性蛋白,并与炎症反应增强相关,已证明能降低ESR2的表达和活性。Co-IP和GST-pull down证实二者的结合(图5B),免疫荧光也显示两者在HaCaT细胞质中共定位(图5C)。进一步研究发现,ALDH3A1KO可上调糖尿病小鼠创面组织中HSPA1A蛋白水平,而ALDH3A1过表达则降低MGO处理的HaCaT细胞中HSPA1A表达(图5D)。CHX追踪实验表明,ALDH3A1促进HSPA1A蛋白降解,但不影响其mRNA水平(图5E)。
在临床样本中,糖尿病创面组织中HSPA1A表达显著升高(图5F)。过表达HaCaT细胞中的HSPA1A,则会抑制HaCaT细胞的增殖和迁移,并增加炎症因子的表达(图5G-J)。挽救实验发现,HSPA1A过表达可逆转ALDH3A1过表达影响的HaCaT促增殖、迁移及抗炎作用,而雌激素信号抑制剂ICI 182780则加剧了这一效应(图5K-N)。
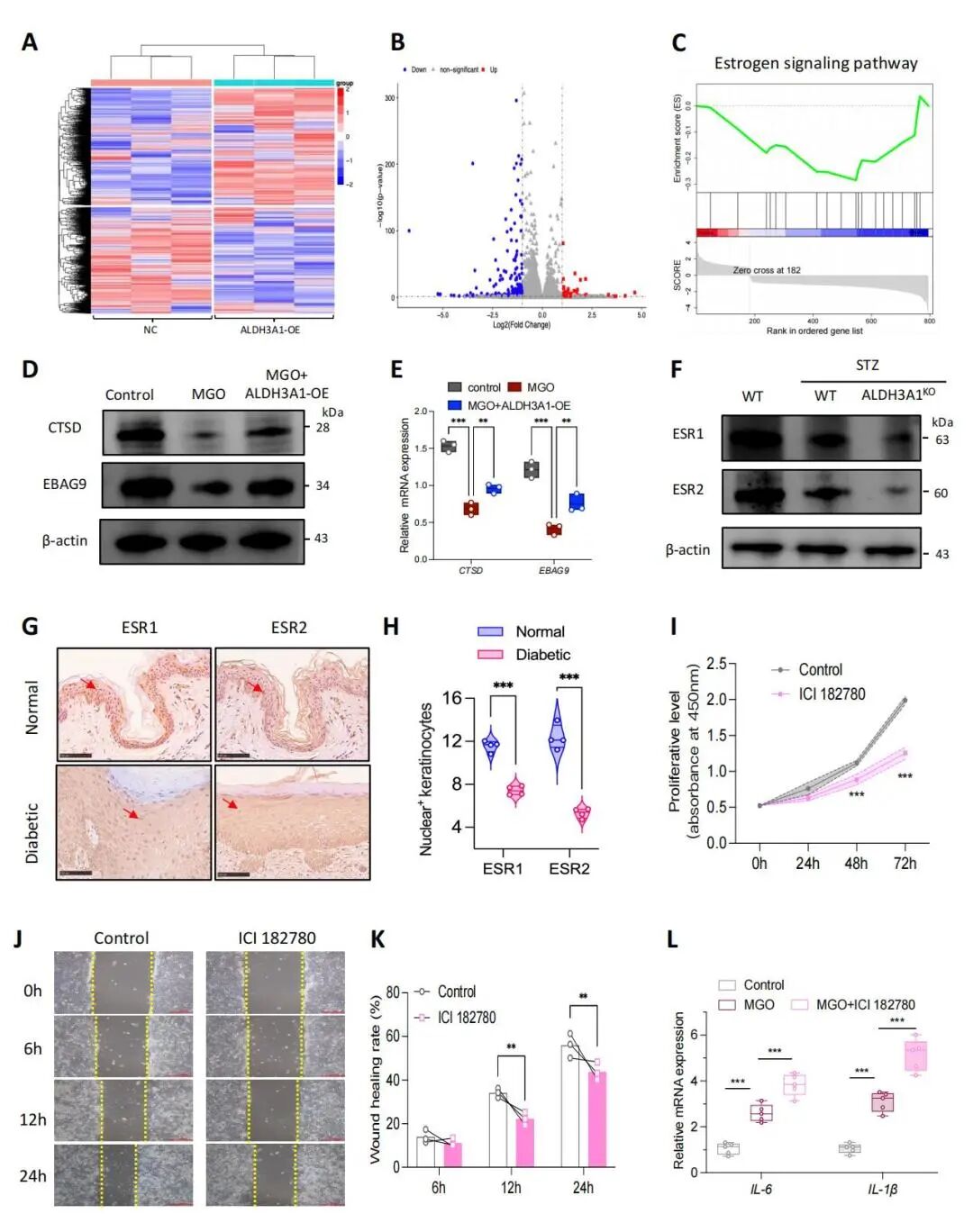
图4 ALDH3A1通过雌激素信号通路促进糖尿病伤口愈合
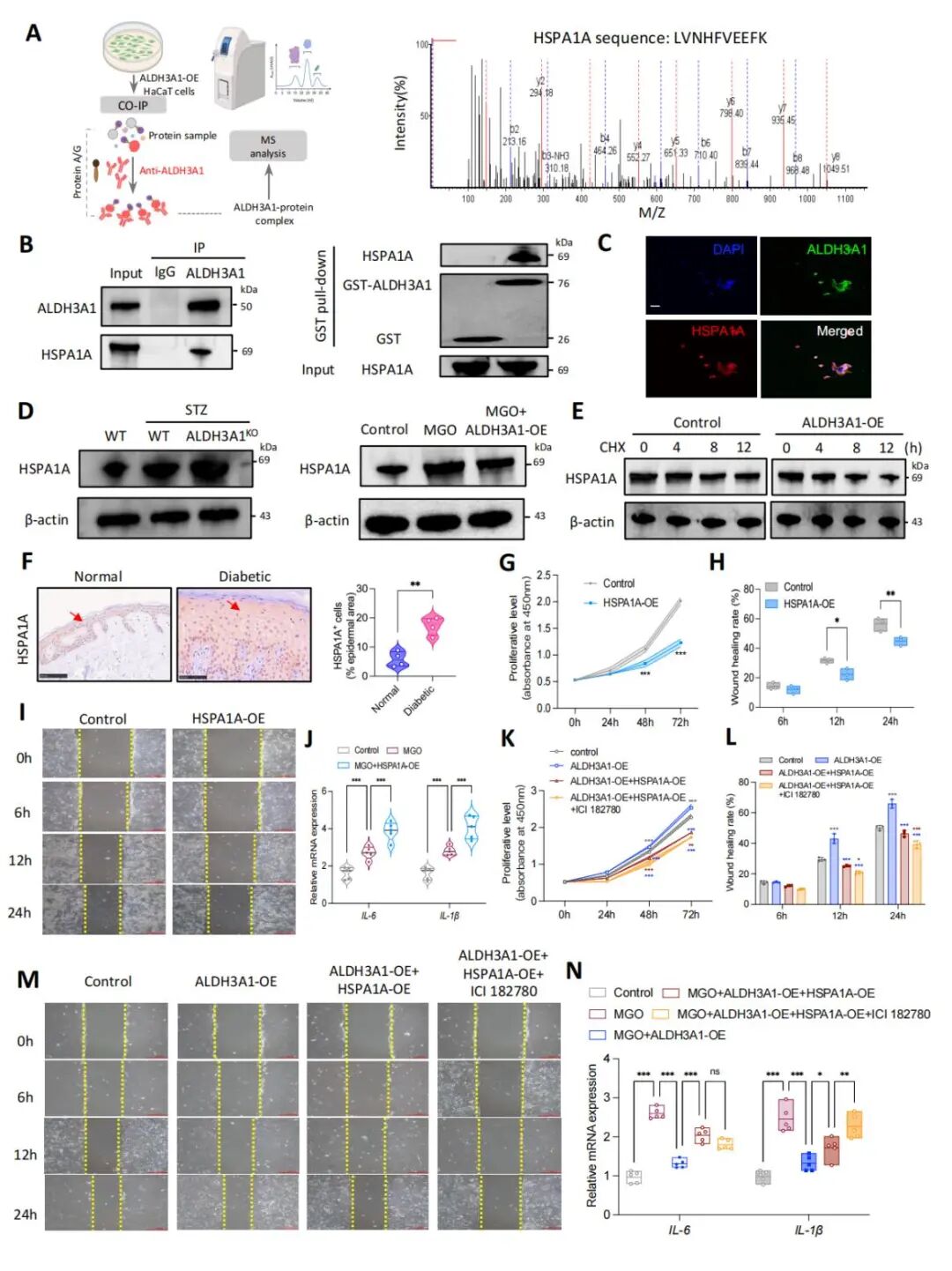 图5 ALDH3A1通过抑制HSPA1A蛋白稳定性激活雌激素信号通路
图5 ALDH3A1通过抑制HSPA1A蛋白稳定性激活雌激素信号通路4. AL@FG 构建,增强AL的递送效率,促进糖尿病创面愈合
基于上述实验结果,研究者设计了一种催化纳米递送系统AL@FG,克服溶酶体降解,可将ALDH3A1的细胞内递送效率提高9.4倍(图6)。体内外疗效实验结果表明,与单独使用AL或临床标准药物rb-bFGF相比,AL@FG对HaCaT细胞的治疗作用更显著,并可显著促进人脐静脉内皮细胞(HUVEC)增殖。并且,db/db+AL@FG组再上皮化速度最快且完整,血管新生丰富,显著优于AL和rb-bFGF组(图7)。炎症评估结果表明,AL@FG显著减少炎症细胞浸润,巨噬细胞呈现出M2型极化(图8)。
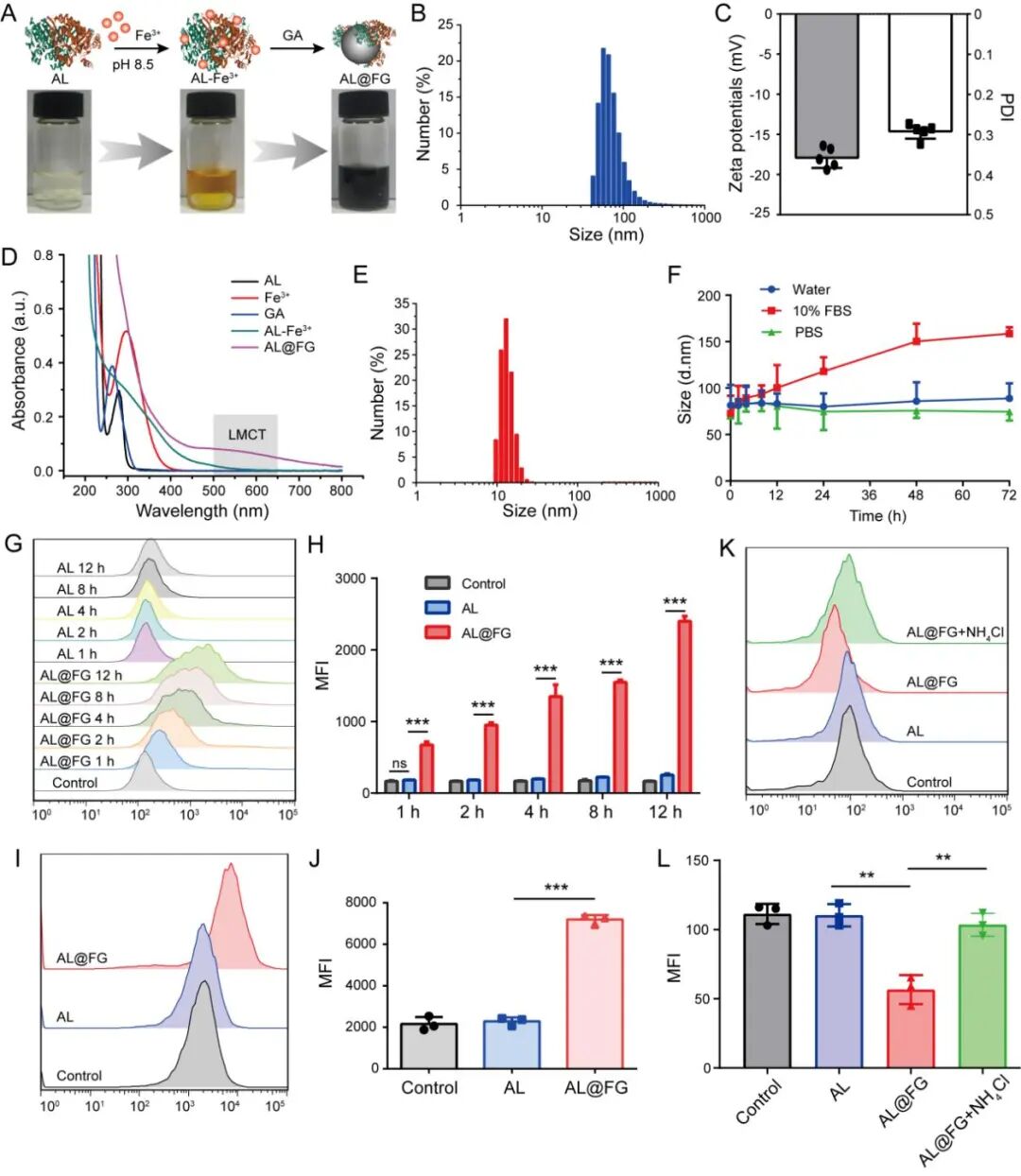
图6 AL@FG的制备与表征
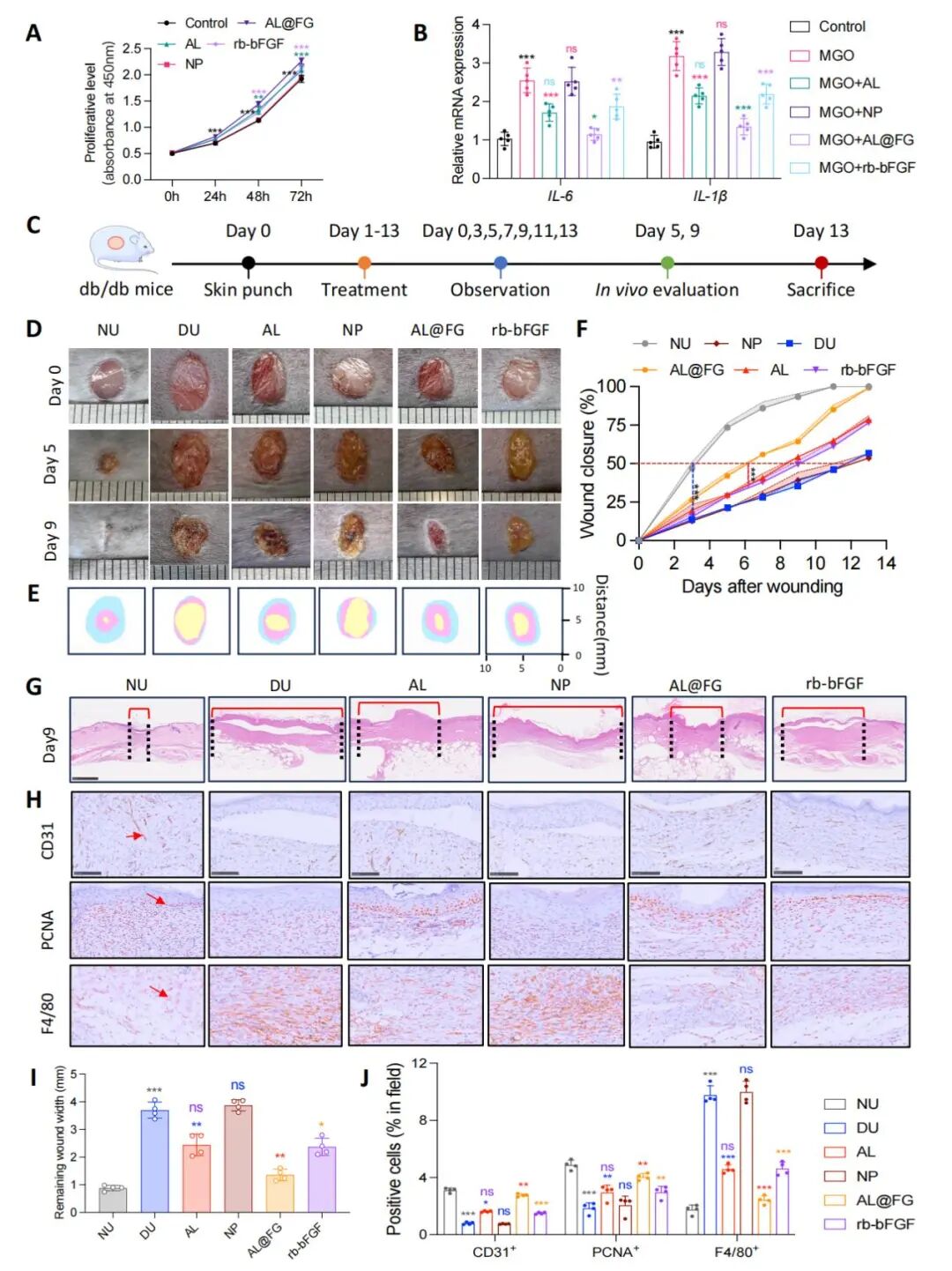 图7应用AL@FG增强了AL的治疗功效
图7应用AL@FG增强了AL的治疗功效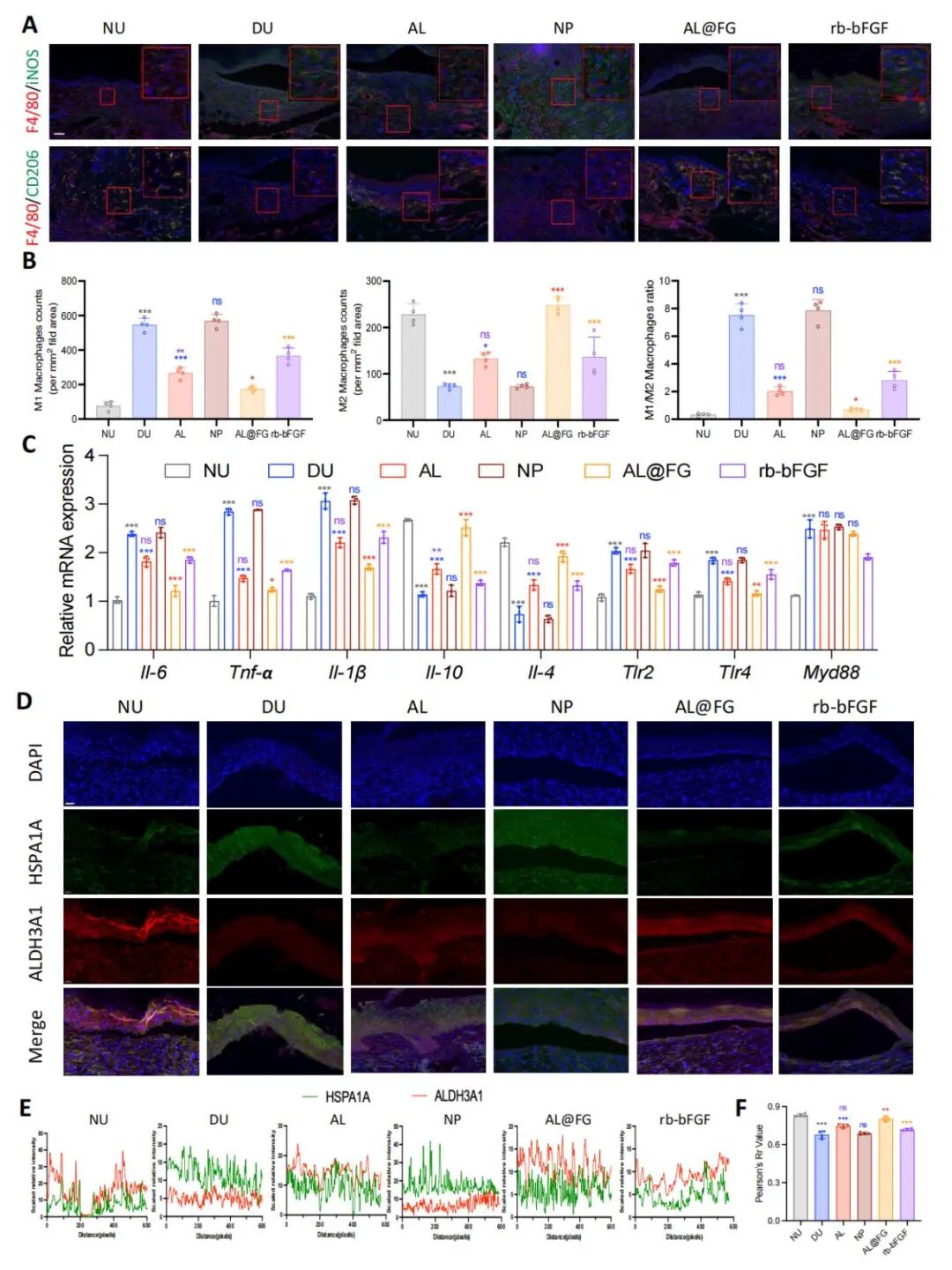 图8 应用AL@FG显著改善糖尿病伤口巨噬细胞极化障碍
图8 应用AL@FG显著改善糖尿病伤口巨噬细胞极化障碍文章总结
研究者基于中医外治法的临床优势,采取“以药钓靶”的研究策略,从已有临床疗效、实验表型的生肌化瘀膏组学数据中“垂钓”出药物作用的分子靶点。首次阐明ALDH3A1在加速糖尿病创面愈合中的关键性功能(已同步获批国家发明专利),并据此开发了一种简单、高效、具有转化价值的金属-多酚纳米递送系统AL@FG,使蛋白递送效率提高9.4倍,且在疗效上优于临床标准 rb-bFGF。为蛋白类抗炎药物在慢性创面及其他组织修复场景中的临床转化提供了可落地的技术路线。该团队“以药钓靶”的研究策略亦在其他难治性皮肤病领域发表了多篇高水平论著,为基于中医特色的基础研究开展提供了范式与参考。
相关文章
更多 >

