巨噬细胞对机械拉伸的非单调性反应会影响皮肤伤口愈合
2025-11-07 来源:本站 点击次数:749Non-monotonic response of macrophages to mechanical stretch impacts skin wound healing
Keywords: Macrophages; Mechanical stretch; Skin cells; Wound healing; YAP/TAZ.
在生理与病理状态下,皮肤持续承受机械应力作用。巨噬细胞作为皮肤稳态维持与伤口愈合的核心调控者,通过表型动态转换协调炎症、增殖及重塑三个阶段。其早期促炎表型(M1)通过释放TNF-α、IL-1β等因子清除损伤组织,后期抗炎表型(M2)则分泌IL-4、IL-13及VEGF、bFGF等生长因子,直接促进成纤维细胞迁移、角质形成细胞增殖和血管新生。这种时空特异性调控使巨噬细胞成为机械力影响伤口愈合的关键媒介。
点击了解: 牵张应变细胞培养仪
皮肤机械微环境的改变深刻影响细胞行为。尽管循环拉伸对巨噬细胞极化的研究已有报道,但皮肤伤口teyou的静态拉伸效应尚未系统阐明。现有研究表明,33%静态拉伸可诱导巨噬细胞向M2表型转化,体外实验也证实IL-4/IL-13能增强此过程。然而,不同强度静态拉伸对巨噬细胞功能的梯度效应、相关信号通路及其对皮肤细胞的旁分泌作用仍存在显著认知空白。
点击了解: 细胞力学刺激培养系统
基于此,中国科学技术大学生命科学与医学部在一项研究中,创新性地建立7%(低)、15%(中)、21%(高)三梯度静态拉伸模型,重点探究机械拉伸对巨噬细胞活力、极化及YAP/TAZ信号通路的非单调响应规律;通过条件培养基(MS-CM)解析机械力旁分泌皮肤细胞行为的级联效应;在体内外模型中验证最优拉伸强度对血管生成与真皮重建的促进作用。该工作为机械微环境调控巨噬细胞功能提供了新视角。研究成果发表于“Cellular & molecular biology letters”期刊题为“Non-monotonic response of macrophages to mechanical stretch impacts skin wound healing”。

首先,研究人员开发了定制化细胞拉伸装置,其与市售伸展底板整合后可模拟皮肤细胞的连续拉伸微环境。该设备基于真空泵、压力箱及负压控制器构建(图1A),其中压力传感器实时监测负压强度并自动调节输出参数(图1B),通过柔性六孔板底部的硅胶膜双轴形变对贴壁细胞施加均匀静态拉伸(图1C)。通过建立压力强度(30/60/90 kPa)与硅胶膜变形指数的线性回归模型(图1D),实现了15%(低)、21%(高)等特定机械拉伸(MS)强度的精准控制。该系统的可编程压力调控模块与商业底板协同工作,为研究机械应力对细胞行为的剂量效应提供了高精度实验平台,特别适用于解析不同MS强度下巨噬细胞非单调响应机制的研究需求。
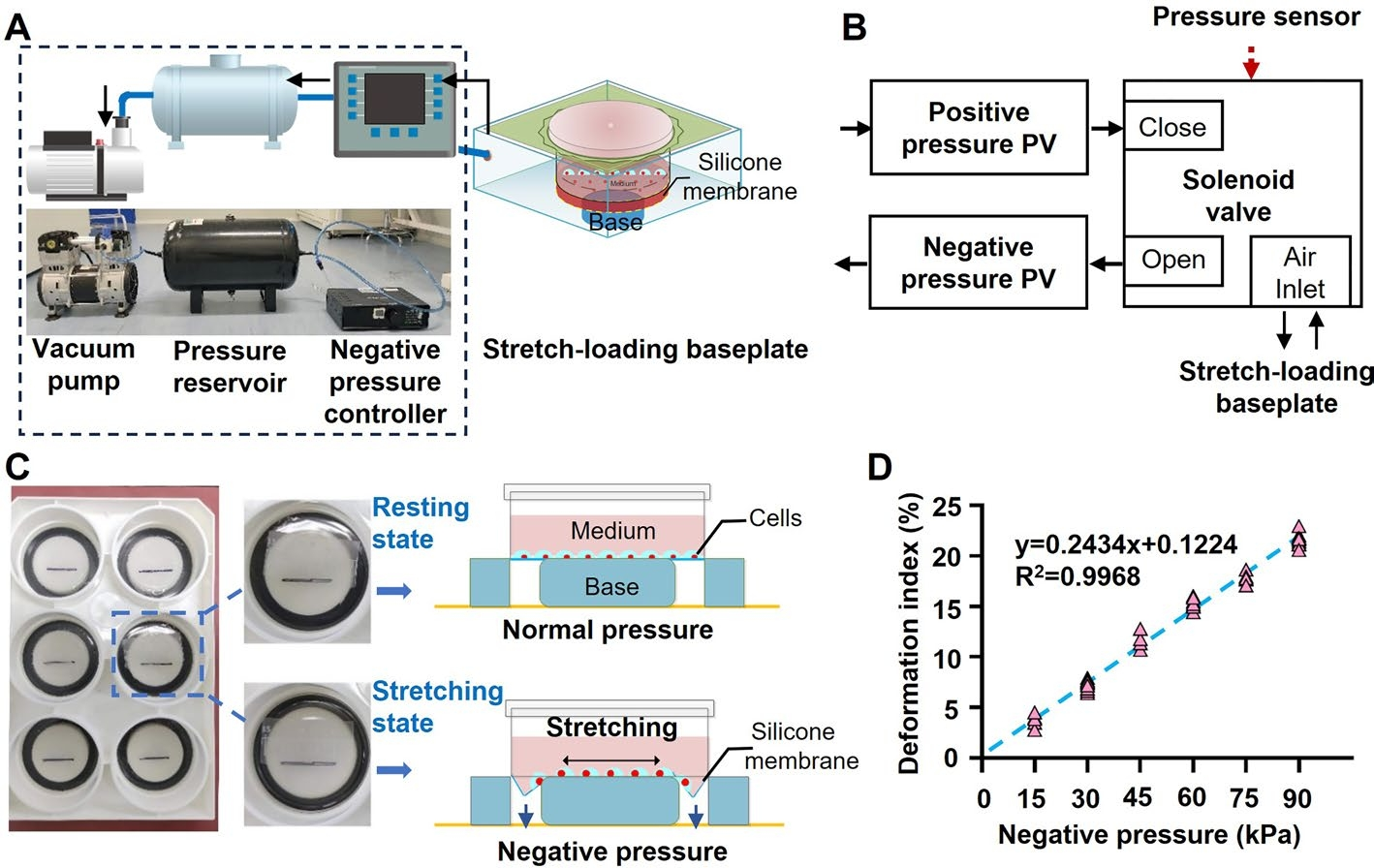
图1 细胞拉伸装置示意图。
然后,研究人员通过定制拉伸装置对THP-1分化巨噬细胞施加7%(低)、15%(中)、21%(高)静态机械拉伸(MS),发现其对细胞活力与表型呈现非单调调节(图2A)。CCK-8检测显示15% MS显著促进细胞增殖,而21% MS抑制生长,WB分析进一步证实15% MS通过降低BAX/BCL2比值抑制凋亡(图2B-D)。流式细胞术显示15% MS 最显著诱导M2极化(CD206↑/CD86↓),M2/M1比率较对照组提升1.8倍(图2E-G)。qPCR分析同步验证,15% MS组促炎因子(TNF-α、IL-1β、IL-6)显著下调,抗炎因子(IL-4、IL-10)及促愈合生长因子(bFGF、VEGFA、PDGFA等)表达达峰值,其中PDGFA上调7倍(图2H-I)。该非单调响应揭示中等强度MS(15%)通过增强M2极化与分泌组重塑,为机械微环境调控伤口愈合提供新依据。
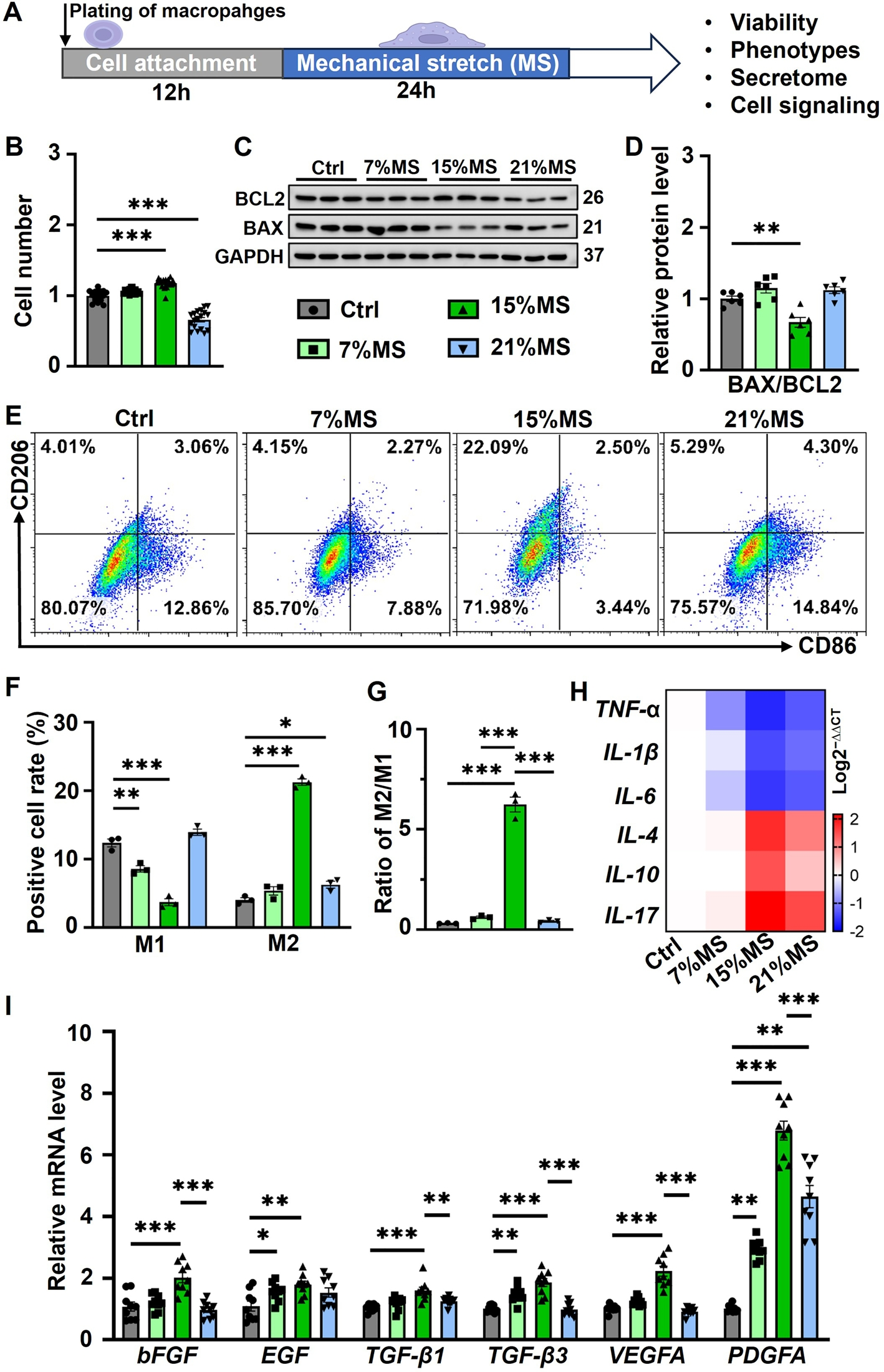
图2 不同机械拉伸强度对巨噬细胞存活与极化的影响。
接着,研究人员揭示了机械拉伸(MS)对巨噬细胞YAP/TAZ机械转导通路的非单调调控机制。通过免疫印迹及荧光染色发现,15% MS显著提升YAP/TAZ总表达量,并驱动其核定位比例达68%(图3A-E)。核质分布定量显示,7% MS引起胞内YAP/TAZ轻度累积,15% MS使核内蛋白占比提升至峰值,而21% MS虽提高胞质水平却抑制核转位(图3F-H)。下游靶基因分析表明,15% MS组血管生成因子CYR61和CTGF的mRNA及蛋白表达分别上调4.8倍和3.2倍(图3I-J),显著高于7%和21% MS组的1.5-2.3倍增幅。这种强度依赖性调控证实15% MS通过协同增强YAP/TAZ表达与核易位,最有效激活机械信号转导,为阐释巨噬细胞机械感知的阈值效应提供了分子基础。
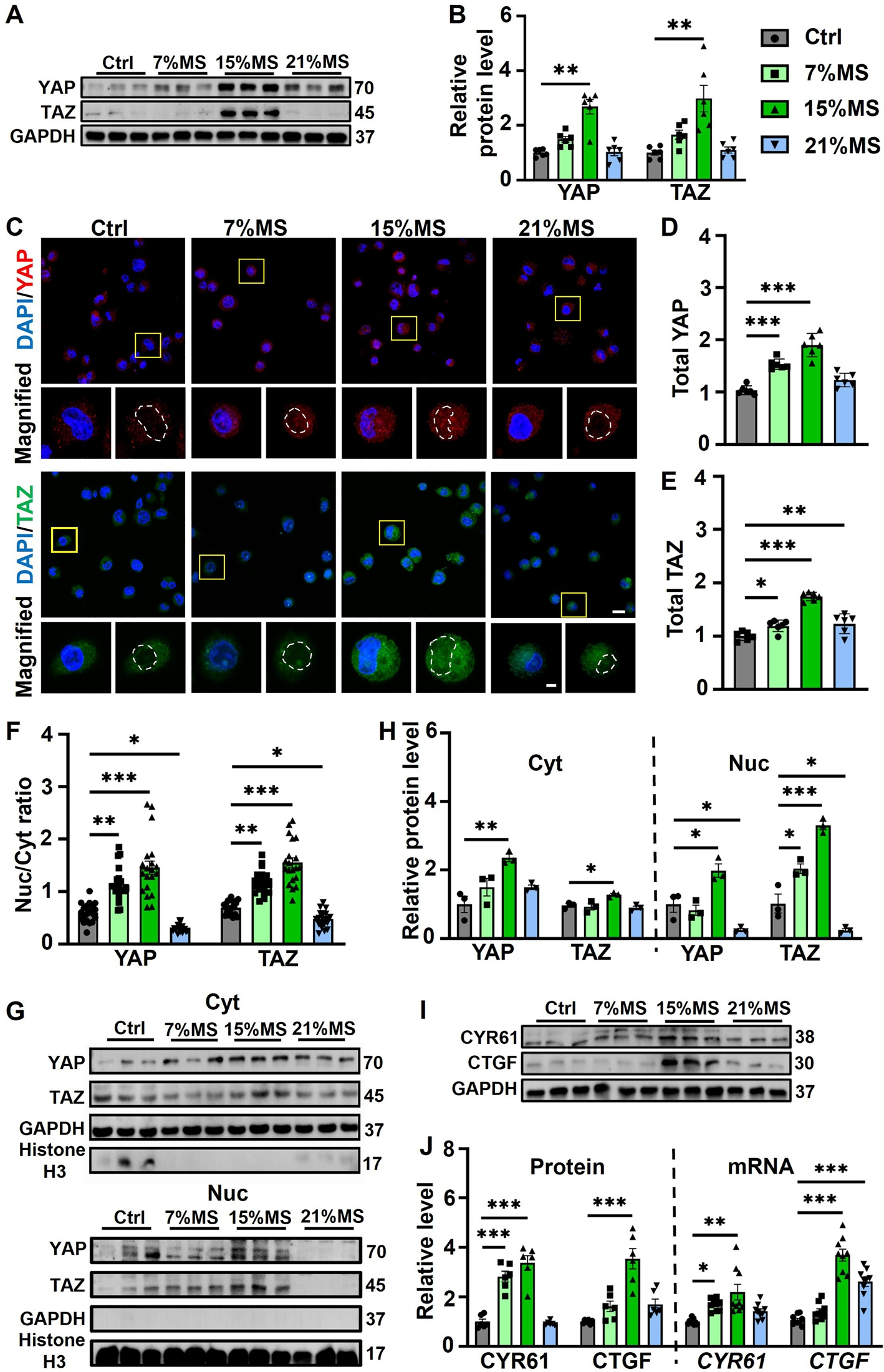
图3 暴露于不同水平机械拉伸下的巨噬细胞中YAP/TAZ通路的调控。
进一步,研究人员通过巨噬细胞条件培养基(MS-CM)解析了机械拉伸(MS)对皮肤细胞的旁分泌调控机制。15% MS处理的巨噬细胞分泌组显著促进角质形成细胞迁移(图4B-C),但对细胞活力无影响(图4A)。在内皮细胞中,15%MS-CM使细胞迁移速度提高2.3倍(图4E-F),并最显著增强体外血管生成能力(图4G-H)。成纤维细胞经15%MS-CM处理后,α-SMA和胶原I/III表达达峰值(图4I-J),表明其活化程度最高。这种强度依赖性效应揭示15%MS通过优化巨噬细胞分泌组,协同促进再上皮化、血管新生与真皮重建,为机械力免疫修复细胞调控提供依据。
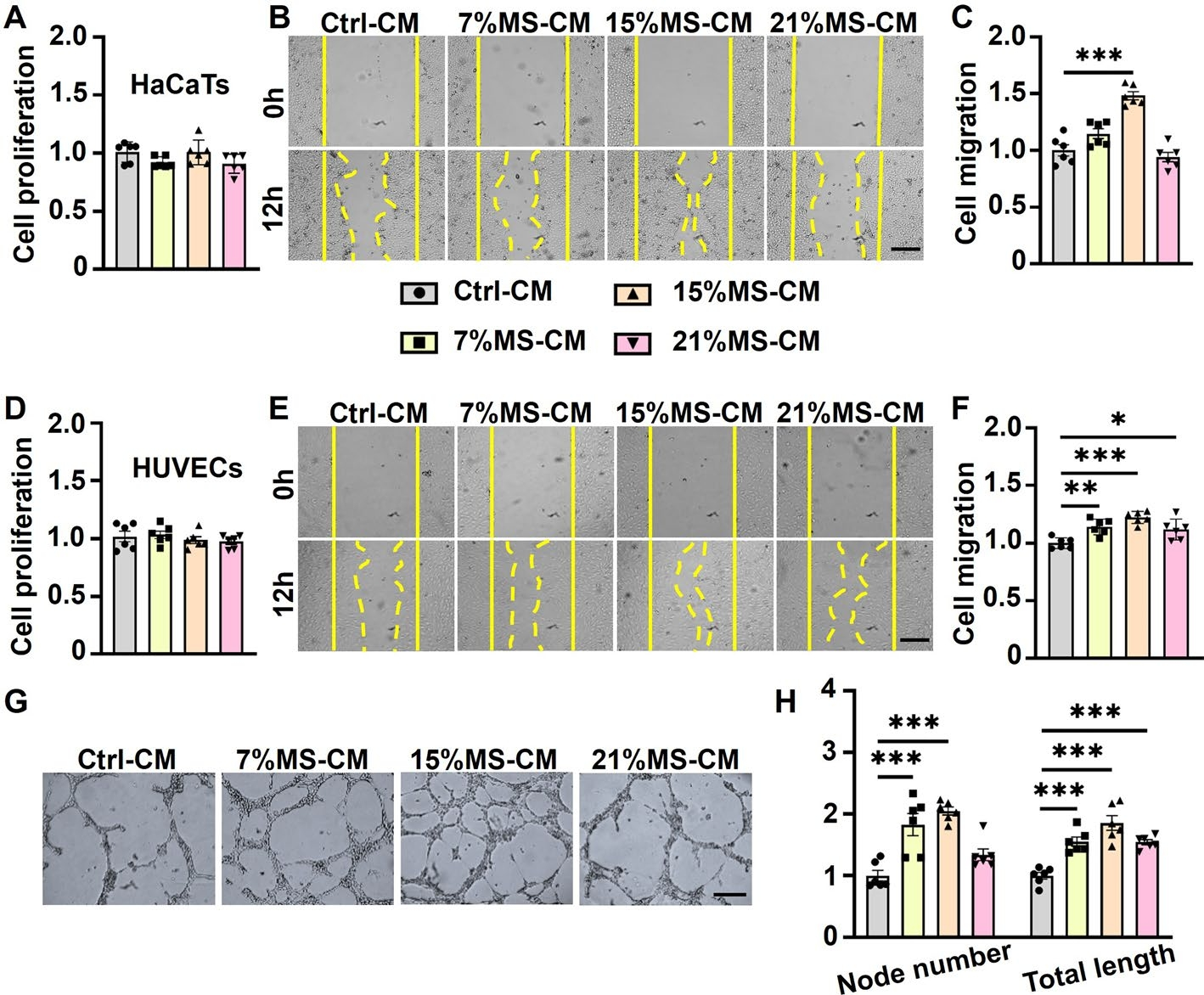
图4 不同机械拉伸条件培养基对角质形成细胞和内皮细胞的影响。
研究揭示机械拉伸处理的巨噬细胞分泌组(MS-CM)对成纤维细胞功能呈现强度依赖性调控。15% MS-CM显著促进成纤维细胞增殖(图5A)并加速迁移(图5B-C)。免疫染色与WB分析证实,15% MS-CM诱导α-SMA表达上调3.7倍,同步增强胶原I和纤连蛋白合成(图5D-G),标志成纤维细胞向促修复的肌成纤维细胞转化。相较之下,7%与21% MS-CM对上述指标的调控效应显著减弱。这种非单调响应模式与巨噬细胞旁分泌因子的剂量效应直接相关,证实15% MS通过优化分泌组组成,有效激活成纤维细胞的ECM重塑功能,为机械力调控真皮再生提供了关键分子证据。
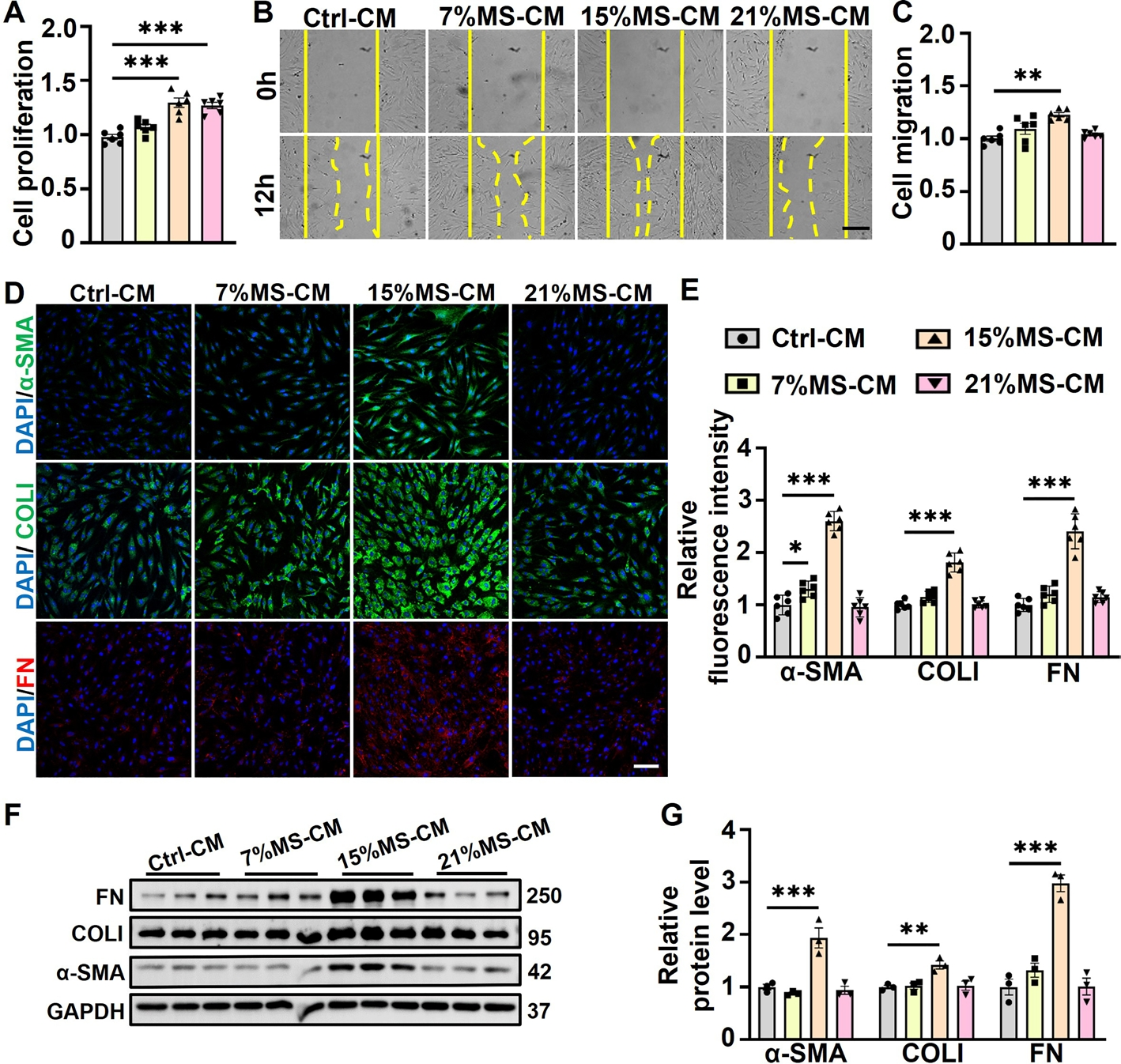
图5 机械拉伸条件培养基对成纤维细胞的调控作用。
最后,研究人员通过小鼠全厚度伤口模型证实,15%MS处理的巨噬细胞分泌组显著加速创面愈合进程(图6A)。与对照组相比,15%MS-CM治疗组在D10、D14、D21的创面闭合率分别提升28%、35%和42%(图6B-C),且D21时实现完全上皮化(图6D-E)。血管生成分析显示,15%MS-CM组CD34+α-SMA+血管样结构数量较对照组增加3.2倍(图6F-G),Masson染色证实其胶原沉积量提升1.8倍(图7A-B)。天狼星红偏振光分析揭示15%MS-CM组I/III型胶原比例较对照组提高2.4倍(图7C-D),提示更成熟的ECM重塑进程。该双重调控机制表明:15%MS通过巨噬细胞分泌组优化,协同促进血管新生与胶原重构,使创面修复进程提前进入重塑期,为开发基于机械力调控的智能敷料提供了关键实验依据。
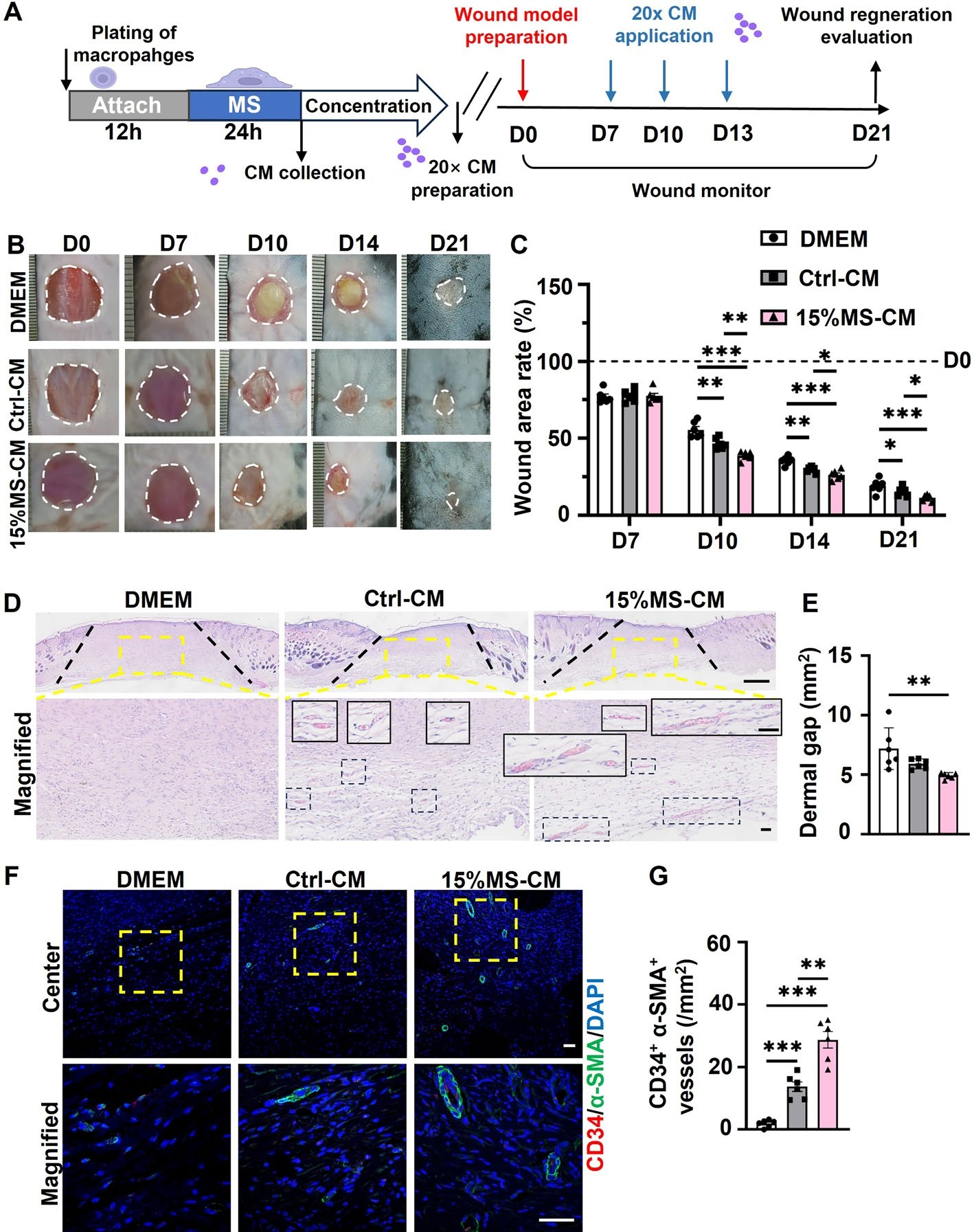
图6 在小鼠伤口模型中,15%机械拉伸条件培养基对伤口愈合及血管生成的影响。
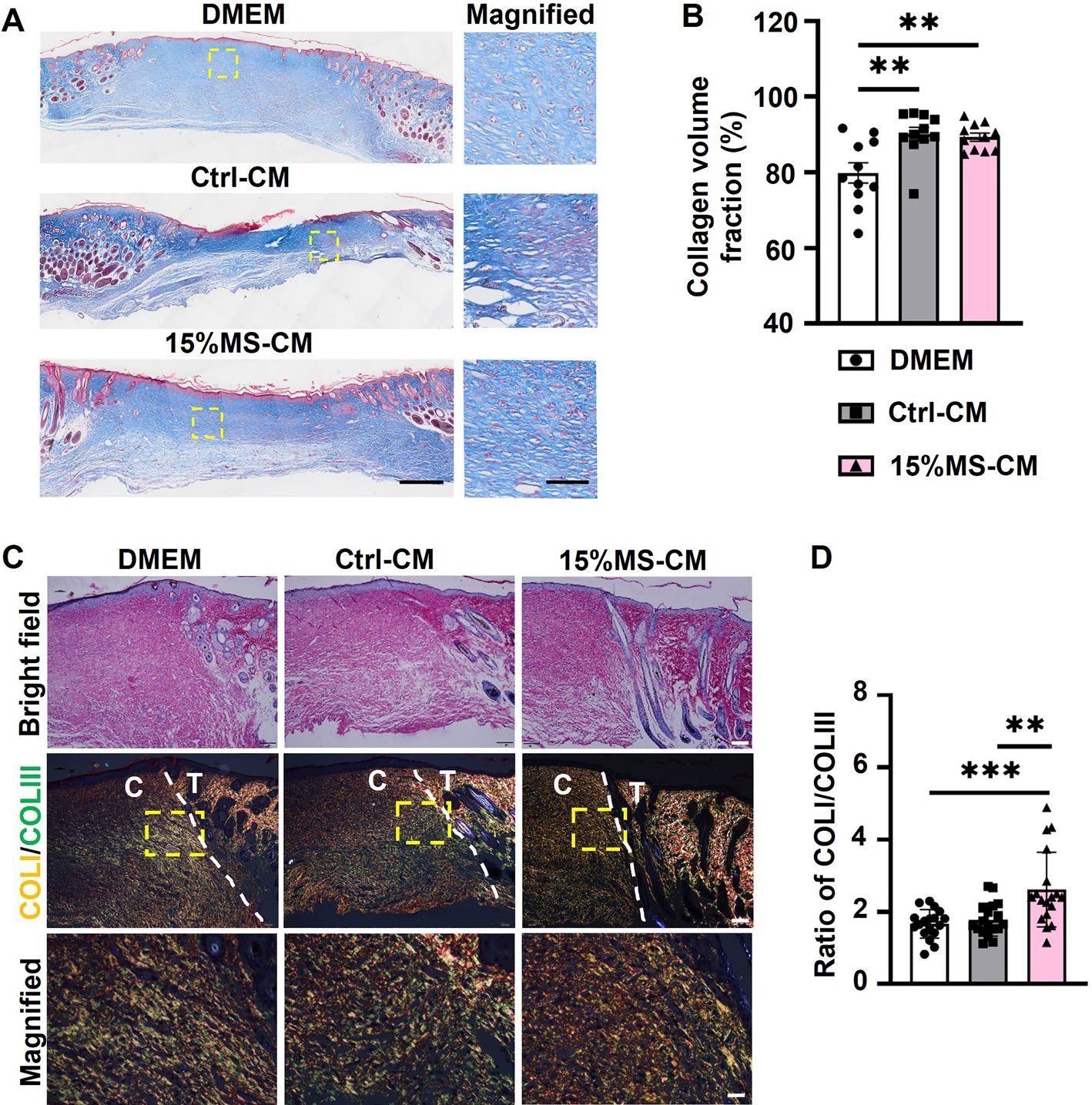
图7 15%的机械拉伸条件培养基提高了再生伤口组织中I型与III型胶原的比值及其沉积量。

图8 图片摘要。
总之,研究揭示了巨噬细胞对机械拉伸(MS)的非单调响应规律及其在皮肤再生中的核心调控作用。巨噬细胞在7-21%静态拉伸强度下呈现双相反应:15% MS显著促进细胞活力、诱导M2极化并激活YAP/TAZ通路,而7%与21% MS效应显著减弱。这种强度依赖性调控通过旁分泌机制重塑皮肤细胞功能,15% MS处理的巨噬细胞分泌组(MS-CM)使角质形成细胞迁移加速1.8倍、内皮血管生成能力增强3.1倍、成纤维细胞胶原合成提升4.1倍。小鼠全层伤口模型证实,15% MS-CM治疗使创面闭合率提高42%,CD34+α-SMA+血管密度增加3.2倍,I/III型胶原比例提升2.4倍,显著加速组织重塑进程。该发现为临床组织扩张术的力学参数优化及智能敷料开发提供了关键理论依据,未来需通过3D器官模型深化机械免疫再生的多组学研究。
参考文献:Wei Q, Du F, Cui J, Xu J, Xia Y, Li S, Deng Q, Xu X, Zhang J, Yu S. Non-monotonic response of macrophages to mechanical stretch impacts skin wound healing. Cell Mol Biol Lett. 2025 Jul 15;30(1):82. doi: 10.1186/s11658-025-00764-0. PMID: 40665211; PMCID: PMC12261726.
原文链接:https://pubmed.ncbi.nlm.nih.gov/40665211/
图片来源:所有图片均来源于参考文献
小编旨在分享、学习、交流生物科学等领域的研究进展。如有侵权或引文不当请联系小编修正。如有任何的想法以及建议,欢迎联系小编。感谢各位的浏览以及关注!进入官网www.naturethink.com或关注“Naturethink”公众号,了解更多相关内容。
点击了解: 牵张应变细胞培养仪
点击了解: 细胞力学刺激培养系统

